Professional Documents
Culture Documents
El PH en La Conservación de Alimentos
Uploaded by
luisc4076567%(9)67% found this document useful (9 votes)
45K views5 pagesOriginal Title
El pH en la conservación de alimentos
Copyright
© Attribution Non-Commercial (BY-NC)
Available Formats
DOC, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
67%(9)67% found this document useful (9 votes)
45K views5 pagesEl PH en La Conservación de Alimentos
Uploaded by
luisc40765Copyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOC, PDF, TXT or read online from Scribd
You are on page 1of 5
El pH en la conservación de alimentos
DEFINICIÓN pH
El pH es un símbolo que indica si una sustancia es ácida, neutra o básica. El pH
se calcula por la concentración de iones de hidrógeno, un factor que controla la
regulación de muchas reacciones químicas, bioquímicas y microbiológicas. La
escala de pH es de 0 a 14. La disolución neutra, tiene un pH de 7, valores
menores de 7 indican una disolución acida y valores superiores a 7 indican una
disolución alcalina.
EFECTO DEL pH SOBRE LOS MICROORGANISMOS
El crecimiento de los microorganismos requiere principalmente de nutrientes,
agua, una
temperatura adecuada y determinados niveles de pH.
En estado natural las frutas tienen pH bastantes ácidos y las verduras, las
carnes y pescados son
ligeramente ácidos.
Los valores bajos de pH (ácido) pueden ayudar en la conservación de los
alimentos de dos maneras: directamente, inhibiendo el crecimiento microbiano,
e indirectamente, a base de disminuir la resistencia al calor de los
microorganismos, en los alimentos que vayan a ser tratados térmicamente.
Los alimentos conservados por acidificación natural (fermentación láctica),
derivan sobre todo de la leche (yogur, queso), de la carne (embutidos
fermentados) y de productos vegetales (coliflor fermentada, encurtidos, etc.).
También se puede inhibir la alteración microbiana de algunos alimentos por
acidificación artificial, por ejemplo, con ácido acético o cítrico, en el caso de
productos vegetales.
El valor de pH igual o inferior a 4,5 es un punto de control crítico (PCC) en el
procesado térmico de alimentos enlatados para inhibir el crecimiento de
Clostridium botulinum. A pH inferiores a 4,2 se controlan casi todos los
microorganismos que producen intoxicaciones alimentarias, pero algunas
levaduras, hongos y bacterias acidolácticas se desarrollan bien a pH inferiores
a éste.
En la mayor parte de las conservas de frutas, al ser naturalmente ácidas,
permiten el empleo de temperaturas inferiores a los 100°C. En el caso de
hortalizas y verduras, con un pH ligeramente mas elevado que las frutas,
necesitan un tratamiento térmico superior a 100ºC en autoclave, o una
acidificación previa hasta pH igual o inferior a 4,5, modificando las
características del medio interno del alimento.
EFECTO SOBRE LOS COMPONENTES DE LOS ALIMENTOS
El pH afecta a muchas propiedades funcionales como son: el color, flavor y
textura de los alimentos. Las pulpas de frutas ácidas con pH inferiores a 3,5
forman geles débiles que tienden a colapsarse. La albúmina del huevo es un
importante ingrediente de los alimentos debido a su capacidad para incorporar
otros ingredientes mediante la formación de una estructura tridimensional del
gel. Las propiedades del gel dependerán entre otras variables del pH. El
comportamiento de las proteínas es claramente dependiente del pH.
CALCULO DE pH
El valor pH es igual al logaritmo negativo de la actividad o concentración
molar de los iones hidrógeno
pH = -log[H+]
Al ser una escala logarítmica, no lineal, un pH de 3,0 es 10 veces más ácido
que un pH de 4,0.
MEDIDA DEL pH:
El instrumento de medida se llama pHmetro. Es un minivoltímetro que mide la
diferencia de potencial entre dos electrodos: un electrodo de referencia
(generalmente de plata/cloruro de plata) y un electrodo de vidrio poroso que es
sensible a la concentración de iones hidrógeno, a una temperatura estable de
20ºC.
También se puede medir de forma aproximada el pH de una disolución
empleando indicadores, ácidos o bases débiles que presentan diferente color
según el pH. Generalmente se emplea papel indicador, que se trata de papel
impregnado de una mezcla de indicadores.
ALGUNOS EJEMPLOS PRÁCTICOS
En el caso de la preparación de una mayonesa, la presencia de una posible
contaminación con Salmonella en el huevo, se puede inhibir si dejamos la
yema en contacto unos minutos con un ácido (limón=acido cítrico o
vinagre=acido acético) y luego hacemos la emulsión con el aceite. Si se realiza
primero la emulsión y luego se agrega el acido, el aceite protege a la
Salmonella y no tendrá ningún efecto inhibidor, solo contribuirá a dar sabor y
fluidez a la mayonesa.
Si preparamos una crema pastelera y realizamos el mismo procedimiento de
poner en contacto las yemas con el zumo del limón, inhibiremos las bacterias y
además, el tratamiento térmico posterior será más efectivo y conseguiremos
un producto con mayor seguridad alimentaria.
Cuando modificamos el pH de una proteína, podemos obtener efectos
beneficiosos, como por ejemplo el agregado de crémor tártaro (tartrato ácido
de potasio) a unas claras frescas favoreciendo el montado de las mismas
(debido a la modificación de la estructura espacial de las proteínas por la
acción del ácido), que favorece la aireación de las claras. Si la cantidad de
ácido agregado a una proteína es elevada y durante un tiempo prolongado,
como es en el caso del cebiche, el acido cítrico desnaturaliza la proteína,
modificando sabor, textura y gusto; es lo que conocemos como una cocción
ácida del pescado.
Para finalizar, los ácidos tienen un efecto antioxidante que evita el
pardeamiento enzimático de las frutas, es el caso de las manzanas o peras con
el zumo de limón. Recordar que las enzimas también son proteínas y por ello se
modifica su estructura por acidificación.
Fuente: www.aulachocovic.es/docs/articles/ph.pdf
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA
CENTRO UNIVERSITARIO DEL SUR
INGENIERIA AGROINDUSTRIAL
PROCESAMIENTO DE ALIMENTOS I
ING. EDDY GONZALEZ
pH en la conservación de los alimentos
Luis Carlos Ordoñez Avila
200540765
You might also like
- Conservacion Mediante La Modificacion de PHDocument17 pagesConservacion Mediante La Modificacion de PHNatalia Colli Gutierrez100% (2)
- Elaboración de Encurtido de PepinilloDocument8 pagesElaboración de Encurtido de PepinilloDilmer Dioner100% (3)
- Practica de AditivosDocument5 pagesPractica de AditivosYessenia Miñope Custodio100% (1)
- Humedad IntermediaDocument3 pagesHumedad Intermedianathy00015100% (1)
- Metodo de Conservacion Por AcidificacionDocument3 pagesMetodo de Conservacion Por AcidificacionANGIE ARLETTE HIDALGO APAZA0% (1)
- Flavor de Los Alimentos CuerpoDocument8 pagesFlavor de Los Alimentos CuerpoFabiola Del Pilar Curo100% (1)
- Evaluacion y Control de Calidad en Los Encurtidos de HortalizasDocument11 pagesEvaluacion y Control de Calidad en Los Encurtidos de HortalizasDavid VictorianoNo ratings yet
- Escaldado de Los AlimentosDocument9 pagesEscaldado de Los AlimentosAdrimarospina85% (13)
- Aditivos Utilizados en La Industria CarnicaDocument5 pagesAditivos Utilizados en La Industria CarnicaSalomon Orjuela SilvaNo ratings yet
- Alimentos de Humedad IntermediaDocument2 pagesAlimentos de Humedad IntermediaKaren MazariegosNo ratings yet
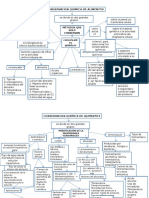
- Mapa Conceptual Conservacion Quimica de AlimentosDocument2 pagesMapa Conceptual Conservacion Quimica de AlimentosGabriela Garcia86% (7)
- Elaboracion de Salsa de TomateDocument9 pagesElaboracion de Salsa de TomateGabriela SamiNo ratings yet
- RECOMENDACIONES EncurtidosDocument2 pagesRECOMENDACIONES EncurtidosGian Cordova CH100% (1)
- El PH en Las FrutasDocument1 pageEl PH en Las Frutasf270171No ratings yet
- Deterioro de Alimentos Practica 2Document11 pagesDeterioro de Alimentos Practica 2erimar ZelaNo ratings yet
- Análisis fisicoquímico mermelada fresaDocument5 pagesAnálisis fisicoquímico mermelada fresaSussan Julca Rondan67% (6)
- Deterioro de Los Alimentos EnlatadosDocument24 pagesDeterioro de Los Alimentos EnlatadosSocorro Elvira Culquicondor Santur67% (6)
- Resultados EncurtidosDocument1 pageResultados EncurtidosFernando CroNo ratings yet
- Laboratorio Nº7ketchupDocument6 pagesLaboratorio Nº7ketchupMelby Gabriela Zarate100% (1)
- Encurtidos No FermentadosDocument5 pagesEncurtidos No FermentadosLuis Eduardo Flórez FlórezNo ratings yet
- LOS 7 PRINCIPIOS HACCPDocument4 pagesLOS 7 PRINCIPIOS HACCPamemora67% (9)
- Apuntes Unidad 2 Reguladores de PHDocument4 pagesApuntes Unidad 2 Reguladores de PHYosse GonzalezNo ratings yet
- Informe - Fermentación de La Col o ChucrutDocument6 pagesInforme - Fermentación de La Col o ChucrutXtian Edú50% (2)
- Pruebas de Seleccion, Reconocimiento de Sabores BasicosDocument5 pagesPruebas de Seleccion, Reconocimiento de Sabores BasicosCindy Arrieta Monzalvo40% (5)
- Dia 1 Vida Anaquel IntroduccionDocument96 pagesDia 1 Vida Anaquel IntroduccionDavid Santaria Vargas50% (2)
- CUESTIONARIODocument10 pagesCUESTIONARIOKarol Lizbeth Yanarico Fernández100% (2)
- Salsa KetchupDocument16 pagesSalsa Ketchupmitzi milagrosNo ratings yet
- Tecnologia de Alimentos CarbohidratosDocument3 pagesTecnologia de Alimentos CarbohidratosFernando Miranda PerezNo ratings yet
- Indice de ReichertDocument6 pagesIndice de ReichertcjcarvajalcNo ratings yet
- Proceso de pelado químico de frutas y hortalizasDocument11 pagesProceso de pelado químico de frutas y hortalizasIda Marisol Zapata CarrascoNo ratings yet
- PRACTICA-Elaboracion de Salsa Ketchup y Alverjas en SalmueraDocument9 pagesPRACTICA-Elaboracion de Salsa Ketchup y Alverjas en SalmueraelnapbNo ratings yet
- Parametros Intrinsecos y ExtrinsecosDocument5 pagesParametros Intrinsecos y ExtrinsecosCris Mora80% (15)
- Elaboración de cátsup de Tomate: Proceso, Nutrición y BeneficiosDocument10 pagesElaboración de cátsup de Tomate: Proceso, Nutrición y BeneficiosPablo RafaelNo ratings yet
- Encurtidos en VinagreDocument28 pagesEncurtidos en VinagreLiz Calderon MolloNo ratings yet
- Mecanismos generación sabores olores alimentosDocument21 pagesMecanismos generación sabores olores alimentosClaudia Murillo CzNo ratings yet
- Practica de Frutas en AlmibarDocument6 pagesPractica de Frutas en AlmibarRossy RJ50% (2)
- ELABORACIÓN DE EscabecheDocument9 pagesELABORACIÓN DE Escabechejonathan0% (1)
- Metodos de Conservacion-CuradoDocument17 pagesMetodos de Conservacion-CuradoEloy Tristan Gonzales100% (1)
- Fundamento Teorico de Nectar de ManzanaDocument3 pagesFundamento Teorico de Nectar de ManzanaSheilly BravoNo ratings yet
- Ensayo Alimentos FuncionalesDocument5 pagesEnsayo Alimentos FuncionalesBetza TroyaNo ratings yet
- Espectofotometrìa y Determinacion de PH en Jugos de FrutasDocument6 pagesEspectofotometrìa y Determinacion de PH en Jugos de FrutasMario Morales0% (1)
- Evaluación Sensorial (Pruebas de Umbral)Document4 pagesEvaluación Sensorial (Pruebas de Umbral)Javier CantilloNo ratings yet
- La Biotecnologia en Los ColorantesDocument2 pagesLa Biotecnologia en Los ColorantesJeimy Lizeth Arias MontenegroNo ratings yet
- Factores Intrinsecos y ExtrinsecosDocument10 pagesFactores Intrinsecos y ExtrinsecosjosueNo ratings yet
- Conservación de Los Alimentos Por AzúcaresDocument5 pagesConservación de Los Alimentos Por AzúcaresDaniel VargasNo ratings yet
- Acidulantes - Alcalinizantes y Reguladores de PHDocument17 pagesAcidulantes - Alcalinizantes y Reguladores de PHAleja Jaramillo100% (1)
- Marco TeóricoDocument9 pagesMarco TeóricoAlex Luna Salazar0% (1)
- Práctica 2-Mermelada de PiñaDocument15 pagesPráctica 2-Mermelada de PiñaDayan Ch J33% (3)
- POES Horno, Anafe y MarmitaDocument6 pagesPOES Horno, Anafe y MarmitaEstudia NutriNo ratings yet
- Análisis Sensorial de AlimentosDocument57 pagesAnálisis Sensorial de AlimentosNelly Lopez Barbery86% (7)
- Esterilización alimentos métodosDocument9 pagesEsterilización alimentos métodosWesRes100% (2)
- Carne - PH Marco TeoricoDocument4 pagesCarne - PH Marco TeoricoCristopherEsquivelSaavedra100% (1)
- La Limpieza y Desinfección EmbutidosDocument35 pagesLa Limpieza y Desinfección EmbutidosHilary Kelly0% (2)
- Determinacion de PH y Acidez Titulable AngireDocument14 pagesDeterminacion de PH y Acidez Titulable AngireJesus Cornejo BurgosNo ratings yet
- Universidad Nacional de Frontera de Sullana: Facultad de Ingeniería de Industrias AlimentariasDocument9 pagesUniversidad Nacional de Frontera de Sullana: Facultad de Ingeniería de Industrias AlimentariasJefferson Jesús Zapata CamachoNo ratings yet
- Determinación pH AlimentosDocument12 pagesDeterminación pH AlimentosBrayan TorresNo ratings yet
- Nivel de PH en Conservas - TeffaDocument2 pagesNivel de PH en Conservas - TeffaEder ApazaNo ratings yet
- 1-Ph de Los AlimentosDocument19 pages1-Ph de Los AlimentosAdriana Marianela QA100% (1)
- Guía de laboratorio No. 3Document9 pagesGuía de laboratorio No. 3GeraldinecarNo ratings yet
- Determinación de pH, acidez y pK en alimentosDocument9 pagesDeterminación de pH, acidez y pK en alimentosMiyey Gutierrez OrduzNo ratings yet
- Cristalografia 1-2Document10 pagesCristalografia 1-2Ader Rada ValdizanNo ratings yet
- Reporte de La Actividad de SolubilidadDocument6 pagesReporte de La Actividad de SolubilidadwendyNo ratings yet
- Bibliografía y seguridad en soldaduraDocument83 pagesBibliografía y seguridad en soldaduraGuzmanPomaGiovannyNo ratings yet
- ElctrirepasoDocument17 pagesElctrirepasoDar MendezNo ratings yet
- Guía Práctica #03 Máquinas EléctricasDocument7 pagesGuía Práctica #03 Máquinas EléctricasJheremitNo ratings yet
- Tablas Dinamica de FluidosDocument11 pagesTablas Dinamica de FluidosRicardo CruzNo ratings yet
- Tipos de Suelo Por Su OrigenDocument4 pagesTipos de Suelo Por Su OrigenyudiNo ratings yet
- Previo. Caidas de PresionDocument6 pagesPrevio. Caidas de PresionDavid Ramirez TorresNo ratings yet
- La Tienda de Don ChuchoDocument53 pagesLa Tienda de Don ChuchonnNo ratings yet
- Cinética Química. Soluciones Ejercicios PDFDocument16 pagesCinética Química. Soluciones Ejercicios PDFgeovadis meza garridoNo ratings yet
- Metalurgia Extractiva de Metales No Ferrosos PDFDocument3 pagesMetalurgia Extractiva de Metales No Ferrosos PDFTexx TexxNo ratings yet
- Examen Ingenieria AmbientalDocument9 pagesExamen Ingenieria AmbientalMelidy Eided Hinostroza Mitacc100% (1)
- Proyecto 1Document19 pagesProyecto 1Jose Manuel Herrera ChavezNo ratings yet
- Cuáles Son Las Subramas de La FísicaDocument3 pagesCuáles Son Las Subramas de La FísicaOswaldo Gámez100% (1)
- Mquiz 1 - Semana 3 - CB - PRIMER BLOQUE-FLUIDOS Y TERMODINAMICA - (GRUPO3)Document5 pagesMquiz 1 - Semana 3 - CB - PRIMER BLOQUE-FLUIDOS Y TERMODINAMICA - (GRUPO3)faberNo ratings yet
- FT Gaia Shotcrete EsDocument2 pagesFT Gaia Shotcrete Esvolcom_carNo ratings yet
- Cálculo Condensaciones - DITEC - V2.17Document40 pagesCálculo Condensaciones - DITEC - V2.17carolinaperez10% (1)
- Evaluación N 1 - 285425 - FÍSICO QUÍMICA - CPEL 2023-00 - M1-PRELMCIIN04A1Document6 pagesEvaluación N 1 - 285425 - FÍSICO QUÍMICA - CPEL 2023-00 - M1-PRELMCIIN04A1alex canoNo ratings yet
- Cap6. Deshidratacion Del Gas Natural I-2020 PDFDocument99 pagesCap6. Deshidratacion Del Gas Natural I-2020 PDFRoly LopezNo ratings yet
- Ii Examen de Análisis Instrumental PDFDocument2 pagesIi Examen de Análisis Instrumental PDFLina Chavez OrtegaNo ratings yet
- Geología y Meteorología de Gran CanariaDocument3 pagesGeología y Meteorología de Gran CanariaEladio MurcianoNo ratings yet
- Retro Ejercicios Calculos U2 Ad17Document12 pagesRetro Ejercicios Calculos U2 Ad17Jose EcNo ratings yet
- TP04b-BEAb - 23Document2 pagesTP04b-BEAb - 23Daniel Roman CoronelNo ratings yet
- Acumuladores y Su FuncionamientoDocument4 pagesAcumuladores y Su FuncionamientoAshley MartinezNo ratings yet
- Informe Lab. Movimiento en Un PlanoDocument4 pagesInforme Lab. Movimiento en Un PlanoAriadna Carrillo0% (1)
- Taller Tercer Corte - Semana 12-15Document13 pagesTaller Tercer Corte - Semana 12-15Steven Martinez RodriguezNo ratings yet
- CuestionarioDocument4 pagesCuestionarioZaida Anabel Valarezo AstudilloNo ratings yet
- 2.2 Flujo de Energía 5 KDocument11 pages2.2 Flujo de Energía 5 KSalvador Perez MezaNo ratings yet
- Destilación Fundamentación TeoricaDocument9 pagesDestilación Fundamentación TeoricaGERALDINE URBANO SANDOVALNo ratings yet
- Examen ResueltoDocument3 pagesExamen ResueltoJesus Ricardo RodriguezNo ratings yet