Professional Documents
Culture Documents
Informe de Quimica Laboratorio
Uploaded by
Pedro Rubio GallardoOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Informe de Quimica Laboratorio
Uploaded by
Pedro Rubio GallardoCopyright:
Available Formats
Universidad de Chile Facultad de Ciencias Laboratorio de Qumica
Dimensiones Moleculares Estimacin del numero de Avogadro
Nombres: Vicente Muoz Pedro Rubio Carrera: Licenciatura en ciencias con mencin en qumica
Parte experimental I. Materiales Bandeja de plstico Etanol Pipeta Parcial Agua potable Licopodio Acido oleico Hielo
II. Procedimiento - Se debe conocer el volumen de una gota de la solucin que depositara para formar la monocapa por lo tanto, previamente tendr que calibrar la pipeta. Siga las instrucciones, entregadas por su profesor de laboratorio, - Agregue agua a una bandeja; de tal forma que cubra su superficie sin que esta se derrame. Cuando sta est quieta, espolvoree su superficie polvos talcos, licopodio u otros. - Agregue exactamente 1 gota: de solucin; de acido oleico sobre el centro de la superficie. Mida varios dimetros de la mancha, tal que el promedio de ellos sea representativo o confiable. - Anote la concentracin de la solucinele acido oleico utilizada. - Lave la bandeja con detergente y agua, y repita: el experimento. Si la diferencia entre los dos dimetros promedio es mayor que 2 cm., repita el experimento una vez ms. III. Preguntas 1. Calcule el rea de la monocapa utilizando el promedio de los dimetros asumiendo una circunferencia. (A= r 2) R: Asumiendo que la forma de la monocapa es circular, la superficie formada debe ser sacada por la formula A= r2 . Habiendo medido previamente el radio de la monocapa, se puede calcular el rea de la circunferencia formada en la bandeja:
A = r2 A = (3,2)2 A = 32,17 cm2 Por lo tanto el rea de la circunferencia es de 32,17cm2.
2. Calcule el volumen de cido puro en la monocapa de acido graso. R: Al pipetear 1cc pudimos determinar el nmero de gotas contenidos en este volumen y a si el volumen de la gota (0.022 cc), luego pudimos determinar los moles en 1 gota por proporcin con la concentracin molar obtenida al inicio de acido oleico (1.52 x 10-3 M).
X= 0.022 cc x 1.52 x 10-3 M 1000 cc
X= 3.34 x 10-8 mol.
Con esta informacin y la masa molar del acido oleico dado al inicio se puede determinar la masa contenida en una gota
masa masa molar 3.34 x 10-8 mol = masa /282.5 g/mol masa = 9.44 x10-6 g.
mol =
Conociendo la masa y la densidad del acido oleico se puede determinar el volumen densidad = masa / volumen 0.895 g/cc = (9.44 x10-6 g) / volumen volumen = 1.05 x10-5 cc
Por lo tanto se determina que el volumen de acido oleico puro en la monocapa es de 1.05 x10-5 cc. 3.-Calcule la altura de la capa, sabiendo que. Volumen=base x altura R: Conociendo el rea de la circunferencia y el volumen de la monocapa de acido oleico se puede calcular la altura de la capa volumen = base x altura 1.05 x10-5 cc = 32,17 cm2 x altura Altura = 3.26 x 10-7 cm
4. Suponga los siguientes: modelos de molcula: para el clculo, a. Que las molculas de cido oleico sean cbicas R:
Volumen molcula = h3= 3.46 x 10
-20
cc
N de molculas= Volumen Total = 1.05 x10-5 = 3.034x1014 Volumen molcula 3.46 x 10 -20 N de Avogadro= N de molculas 3.034x1014 = = 9.08 x 1021 -8 N de moles 3.34 x 10
b. Que sean esfricas R:
h = Radio 2 Volumen molcula = 4r3= 1.0 x 10-20 cc 3 N de moleculas= Volumen Total = 1.05 x10-5 = 1.05 x 1015 Volumen molcula 1.0 x 10-20 N de avogadro = N de molculas 1.05 x 1015 = = 3.14 x 1022 N de moles 3.34 x 10-8
c. Que sean cilndricas. suponga que la altura de la molcula es 10 veces el radio m olecular { esqueleto.'C-C, de form a helicoidal). el es
R:
Volumen molcula = A
basal
x h = 1.1 x 10
-21
cc
N de moleculas= Volumen Total = 1.05 x10-5= 9.54 x 1015 Volumen molcula 1.1 x 10
-21
N de avogadro = N de molculas 9.54 x 1015 = = 2.85 x 1023 -8 N de moles 3.34 x 10
5. Qu efecto tendr en sus: resultados si la pelcula no fuera una monocapa? R: En el caso que fuera una bicapa, el nmero de Avogadro se debera de realizar de la misma forma, pero cambiara la altura de la capa y tendra que reformular la estructura de la molcula y tambin la masa molar que debera aumentar. En el caso de la tricapa el proceso es similar, calcular la altura de la molcula y de las capas, luego el rea y as sucesivamente. Pero deber tener la misma capacidad de formar un cuerpo geomtrico de volumen calculable (Un cilindro pero con distintas capas).
6.- Es nmero de Avogadro calculado ser mayor o menor si e! esqueleto de carbono de la molcula, no es perpendicular a la superficie del agua. R: Si la molcula no tomara la forma perpendicular, es decir, cambiara el grado de inclinacin de la molcula con respecto a la superficie con agua, cambiaria el proceso de calculo del rea, porque la altura de la molcula va a disminuir y tambin la superposicin de las molculas. Al realizar el calculo del numero de Avogadro nos daremos cuenta que es mayor, por las siguientes razones:
El volumen de la molcula ser menor al normal, ya que la altura disminuira. Al hacer la operacin del clculo del nmero de molculas da un nmero ms grande al disminuir el volumen de la molcula. Posteriormente al hacer la relacin con el nmero de molculas (Que ser menor) y el nmero de moles, el nmero de avogadro aumentar.
7.- Calcule la superficie de agua que cubrira un mol de cido oleico R: Con los datos conocidos de cuanto cubre 1 gota de acido oleico queda la siguiente relacin de proporcionalidad:
3.34 x 10-8 mol = 1 mol 32.17 cm2 X= 0.96 x 109 Por lo tanto el area de que cubriria 1 mol de acido oleico es: 0.96 x 109 8,- Se ha sugerida que las monocapas de acida grasos, podran ser utilizadas para reducir la perdida de agua por evaporacin de los reservorios, Calcule la masa de cido oleico necesaria para cubrir la superficie de un reservorio natural de 100 Km2. (Superficie aproximada del lago Rapel) R: Conociendo el rea a cubrir que son 100 km2 y la densidad del acido oleico y la altura de la molcula se puede realizar las siguientes relaciones: rea= 100 km2 = 1 x 1012 cm2 Densidad del acido oleico= 0.895 g/cc Altura= 3.26 x 10-7 cm rea x Altura = Volumen 1 x 1012 cm2 x 3.26 x 10-7 cm = 326000 cc Densidad = Masa Volumen 0.895 g/cc = Masa 326000 cc Masa= 291770 g x
You might also like
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- Solucionario de Mecanica de FlidosDocument427 pagesSolucionario de Mecanica de FlidosAmérico Rumín67% (15)
- Desconexion ParticularDocument1 pageDesconexion ParticularRonald Monzón100% (1)
- Atención Telefónica 2018Document51 pagesAtención Telefónica 2018Garfield Salas MorisNo ratings yet
- Ponchado de CablesDocument12 pagesPonchado de Cablesestiven_cobosNo ratings yet
- Ejercicios de espectrofotometría y cálculos de concentraciónDocument2 pagesEjercicios de espectrofotometría y cálculos de concentraciónricardoNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Lav. Quim N°5Document14 pagesLav. Quim N°5benjamin quijaiteNo ratings yet
- Estimación del Número de Avogadro a través de la Dimensión MolecularDocument10 pagesEstimación del Número de Avogadro a través de la Dimensión MolecularPaloma FuenzalidaNo ratings yet
- PROBLEMAS DE QUÍMICA Y FÍSICA RESUELTOSDocument131 pagesPROBLEMAS DE QUÍMICA Y FÍSICA RESUELTOSLeonardo Suarez Mollinedo30% (10)
- Cuestionario DASHDocument6 pagesCuestionario DASHPaula Ortiz OyarzunNo ratings yet
- Manual de Buceo (III) - Armada de ChileDocument129 pagesManual de Buceo (III) - Armada de ChileCarlos Arturo Martinez Salcedo100% (1)
- Introduccion ProgramacionDocument317 pagesIntroduccion ProgramacionMiguelNo ratings yet
- Preparación de soluciones: concentración y cálculosDocument6 pagesPreparación de soluciones: concentración y cálculos1lvaro1javier1mej1a1100% (7)
- 2bachillerato QuimicaDocument146 pages2bachillerato QuimicaIsel Nufio40% (5)
- Informe de Laboratorio 2 QuimicaDocument13 pagesInforme de Laboratorio 2 QuimicaAlfonsoAndrésTolozaAcevedo33% (3)
- LabDocument19 pagesLabCamy RabioliNo ratings yet
- Adsorción de Ácido Acético Con Carbón ActivadoDocument26 pagesAdsorción de Ácido Acético Con Carbón ActivadoAndres Garcia OcampoNo ratings yet
- Capa MonomolecularDocument8 pagesCapa MonomolecularIanNo ratings yet
- Práctica Química - Determinación Del Número de AvogadroDocument5 pagesPráctica Química - Determinación Del Número de Avogadrodani_1806_fanton0% (1)
- ESTEQUIOMETRIADocument16 pagesESTEQUIOMETRIARomario Quiroz ChaverraNo ratings yet
- Química 4° Año: Iii Momento PedagógicoDocument13 pagesQuímica 4° Año: Iii Momento PedagógicoJose Daniel GomezNo ratings yet
- Informe N°2 de QuimicaDocument2 pagesInforme N°2 de QuimicaEdna Rocio Robles FigueroaNo ratings yet
- Propiedades de Los SólidosDocument19 pagesPropiedades de Los SólidosLina M CastroNo ratings yet
- PDF Solucionario de Mecanica de Flidos - CompressDocument20 pagesPDF Solucionario de Mecanica de Flidos - CompressYEHIKO ALEXANDER HERNANDEZ DIAZNo ratings yet
- Coleccion de Ejercicios Con SolucionDocument179 pagesColeccion de Ejercicios Con SolucionacobosaNo ratings yet
- Manual Practicas Quimica IIDocument121 pagesManual Practicas Quimica IIluisgutierres100% (1)
- Practica - 4 - Numero de AvogadroDocument4 pagesPractica - 4 - Numero de AvogadroalexNo ratings yet
- Practica 1 Numero de Avogadro y El Concepto de MolDocument4 pagesPractica 1 Numero de Avogadro y El Concepto de MolCelia Magdaleno RuvalcabaNo ratings yet
- ParcialDocument2 pagesParcialAngelo VarelaNo ratings yet
- Clave Tercer Examen Parcial Q4 2010Document11 pagesClave Tercer Examen Parcial Q4 2010Paula Ximena Monterroso RojasNo ratings yet
- Prácticas de Laboratorio FisicoquímicaDocument41 pagesPrácticas de Laboratorio Fisicoquímicajunior jimenezNo ratings yet
- Taller Quimica Catalina FlorezDocument8 pagesTaller Quimica Catalina FlorezAlejandro Castillo VélezNo ratings yet
- Determinación del volumen molar de un gasDocument20 pagesDeterminación del volumen molar de un gasMaría100% (1)
- LABORATORIO 06-Química para MineriaDocument12 pagesLABORATORIO 06-Química para MineriaEver Lima choqueNo ratings yet
- Ley de Beer: Curva de Calibración.Document10 pagesLey de Beer: Curva de Calibración.landecomNo ratings yet
- Determinación de la concentración de ácido acético en vinagre mediante titulación ácido-baseDocument12 pagesDeterminación de la concentración de ácido acético en vinagre mediante titulación ácido-baseFelix Santiago100% (2)
- Guia de LboratoriosDocument94 pagesGuia de LboratoriosLuiggy LopezNo ratings yet
- Cuestionario QuimicaDocument9 pagesCuestionario QuimicaRafael VargasNo ratings yet
- 1º Examen de QuimicaDocument4 pages1º Examen de QuimicaRamiro Q LluscoNo ratings yet
- Pract 09 de ReaccionesDocument12 pagesPract 09 de ReaccionesJean Pierre Cirilo SosaNo ratings yet
- Ejercicios PrefasDocument20 pagesEjercicios PrefasRigoberto CallisayaNo ratings yet
- Espectrofotometría de Absorción AtómicaDocument8 pagesEspectrofotometría de Absorción AtómicaCotheWestBourgeoisNo ratings yet
- PDF 12 VolumenesDocument12 pagesPDF 12 VolumenesSergio De La Calle RomeroNo ratings yet
- UNIDADES CONCENTRIONDocument3 pagesUNIDADES CONCENTRIONCarmen RodríguezNo ratings yet
- Taller Ingfluidos 2Document4 pagesTaller Ingfluidos 2Daniel BedoyaNo ratings yet
- IPN Esm Bioca 1Document16 pagesIPN Esm Bioca 1elena floresNo ratings yet
- Boletin 7 Fenomenos de Superficie-24Document1 pageBoletin 7 Fenomenos de Superficie-24martamaesstuNo ratings yet
- Tarea Preparatoria 1Document6 pagesTarea Preparatoria 1Alex BernalNo ratings yet
- EJERCICIOS Transferencia CalorDocument3 pagesEJERCICIOS Transferencia CalorFabian PulgarNo ratings yet
- Análisis Espectrofotométrico de Un Metal en AleaciónDocument7 pagesAnálisis Espectrofotométrico de Un Metal en Aleaciónabi100% (1)
- Pre2 - Daniela Rodriguez324519Document6 pagesPre2 - Daniela Rodriguez324519Alejandra RodriguezNo ratings yet
- PT Ciencias común + Química electivo: guía de práctica de transiciónDocument33 pagesPT Ciencias común + Química electivo: guía de práctica de transiciónFrancisca Camila Oyarzún KomoriNo ratings yet
- Actividades de AprendizajeDocument14 pagesActividades de Aprendizajeafrich81No ratings yet
- Informe 7. Isoterma de Adsorcion WuuuDocument13 pagesInforme 7. Isoterma de Adsorcion WuuumariaNo ratings yet
- Difusión de Gases EjerciciosDocument27 pagesDifusión de Gases EjerciciosJorge Rodriguez MegoNo ratings yet
- 4° Medio QuímicaDocument7 pages4° Medio QuímicaMarcela YusefNo ratings yet
- Ejercicios PrefasDocument19 pagesEjercicios PrefasRigoberto CallisayaNo ratings yet
- Aireacion Por DifusionDocument7 pagesAireacion Por DifusionBryan RiveraNo ratings yet
- Soluciones TreybalDocument27 pagesSoluciones TreybalHéctor Medina OviedoNo ratings yet
- Determinación del Número de Avogadro a través de una capa monomolecular de aceite de olivaDocument6 pagesDeterminación del Número de Avogadro a través de una capa monomolecular de aceite de olivataniarom14No ratings yet
- Maquina de AtwoodDocument3 pagesMaquina de AtwoodPedro Rubio GallardoNo ratings yet
- Malla Quí LicDocument1 pageMalla Quí LicPedro Rubio GallardoNo ratings yet
- Fx115MS 991MS SpanishDocument44 pagesFx115MS 991MS SpanishAqueronteBlog50% (2)
- Como Hacer EBI A4 FinalDocument28 pagesComo Hacer EBI A4 FinalPedro Rubio GallardoNo ratings yet
- Informe de La MaquetaDocument8 pagesInforme de La MaquetaJulio PerezNo ratings yet
- Toshiba Aire Tarifa Reducida 2020Document35 pagesToshiba Aire Tarifa Reducida 2020VEMATELNo ratings yet
- PORTAFOLIO DE TRABAJOS DE ARQUITECTURA 2013, Arq Oscar Daniel Contreras CaroDocument31 pagesPORTAFOLIO DE TRABAJOS DE ARQUITECTURA 2013, Arq Oscar Daniel Contreras Carooscar daniel contrerasNo ratings yet
- Guion Introducción CanalDocument3 pagesGuion Introducción CanalJamesNo ratings yet
- MEMO. CIRC. #014-2020 (VALIDO) Alex OroscoDocument19 pagesMEMO. CIRC. #014-2020 (VALIDO) Alex OroscoAlex Franz Orosco QuintanaNo ratings yet
- MTV 13 Estado Situación FinancieraDocument20 pagesMTV 13 Estado Situación FinancieraelvisNo ratings yet
- Mem ArquitecturaDocument4 pagesMem ArquitecturakattesheyNo ratings yet
- Flamencos y sus medias de víboraDocument11 pagesFlamencos y sus medias de víboraJuan Felipe HernandezNo ratings yet
- Trabajo Final Sssro YoysiDocument19 pagesTrabajo Final Sssro YoysiMile JavierNo ratings yet
- Roles en El Desarrollo de SoftwareDocument30 pagesRoles en El Desarrollo de SoftwareMáximo SoriaNo ratings yet
- Intervenciones de Enf Estado Hiperosmolar HiperglucémicoDocument6 pagesIntervenciones de Enf Estado Hiperosmolar HiperglucémicoMaye Trillo CarranzaNo ratings yet
- Pintura sobre sal: aprende una nueva técnica artísticaDocument2 pagesPintura sobre sal: aprende una nueva técnica artísticaAUGUSTONo ratings yet
- Manual de Garantia y Mantenimiento Skuty LED LineaDocument47 pagesManual de Garantia y Mantenimiento Skuty LED Lineajulian canoNo ratings yet
- LEXICOLOGIAICDDocument5 pagesLEXICOLOGIAICDAhrix SanderNo ratings yet
- Animación 2D: Clásicos y actualesDocument4 pagesAnimación 2D: Clásicos y actualesLeo OelNo ratings yet
- Grupo Serel - Solaqueo de Ducto de Asc - 18 01 23Document1 pageGrupo Serel - Solaqueo de Ducto de Asc - 18 01 23German Pos PaNo ratings yet
- Alfabetización Digital Un Reto de TodosDocument16 pagesAlfabetización Digital Un Reto de TodosLuli MartinezNo ratings yet
- Monografía - RealidadDocument46 pagesMonografía - RealidadCARLOS ANTONIO TORIBIO BOBADILLANo ratings yet
- Examen Matemáticas III 2da VueltaDocument3 pagesExamen Matemáticas III 2da VueltaWenzel Dietrich ValentinaNo ratings yet
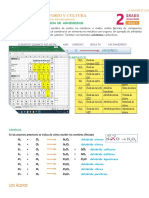
- Formación de anhídridos y ácidosDocument6 pagesFormación de anhídridos y ácidosVictor Raul Torres PerezNo ratings yet
- Simulacio Tiempo Real Protecciones en SEPDocument3 pagesSimulacio Tiempo Real Protecciones en SEPJavier Madrigal OviedoNo ratings yet
- Los TerremotosDocument2 pagesLos Terremotoswilliam OCHOA ESPIRITUNo ratings yet
- Destaque Gamonal 21Document2 pagesDestaque Gamonal 21Rufina Danaith Asencio PomaNo ratings yet
- Moldeo de Metales en Estado Semi So LidoDocument4 pagesMoldeo de Metales en Estado Semi So LidoWilliam AguilarNo ratings yet