Professional Documents
Culture Documents
Titulação potenciométrica de aminoácidos
Uploaded by
Pedro MarizOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Titulação potenciométrica de aminoácidos
Uploaded by
Pedro MarizCopyright:
Available Formats
******************************************* ******** DEPARTAMENTO DE QUMICA
BIOQUMICA EXPERIMENTAL PRTICA 1: PROPRIEDADES CIDO-BASE DE AMINOCIDOS
GRUPO 20 NOMES: ************* ****************
***************, ** DE *** DE ****
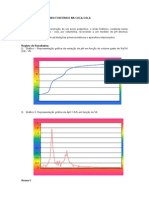
TITULAO POTENCIOMTRICA Os aminocidos esto presentes em todos os seres-vivos e podem ser ligados para formar polmeros muito grandes, as protenas, que possuem papel essencial em nosso organismo. Por isso, de grande importncia que estudemos os aminocidos. Uma propriedade que todo aminocido possui de ser anfotrico, ou seja, eles so ionizados tanto em meio cido quanto em meio bsico, caracterstica que vem da presena de um grupo amino e um grupo carboxila. Com isso, sabemos que todo aminocido tem pelo menos dois valores de pKa, mas pode possuir mais caso sua cadeia possua mais algum grupo ionizvel alm dos caractersticos de aminocidos. Quando se trata de valores de pKa, podemos utilizar a titulao potenciomtrica para realizar experimentos simples e eficientes para estuda-los. Essa tcnica se baseia em uma paulatina adio de uma base forte ou um cido forte numa soluo contendo nosso analito, no caso, um aminocido. Com isso, obtemos valores de pH e seus respectivos volumes de adio; os pHs nos do uma ideia do comportamento cido base do aminocido, enquanto que o volume nos indica quantos mols de cido/base foram adicionados, desde que se conhea a sua concentrao exata. Numa titulao potenciomtrica, usa-se uma bureta para se saber o volume adicionado e um eletrodo para se saber a quantidade de certa espcie em soluo. No caso de nosso experimento, a espcie observada foi o hidrnio (H+), portanto o eletrodo usado foi um pH-metro. Com os dados, fomos capazes de construir um grfico de titulao, que foram comparados com a literatura. Nosso grfico e o comparativo da literatura esto em anexo. A titulao que fizemos foi de cido glutmico com cido clordrico e com hidrxido de sdio. Observando os dois grficos lado a lado, pode-se perceber a semelhana em praticamente todos os pontos, menos nos extremos. Em nossa titulao, a partir de 6 mols de HCl adicionados (-6 no grfico) o valor tende a se estabilizar em pH quase 2, da mesma forma que acontece a partir 3 mols de NaOH (+3 no grfico) se estabilizando em pH 12. Isso ocorre devido sensibilidade do aparelho, que comea a ficar imprecisa, e ao pH das solues adicionadas, que podem no ser suficientes para alterar a partir de certo ponto. A segunda derivada de nosso grfico indica os pontos de inflexio, sendo que quando a segunda derivada vai de negativa para positiva, tem-se uma inflexio cuja concavidade muda de baixo para cima, o que caracteriza os pontos de pKa. Com uma analise dos grficos, pode-se observar que isso ocorre prximo aos valores de pKa pesquisados na literatura: pKa pK1 pK2 pK3 Literatura 2,19 4,25 9,67 Experimental 2,27 4,11 9,79 Erro relativo percentual 3,7 % 3,3 % 1,2 %
Os dados experimentais foram obtidos com o auxlio do programa OriginLab 8.6.
O experimento tambm permitiu a observao do carter tamponante do cido glutmico. Os aminocidos possuem esse carter ter grupos cidos/bsicos fracos, evitando que o pH se altere drasticamente quando se est prximos de algum de seus pKas. O grfico ilustra o tamponamento; nele, nota-se que os pontos prximos dos pKas (marcados com um + vermelho) so os que sofrem menos variao no eixo Y, ou seja, menos alterao em seu pH, seja para maior ou para menor (as extremidades no contam pois so devidas a erros de equipamento). Isso ocorre devido ao equilbrio cido/base de cada um dos grupos ionizveis do cido glutmico (esquema mostrado em anexo); a adio de cido, por exemplo, no protonar todos os stios de todas as molculas do aminocido, haver um equilbrio. Numa soluo sem o cido glutmico, a quantidade base, por exemplo, adicionada seria totalmente refletida no pH, porm, com o cido fraco, chegar um certo pH (o prximo a seu pKa) que a base adicionada comear a ser parcialmente neutralizada pelo cido, e isso causar uma resposta menor no pH. Resumidamente, nosso experimento foi muito satisfatrio, obtivemos resultados prximos da literatura com apenas um experimento, sem duplicata ou triplicata. Conseguimos perceber a caracterstica tamponante do cido glutmico e observar isso na curva de titulao. Para melhorar os resultados, poderamos adicionar mais lentamente, principalmente na rea de interesse, sendo essa a dos pKas ou a do ponto de equivalncia. Alm disso, com um equipamento melhor e cidos e bases diferentes poderamos obter resultados experimentais excelentes. Questes: 1234Escrever a mo, baseado no da literatura. Lembrar de setas no grficos para por a mo. No texto 2,2 2,7; 4,0 4,6; 9,7 10,5. Olhando para o grfico, pode se ver que essas regies so as de menor variao do pH (excluindo as extremidades que esto fora da realidade), o que justifica a possibilidade de utilizar como tampo.
CROMATOGRAFIA EM PAPEL A cromatografia em papel consiste em uma tcnica de separao baseada na diferena de solubilidade entre as amostras e as molculas de gua de hidratao no entorno das fibras de celulose do papel de filtro que constitui a fase estacionria, enquanto arrastadas durante a passagem de um solvente que age como fase mvel. Ao colocar o papel sobre o solvente de Partridge, o solvente absorvido pelo papel e percorre lentamente sua superfcie. Em nvel microscpico podemos entender esse fenmeno pela constante realocao das molculas do solvente na regio na sua regio perifrica devido tenso superficial resultante nesta regio, como resultado o solvente percorre toda a superfcie do papel.
No decorrer do movimento da fase mvel as molculas de aminocidos presentes nas amostras so impulsionadas na direo de movimento da fase mvel, porm sua interao com a fase estacionria retarda esse movimento em maior ou menor grau de acordo com a fora de interao entre o aminocido em questo e a fase estacionria. Dessa forma, aminocidos com estruturas qumicas diferentes (diferentes propriedades fsico-qumicas) so separados nesta tcnica. Cabe lembrar que na separao de aminocidos deve-se utilizar uma fase mvel adequada, na qual eles so pouco solveis, caso contrrio a separao no ocorreria, pois todas as amostras percorreriam a mesma distncia juntamente com a fase mvel. Segue abaixo a tabela com os resultados obtidos. AMINOCIDO Rf esperado Rf medido Erro relativo percentual Glu 0,30 0,28 6% Ala 0,38 0,40 6% Arg 0,20 0,22 6% Leu 0,80 0,77 4% Pro 0,43 0,40 7% Tyr 0,45 0,45 0
http://www2.iq.usp.br/docente/henning/Disciplinas/Bioquimica%20QBQ230N/Apo stila_2010.pdf Podemos notar que os resultados obtidos no experimento esto de acordo com os dados presentes na literatura e apresentam erros relativos percentuais entre 4 e 7%. A diferena entre os valores encontrados com os dados da literatura podem ser devido a diversos fatores como, por exemplo, a espessura no uniforme do papel, umidade do ar (maior umidade do ar implica em um maior nmero de molculas de gua fase mvel- na superfcie do papel) e pH das solues de amostras. Analisando os valores de deslocamento das amostras de aminocidos podemos notar que a arginina possui o menor valor de Rf. Sua estrutura molecular polar e positivamente carregada favorece a interao com as molculas de gua que constituem a fase estacionria permitindo uma maior reteno e conseqentemente um deslocamento menor. Em contrapartida a leucina, com uma estrutura molecular apolar e hidrofbica possui menor interao com a fase estacionria e mais facilmente carregada pela fase mvel, o que contribui para seu maior deslocamento.
RESPOSTAS DAS QUESTES 1. Desenho ok
2. Reao com ninidrina : http://www.sciencedirect.com/science/article/pii/S0003267009008198 R. Jellya, E.L.T. Pattona, C. Lennardb, S. W. Lewisa, K. F. Lim. The detection of latent fingermarks on porous surfaces using amino acid sensitive reagents: A review. Analytica Chimica Acta.V 652, 2009, p 128142.
3. J respondido na discusso 4. J respondido na discusso
https://www3.nd.edu/~aseriann/titrate.html http://www.ebah.com.br/content/ABAAABlKAAF/curva-titulacao-aminoacidos
You might also like
- Interpretação Análise de SolosDocument10 pagesInterpretação Análise de SolosAllison Macambira100% (1)
- Capítulo 6Document7 pagesCapítulo 6Vânia FerreiraNo ratings yet
- Avaliação de Laboratório em Bioquímica - Thiago Amorim - 414641Document6 pagesAvaliação de Laboratório em Bioquímica - Thiago Amorim - 414641Thiago AmorimNo ratings yet
- Interpretação de análise de soloDocument11 pagesInterpretação de análise de soloLeonardo Ribas AmaralNo ratings yet
- Ácido fosfórico Coca-ColaDocument9 pagesÁcido fosfórico Coca-ColaKiany SirleyNo ratings yet
- Relatório Bioquímica - Neutralização Da GlicinaDocument5 pagesRelatório Bioquímica - Neutralização Da GlicinaDébora Raíssa Marçal100% (1)
- Relatório Solução TampãoDocument7 pagesRelatório Solução TampãoLuana Silva FerreiraNo ratings yet
- Titulação de aminoácidos: estudo do efeito-tampãoDocument46 pagesTitulação de aminoácidos: estudo do efeito-tampãoDoug MartinsNo ratings yet
- Titulac - A - o Potenciometrica Da GlicinaDocument15 pagesTitulac - A - o Potenciometrica Da GlicinaCarla Nogueira0% (1)
- Introdução BioquímicaDocument17 pagesIntrodução BioquímicaNu Film CriticsNo ratings yet
- Relatorio Da Aula Pratica de PH e Sistema TampaoDocument5 pagesRelatorio Da Aula Pratica de PH e Sistema TampaoEidem Costa0% (1)
- Análise das propriedades ácido-base dos aminoácidos por meio de titulaçãoDocument7 pagesAnálise das propriedades ácido-base dos aminoácidos por meio de titulaçãoarthur hilarioNo ratings yet
- Alcalinidade e AcidezDocument28 pagesAlcalinidade e AcidezJoseAlfredoCarneiroDosSantosNo ratings yet
- Relatorio PHDocument11 pagesRelatorio PHGiovana AdrieleNo ratings yet
- Experimento 11 - Giovana Jabur Teixeira e Cleidiane Aparecida AraújoDocument6 pagesExperimento 11 - Giovana Jabur Teixeira e Cleidiane Aparecida AraújoGiovana JaburNo ratings yet
- RELATÓRIO CAA - Thaynara CoutinhoDocument42 pagesRELATÓRIO CAA - Thaynara CoutinhoThaynara CoutinhoNo ratings yet
- Equilíbrio de Ácidos e Bases FracosDocument18 pagesEquilíbrio de Ácidos e Bases FracosRuanReisNo ratings yet
- RESUMO ARTIGO - A Highly Fluorescent PH Sensing Membrane For The Alkaline PH Range Incorporating A BODIPY Dye (2013)Document3 pagesRESUMO ARTIGO - A Highly Fluorescent PH Sensing Membrane For The Alkaline PH Range Incorporating A BODIPY Dye (2013)rebecaliriooNo ratings yet
- Relatório de Solução-Tampão Citrato e Ác. CítricoDocument17 pagesRelatório de Solução-Tampão Citrato e Ác. CítricoFelipe Pimentel Paixão100% (1)
- Relatorio Apl 2.1 - AcidooubaseDocument6 pagesRelatorio Apl 2.1 - Acidooubaserebordosa4No ratings yet
- Cinética enzimática em placa de 96 poçosDocument15 pagesCinética enzimática em placa de 96 poçosLucas MoreiraNo ratings yet
- Química - Titulação Ácido-BaseDocument14 pagesQuímica - Titulação Ácido-BaseSato DanNo ratings yet
- Análises Químicas EquilíbrioDocument5 pagesAnálises Químicas EquilíbriomisaelinacioNo ratings yet
- Determinação da constante de dissociação do indicador vermelho de metila por espectrofotometriaDocument7 pagesDeterminação da constante de dissociação do indicador vermelho de metila por espectrofotometriaangiegelainNo ratings yet
- A capacidade tamponante da água de coco, leite e solução tampão de fosfatoDocument12 pagesA capacidade tamponante da água de coco, leite e solução tampão de fosfatoCarol AgostiniNo ratings yet
- Prática 1 - Solução Tampão e PH - Final PDFDocument12 pagesPrática 1 - Solução Tampão e PH - Final PDFAline Cristal100% (1)
- Titulação de Ácido-BaseDocument3 pagesTitulação de Ácido-BaseMatilde HenriqueNo ratings yet
- Relatório 1Document10 pagesRelatório 1Natália CarvalhoNo ratings yet
- Relatório de Quimica 12º Ano - Soluções TampãoDocument10 pagesRelatório de Quimica 12º Ano - Soluções TampãoPaulo GasparNo ratings yet
- Fascículo 6 - Alcalinidade e AcidezDocument28 pagesFascículo 6 - Alcalinidade e AcidezgagolinowilNo ratings yet
- pH, acidez e alcalinidade: características químicas das águasDocument24 pagespH, acidez e alcalinidade: características químicas das águasMariana CarvalhoNo ratings yet
- Análise de Benzoato de SódioDocument10 pagesAnálise de Benzoato de SódioNadia100% (1)
- Relatorio Analitica.Document15 pagesRelatorio Analitica.Marcella Purificacao Di GirolamoNo ratings yet
- Relatório 1 - PH e Tampões - Parte 1Document2 pagesRelatório 1 - PH e Tampões - Parte 1Junior CastagnolliNo ratings yet
- Bioquímica DisciplinaDocument83 pagesBioquímica DisciplinaRaul CleversonNo ratings yet
- Titulação de aminoácido tripróticoDocument3 pagesTitulação de aminoácido tripróticoJunior CastagnolliNo ratings yet
- Análise de estudo dirigido de engenharia bioquímicaDocument9 pagesAnálise de estudo dirigido de engenharia bioquímicaAna Carolina AráujoNo ratings yet
- Cromatografia de Aminoácidos em PapelDocument7 pagesCromatografia de Aminoácidos em PapelGesiane G. Ferreira100% (1)
- Exp. 1 - Determinação Da Constante de Dissociação de IndicadoresDocument10 pagesExp. 1 - Determinação Da Constante de Dissociação de Indicadoresdaniel_fonseca_91No ratings yet
- Determinação da constante de dissociação do vermelho de metila por espectrofotometriaDocument18 pagesDeterminação da constante de dissociação do vermelho de metila por espectrofotometriaLuísa De Melo ArrudaNo ratings yet
- O Principio de Le Chatelier e o Efeito do Íon ComumDocument14 pagesO Principio de Le Chatelier e o Efeito do Íon ComumRicardo LimaNo ratings yet
- Experimento II de VolumetriaDocument3 pagesExperimento II de VolumetriaSuellen Costa0% (1)
- Erro na medição do pH do caldo de cana devido à temperaturaDocument15 pagesErro na medição do pH do caldo de cana devido à temperaturaMárcio Cardoso Proj IndNo ratings yet
- Relatorio 9 AaaaDocument6 pagesRelatorio 9 AaaaCarolyna de MendonçaNo ratings yet
- Determinação Da Capacidade Tamponante de Soluções TampõesDocument3 pagesDeterminação Da Capacidade Tamponante de Soluções TampõesGeovane SouzaNo ratings yet
- Relatorio Aula PraticaDocument6 pagesRelatorio Aula PraticaBielNo ratings yet
- Relatório - Determinação de Ácido Acético em VinagreDocument11 pagesRelatório - Determinação de Ácido Acético em VinagreEdjaine Carriel RosaNo ratings yet
- RELATORIO 4 - Dosagem Do Ácido Acetilsalicílico (AAS) em Medicamentos Por Potenciometria IndiretaDocument12 pagesRELATORIO 4 - Dosagem Do Ácido Acetilsalicílico (AAS) em Medicamentos Por Potenciometria IndiretaRaphael Brigagão100% (1)
- pH e Sistemas TampõesDocument3 pagespH e Sistemas TampõesAline Camurça100% (2)
- Determinação Coeficiente PartiçãoDocument9 pagesDeterminação Coeficiente PartiçãoGuilherme Henrique Dos SantosNo ratings yet
- PRÁTICA V– DETERMINAÇÃO DO PH DE SOLUÇÕES SALINASDocument9 pagesPRÁTICA V– DETERMINAÇÃO DO PH DE SOLUÇÕES SALINASjuliofreitassbNo ratings yet
- Determinação da concentração de ácido fosfórico em Coca-ColaDocument12 pagesDeterminação da concentração de ácido fosfórico em Coca-ColaHellen MacêdoNo ratings yet
- Relatório Actividade ExperimentalDocument10 pagesRelatório Actividade Experimentalvalsassina100% (3)
- Biofísica para ciências biomédicas – 4ª ediçãoFrom EverandBiofísica para ciências biomédicas – 4ª ediçãoNo ratings yet
- Projetos Em Clp Ladder Baseado Na Placa Arduino Uno Parte XiiFrom EverandProjetos Em Clp Ladder Baseado Na Placa Arduino Uno Parte XiiNo ratings yet
- Lista de Exercícios de Química Geral com Reações de VelocidadeDocument2 pagesLista de Exercícios de Química Geral com Reações de VelocidadePedro MarizNo ratings yet
- ElipseDocument4 pagesElipsePedro MarizNo ratings yet
- TesteDocument1 pageTestePedro MarizNo ratings yet
- Relatório - Reação Fotoquímica Da Benzofenona e Rearranjo Pinacol-PinacolonaDocument6 pagesRelatório - Reação Fotoquímica Da Benzofenona e Rearranjo Pinacol-PinacolonaPedro MarizNo ratings yet
- Experimento 7 - Halogênios - Grupo FullMetal - ScribdDocument6 pagesExperimento 7 - Halogênios - Grupo FullMetal - ScribdPedro MarizNo ratings yet
- Relatório - Reação Fotoquímica Da Benzofenona e Rearranjo Pinacol-PinacolonaDocument6 pagesRelatório - Reação Fotoquímica Da Benzofenona e Rearranjo Pinacol-PinacolonaPedro MarizNo ratings yet
- Um Tipo de TextoDocument1 pageUm Tipo de TextoPedro MarizNo ratings yet
- FÍSICA E QUÍMICA: Teste de avaliação do 11o ano com questões sobre reações químicas, equilíbrio químico e propriedades ácido-baseDocument5 pagesFÍSICA E QUÍMICA: Teste de avaliação do 11o ano com questões sobre reações químicas, equilíbrio químico e propriedades ácido-basesofiaNo ratings yet
- Equilíbrios químicos Kc e KpDocument21 pagesEquilíbrios químicos Kc e KpRobson RaduanNo ratings yet
- Lista de exercícios equilíbrio químicoDocument6 pagesLista de exercícios equilíbrio químicoJoice BeatrizNo ratings yet
- Determinação do teor de ácido acético em vinagre por titulação com NaOHDocument5 pagesDeterminação do teor de ácido acético em vinagre por titulação com NaOHVinícius OliveiraNo ratings yet
- Cores Da FenolftaleinaDocument11 pagesCores Da FenolftaleinaRaul AlmeidaNo ratings yet
- Lista Exerc. 2 - Pptação - GravimetriaDocument3 pagesLista Exerc. 2 - Pptação - GravimetriaMark WilsonNo ratings yet
- Aula 3 PH e pOHDocument6 pagesAula 3 PH e pOHBeatrizNo ratings yet
- Relatório Volumetria de ComplexaçãoDocument18 pagesRelatório Volumetria de ComplexaçãovvanessagomesmatosNo ratings yet
- Doseamento Do Ácido Acetilsalicílico Numa Aspirina Por Potenciometria e CondutimetriaDocument39 pagesDoseamento Do Ácido Acetilsalicílico Numa Aspirina Por Potenciometria e Condutimetriadpaulo79100% (2)
- Reações Aquosas e EstequiometriaDocument17 pagesReações Aquosas e EstequiometriaFernanda AmorimNo ratings yet
- Química Analítica - Questionário 4Document3 pagesQuímica Analítica - Questionário 4Alessandro AnacletoNo ratings yet
- AULA - Preparo de SoluçõesDocument52 pagesAULA - Preparo de SoluçõesPolly FernandesNo ratings yet
- Quimica Quantitat.Document26 pagesQuimica Quantitat.toraqk5297No ratings yet
- Aula Pratica 2Document8 pagesAula Pratica 2ZoordiNo ratings yet
- Funções Inorgânicas 2023 - ÁcidosDocument19 pagesFunções Inorgânicas 2023 - Ácidosgiovannamelo2107No ratings yet
- Determinação AA Utilizando Titulação CoulométricaDocument17 pagesDeterminação AA Utilizando Titulação CoulométricaLucas MoraNo ratings yet
- Balsamo Do Peru 03out2012Document1 pageBalsamo Do Peru 03out2012Margarete da Conceição SantosNo ratings yet
- Introdução - Experimento 2Document4 pagesIntrodução - Experimento 2gabrielli yamakawaNo ratings yet
- Ficha de Preparação 6ºtesteDocument7 pagesFicha de Preparação 6ºtesteRafael AfonsoNo ratings yet
- Cur Ti PotDocument185 pagesCur Ti PotAngelkbueno KB KBNo ratings yet
- Relatório Aula IV - Obtenção e Caracterização Da AmôniaDocument11 pagesRelatório Aula IV - Obtenção e Caracterização Da AmôniaNick AllenNo ratings yet
- 03 Padronização de Uma Solução de Hidroxido de Sodio e Determinação de Teor de Acidez em VinagreDocument12 pages03 Padronização de Uma Solução de Hidroxido de Sodio e Determinação de Teor de Acidez em VinagreAntônio Sérgio SouzaNo ratings yet
- Técnicas de pesagem em laboratórioDocument2 pagesTécnicas de pesagem em laboratórioFelipe LucasNo ratings yet
- Volumetria de neutralização: lista de exercíciosDocument5 pagesVolumetria de neutralização: lista de exercíciosAndré Mauricio De OliveiraNo ratings yet
- Cromatografia - Óleo Essencial de Alecrim ViaAromaDocument1 pageCromatografia - Óleo Essencial de Alecrim ViaAromaBruno MatsushitaNo ratings yet
- Resumo Sobre Ácidos e BasesDocument7 pagesResumo Sobre Ácidos e BasesRobson Timoteo Damasceno100% (2)
- 19 - Equilíbrio IônicoDocument3 pages19 - Equilíbrio IônicoツBorutoNo ratings yet
- Lista de exercícios sobre reações em solução aquosa IIDocument2 pagesLista de exercícios sobre reações em solução aquosa IIEvelyn Santos ResqueNo ratings yet
- Diluição e MisturaDocument15 pagesDiluição e MisturaozikaaapedrinhoNo ratings yet
- Ficha Avaliação Moduloq4Document4 pagesFicha Avaliação Moduloq4daires73No ratings yet