Professional Documents
Culture Documents
Amino Ácid o
Uploaded by
Bruno Vega Chicoma0 ratings0% found this document useful (0 votes)
23 views12 pagesCopyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
23 views12 pagesAmino Ácid o
Uploaded by
Bruno Vega ChicomaCopyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 12
Aminocido
Un aminocido es una molcula orgnica con un grupo amino (-NH
2
) y un grupo carboxilo (-COOH). Los
aminocidos ms frecuentes y de mayor inters son aquellos que forman parte de lasprotenas. Dos
aminocidos se combinan en una reaccin de condensacin entre el grupo amino de uno y el carboxilo del
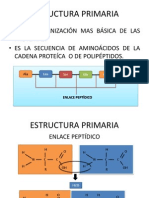
otro, liberndose una molcula de agua y formando un enlace amida que se denomina enlace peptdico;
estos dos "residuos" de aminocido forman un dipptido. Si se une un tercer aminocido se forma
un tripptido y as, sucesivamente, hasta formar unpolipptido. Esta reaccin tiene lugar de manera
natural dentro de las clulas, en los ribosomas.
Todos los aminocidos componentes de las protenas son L-alfa-aminocidos. Esto significa que el
grupo amino est unido al carbono contiguo al grupo carboxilo (carbono alfa) o, dicho de otro modo, que
tanto el carboxilo como el amino estn unidos al mismo carbono; adems, a este carbono alfa se unen
un hidrgeno y una cadena (habitualmente denominada cadena lateral o radical R) de estructura variable,
que determina la identidad y las propiedades de cada uno de los diferentes aminocidos. Existen cientos
de radicales por lo que se conocen cientos de aminocidos diferentes, pero slo 22 (los dos ltimos fueron
descubiertos en el ao 2002) forman parte de las protenas y tienen codones especficos en el cdigo
gentico.
La unin de varios aminocidos da lugar a cadenas llamadas pptidos o polipptidos, que se denominan
protenas cuando la cadena polipeptdica supera una cierta longitud (entre 50 y 100 residuos aminocidos,
dependiendo de los autores) o la masa molecular total supera las 5000 uma y, especialmente, cuando
tienen una estructura tridimensional estable definida.
Estructura general de un aminocido[editar]
La estructura general de un alfa-aminocido se establece por la presencia de un carbono central (alfa)
unido a un grupo carboxilo (rojo en la figura), un grupo amino (verde), un hidrgeno (en negro) y la cadena
lateral (azul):
"R" representa la cadena lateral, especfica para cada aminocido. Tanto el carboxilo como el amino
son grupos funcionales susceptibles de ionizacin dependiendo de los cambios de pH, por eso ningn
aminocido en disolucin se encuentra realmente en la forma representada en la figura, sino que se
encuentra ionizado.
A pH bajo (cido), los aminocidos se encuentran mayoritariamente en su forma catinica (con carga
positiva), mientras que a pH alto (bsico) se encuentran en su forma aninica (con carga negativa). Para
valores de pH intermedios, como los propios de los medios biolgicos, los aminocidos se encuentran
habitualmente en una forma de ion dipolar o zwitterin (con un grupo catinico y otro aninico).
Clasificacin[editar]
Existen muchas formas de clasificar los aminocidos; las dos que se presentan a continuacin son las ms
comunes.
Segn las propiedades de su cadena[editar]
Otra forma de clasificar los aminocidos de acuerdo a su cadena lateral.
Los aminocidos se clasifican habitualmente segn las propiedades de su cadena lateral:
Neutros polares, polares o hidrfilos : serina (Ser, S), treonina (Thr, T), cistena (Cys, C), glutamina (Gln,
Q), asparagina (Asn, N) , tirosina (Tyr, Y) y glicina (Gly, G).
Neutros no polares, apolares o hidrfobos: alanina (Ala, A), valina (Val, V), leucina (Leu, L), isoleucina
(Ile, I), metionina (Met, M), prolina (Pro, P), fenilalanina (Phe, F) y triptfano (Trp, W).
Con carga negativa o cidos: cido asprtico (Asp, D) y cido glutmico (Glu, E).
Con carga positiva o bsicos: lisina (Lys, K), arginina (Arg, R) e histidina (His, H). fenilalanina (Phe, F),
tirosina (Tyr, Y) y triptfano (Trp, W) (ya incluidos en los grupos neutros polares y neutros no polares).
Segn su obtencin[editar]
A los aminocidos que deben ser captados como parte de los alimentos se los llama esenciales; la carencia
de estos aminocidos en la dieta limita el desarrollo del organismo, ya que no es posible reponer las clulas
de los tejidos que mueren o crear tejidos nuevos, en el caso del crecimiento. Para el ser humano, los
aminocidos esenciales son:
Valina (Val, V)
Leucina (Leu, L)
Treonina (Thr, T)
Lisina (Lys, K)
Triptfano (Trp, W)
Histidina (His, H) *
Fenilalanina (Phe, F)
Isoleucina (Ile, I)
Arginina (Arg, R) *
Metionina (Met, M)
A los aminocidos que pueden sintetizarse en el propio organismo se los conoce como no esenciales y son:
Alanina (Ala, A)
Prolina (Pro, P)
Glicina (Gly, G)
Serina (Ser, S)
Cistena (Cys, C) **
Asparagina (Asn, N)
Glutamina (Gln, Q)
Tirosina (Tyr, Y) **
cido asprtico (Asp, D)
cido glutmico (Glu, E)
Estas clasificaciones varan segn la especie e incluso, para algunos aminocidos, segn los autores. Se han
aislado cepas de bacterias con requerimientos diferenciales de cada tipo de aminocido.
Segn la ubicacin del grupo amino[editar]
Alfa-aminocidos: El grupo amino est ubicado en el carbono n. 2 de la cadena, es decir el primer
carbono a continuacin del grupo carboxilo (histricamente este carbono se denomina carbono alfa).
La mayora de las protenas estn compuestas por residuos de alfa-aminocidos enlazados mediante
enlaces amida (enlaces peptdicos).
Beta-aminocidos: El grupo amino est ubicado en el carbono n. 3 de la cadena, es decir en el
segundo carbono a continuacin del grupo carboxilo.
Gamma-aminocidos: El grupo amino est ubicado en el carbono n. 4 de la cadena, es decir en el
tercer carbono a continuacin del grupo carboxilo.
Aminocidos codificados en el genoma[editar]
Los aminocidos proteicos, cannicos o naturales son aquellos que estn codificados en el genoma; para la
mayora de los seres vivos son 20: alanina, arginina, asparagina, aspartato, cistena, fenilalanina, glicina,
glutamato, glutamina, histidina, isoleucina, leucina, lisina, metionina, prolina, serina, tirosina, treonina,
triptfano y valina.
Sin embargo, hay excepciones: en algunos seres vivos el cdigo gentico tiene pequeas modificaciones y
puede codificar otros aminocidos. El aminocido nmero 21 es la selenocistena, que aparece tanto en
eucariotas como procariotas y arqueas, y el nmero 22 es la pirrolisina que aparece slo en arqueas.
1
2
3
Aminocidos modificados[editar]
Las modificaciones postraduccionales de los 20 aminocidos codificados genticamente conducen a la
formacin de 100 o ms derivados de los aminocidos. Las modificaciones de los aminocidos juegan con
frecuencia un papel de gran importancia en la correcta funcionalidad de una protena.
Son numerosos los ejemplos de modificacin postraduccional de aminocidos. La formacin de puentes
disulfuro, claves en la estabilizacin de la estructura terciaria de las protenas, est catalizada por
una disulfuro isomerasa. En las histonas tiene lugar la metilacin de las lisinas. En el colgeno abunda el
aminocido 4-hidroxiprolina, que es el resultado de la hidroxilacin de la prolina. La metionina inicial de
todos los polipptidos (codificada por el codn de inicio AUG) casi siempre se elimina por protelisis.
4
Algunos aminocidos no proteicos tienen funcin propia, por ejemplo
como neurotransmisores o vitaminas. Por ejemplo, la beta-alanina o el cido gamma-aminobutrico
(GABA). Existen muchos aminocidos no proteicos que juegan papeles distintos en la naturaleza y pueden
o no provenir de aminocidos. Ejemplos de estos aminocidos no protenicos son:
Sarcosina
Etilglicina o cido -aminobutrico (AABA)
cido djenclico
Hipoglicinas A y B
Mimosina
Aliina
Canalina
Canavanina
Ornitina
Homometionina
Homoserina
Homoarginina
Homofenilalanina
Homocistena
Homoleucina
Cistationina
Norvalina
Norleucina
Ciclopentenilglicina
-Alanina
cido gamma-aminobutrico
cido ibotnico
cido pipeclico
cido guanidinactico
Taurina
cido trans-2-amino-5-cloro-4-hexenoico
cido trans-2-amino-5-cloro-6-hidroxi-4-hexenoico
cido 2-amino-4-cloro-4-pentenoico
cido diaminopimlico
Semialdehdo asprtico
Semialdehdo glutmico
Citrulina
DOPA
Quinurenina
Nicotianina
cido 2-azetidincarboxlico
-(4-hidroxibenzotiazol-6-il)alanina
-(2-metil-4-hidroxibenzotiazol-6-il)-alanina
Indospicina
N-(indol-3-acetil)lisina
(p-hidroximetil)fenilalanina
0-etil-L-homoserina, aislada de Corynebacterium ethanolaminophilum
5-Hidroxitriptfano
cido licoprdico, aislado de Lycoperdon perlatum
cido lentnico
cido estizolobnico
cido estizolbico
Tiroxina
Azoxibacilina
Propiedades[editar]
cido-bsicas.
Se refiere al comportamiento de cualquier aminocido cuando se ioniza. Cualquier aminocido
puede comportarse como cido y como base, por lo que se denominan sustancias anfteras.
Cuando una molcula presenta carga neta cero est en su punto isoelctrico. Si un aminocido
tiene un punto isoelctrico de 6,1 su carga neta ser cero cuando el pH sea 6,1.
Los aminocidos y las protenas se comportan como sustancias tampn.
pticas.
Todos los aminocidos excepto la glicina tienen 4 sustituyentes distintos sobre su carbono alfa
(carbono asimtrico o quiral), lo que les confiere actividad ptica; esto es, sus disoluciones desvan
el plano de polarizacin cuando un rayo de luz polarizada las atraviesa. Si el desvo del plano de
polarizacin es hacia la derecha (en sentido horario), el compuesto se denominadextrgiro,
mientras que si se desva a la izquierda (sentido antihorario) se denomina levgiro. Un aminocido
puede en principio existir en sus dos formas enantiomricas (una dextrgira y otra levgira), pero
en la naturaleza lo habitual es encontrar slo una de ellas.
Estructuralmente, las dos posibles formas enantiomricas de cada aminocido se denominan
configuracin D o L dependiendo de la orientacin relativa en el espacio de los 4 grupos distintos
unidos al carbono alfa. Todos los aminocidos proteicos son L-aminocidos, pero ello no significa
que sean levgiros.
Se consideran L-aminocidos los que estructuralmente derivan de L-gliceraldehdo y D-aminocidos
los derivados del D-gliceraldehdo.
Qumicas.
Las que afectan al grupo carboxilo, como la descarboxilacin.
Las que afectan al grupo amino, como la desaminacin.
Las que afectan al grupo R o cadena lateral.
Solubilidad.
No todos los aminocidos son solubles en agua debido a la diferente naturaleza de su cadena
lateral, por ejemplo si sta es ionizable el aminocido ser ms soluble.
Reacciones de los aminocidos[editar]
Los aminocidos sufren en los seres vivos tres reacciones
principales que se inician cuando un aminocido se une con
el fosfato de piridoxal formando una base de Schiff o aldimina.
De ah en adelante la transformacin depende de las enzimas,
que tienen en comn el uso del fosfato de piridoxal
como coenzima. Las reacciones que se desencadenan pueden
ser:
1. La transaminacin, que necesita la participacin de
un -cetocido;
2. La descarboxilacin;
3. La racemizacin, que es la conversin de un compuesto
L en D, o viceversa. Aunque en las protenas los
aminocidos estn presentes nicamente en la
configuracin L, en las bacterias podemos encontrar
algunos D-aminocidos formando parte de pptidos
pequeos
Aminocidos esenciales
Los aminocidos esenciales son aquellos que el propio organismo no puede sintetizar por s mismo. Esto
implica que la nica fuente de estos aminocidos en esos organismos es la ingesta directa a travs de
la dieta. Las rutas para la obtencin de los aminocidos esenciales suelen ser largas y energticamente
costosas.
Cuando un alimento contiene protenas con todos los aminocidos esenciales, se dice que son de alta o de
buena calidad, aunque en realidad la calidad de cada uno de los aminocidos contenidos no cambia.
Incluso se pueden combinar (sin tener que hacerlo al mismo tiempo) las protenas de legumbres con
protenas de cereales para conseguir todos los aminocidos esenciales en nuestra nutricin diaria, sin que
la calidad real de esta nutricin disminuya. Algunos de los alimentos con todos los aminocidos esenciales
son: la carne, los huevos, los lcteos y algunos vegetales como la espelta, la soja y la quinoa.
Combinaciones de alimentos que suman los aminocidos esenciales
son: garbanzos y avena, trigo y habichuelas, maz y lentejas, arroz yman (cacahuetes), etc. En definitiva,
legumbres y cereales ingeridos diariamente, pero sin necesidad de que sea en la misma comida.
No todos los aminocidos son esenciales para todos los organismos (de hecho slo nueve lo son), por
ejemplo, la alanina (no esencial) en humanos se puede sintetizar a partir del piruvato.
La arginina puede ser esencial en los nios muy pequeos ya que sus requerimientos son mayores que su
capacidad para sintetizar este aminocido.
Conjunto Bsico de 20 aminocidos
Esenciales No esenciales
Isoleucina Alanina
Leucina Tirosina
Lisina Aspartato
Metionina Cistena
Fenilalanina Glutamato
Treonina Glutamina
Triptfano Glicina
Valina Prolina
Histidina Serina
Arginina (condicionalmente) Asparagina
Los aminocidos que contienen azufre, metionina y cistena, se pueden convertir uno en el otro, por lo que
por conveniencia se consideran una nica fuente. Del mismo modo, la arginina, ornitinay citrulina son
interconvertibles, y tambin se consideran una nica fuente de aminocidos nutricionalmente
equivalentes.
En otros mamferos distintos a los humanos, los aminocidos esenciales pueden ser considerablemente
distintos. Por ejemplo, a los gatos les falta la enzima que les permitira sintetizar lataurina, que es un cido
derivado de la cistena, as que la taurina es esencial para los gatos.
Un detalle interesante es que casi ningn animal puede sintetizar lisina.
Deficiencia de aminocidos esenciales[editar]
Los aminocidos que son esenciales en la dieta humana fueron establecidos en una serie de experimentos
liderados por William Cumming Rose. Estos experimentos involucraron dietas elementales a estudiantes
graduados saludables. Estas dietas consistieron en almidn de maz, sacarosa, mantequilla sin protena,
aceite de maz, sales inorgnicas, las vitaminas conocidas, un caramelo hecho con extracto de hgado
saborizado con aceite de menta (para suplir una deficiencia de cualquier vitamina desconocida), y mezclas
de aminocidos individuales altamente purificados. El Dr. Rose not sntomas de nerviosismo, fatiga y
mareos en mayor o menor grado cuando los sujetos eran privados de un aminocido esencial.
La deficiencia de aminocidos esenciales debe ser distinguida de la malnutricin por deficiencia de
protenas, la cual puede manifestarse como marasmo o sndrome de kwashiorkor. El kwashiorkor fue
alguna vez atribuido a una deficiencia de protenas en individuos que consumen suficientes protenas. Sin
embargo esta teora ha sido desafiada por hallazgos que revelan que no existen diferencias en las dietas de
nios desarrollando marasmo en comparacin con los que desarrollan.
u son los aminocidos?
Son sustancias cristalinas, casi siempre de sabor dulce; tienen carcter cido como propiedad bsica y
actividad ptica; qumicamente son cidos carbnicos con, por lo menos, un grupo amino por
molcula, 20 aminocidos diferentes son los componentes esenciales de las protenas.-
Los aminocidos son las unidades elementales constitutivas de las molculas denominadas Protenas. Son
pues, y en un muy elemental smil, los "ladrillos" con los cuales el organismo reconstituye
permanentemente sus protenas especficas consumidas por la sola accin de vivir.
Protenas que son los compuestos nitrogenados ms abundantes del organismo, a la vez que fundamento
mismo de la vida. En efecto, debido a la gran variedad de protenas existentes y como consecuencia de su
estructura, las protenas cumplen funciones sumamente diversas, participando en todos los procesos
biolgicos y constituyendo estructuras fundamentales en los seres vivos. De este modo, actan acelerando
reacciones qumicas que de otro modo no podran producirse en los tiempos necesarios para la vida
(enzimas), transportando sustancias (como la hemoglobina de la sangre, que transporta oxgeno a los
tejidos), cumpliendo funciones estructurales (como la queratina del pelo), sirviendo como reserva
(albmina de huevo), etc.
Los alimentos que ingerimos nos proveen protenas. Pero tales protenas no se absorben normalmente en
tal constitucin sino que, luego de su desdoblamiento ("hidrlisis" o rotura), causado por el proceso de
digestin, atraviesan la pared intestinal en forma de aminocidos y cadenas cortas de pptidos, segn lo
que se denomina " circulacin entero heptica".
Esas sustancias se incorporan inicialmente al torrente sanguneo y, desde all, son distribudas hacia los
tejidos que las necesitan para formar las protenas, consumidas durante el ciclo vital.
Se sabe que de los 20 aminocidos proteicos conocidos, 8 resultan indispensables (o esenciales) para la
vida humana y 2 resultan "semi indispensables". Son estos 10 aminocidos los que requieren ser
incorporados al organismo en su cotidiana alimentacin y, con ms razn, en los momentos en que el
organismo ms los necesita: en la disfuncin o enfermedad. Los aminocidos esenciales ms problemticos
son el triptfano, la lisina y la metionina. Es tpica su carencia en poblaciones en las que los cereales o los
tubrculos constituyen la base de la alimentacin. Los dficit de aminocidos esenciales afectan mucho
ms a los nios que a los adultos.
Hay que destacar que, si falta uno solo de ellos (Aminocido esenciales) no ser posible sintetizar ninguna
de las protenas en la que sea requerido dicho aminocido. Esto puede dar lugar a diferentes tipos de
desnutricin, segn cual sea el aminocido limitante.
Lista de Aminocidos (Esenciales y no esenciales) y funcin de cada una de ellos:
Alanina. Funcin: Interviene en el metabolismo de la glucosa. La glucosa es un carbohidrato simple que
el organismo utiliza como fuente de energa.
Arginina. Funcin: Est implicada en la conservacin del equilibrio de nitrgeno y de dixido de carbono.
Tambin tiene una gran importancia en la produccin de la Hormona del Crecimiento, directamente
involucrada en el crecimiento de los tejidos y msculos y en el mantenimiento y reparacin del sistema
inmunologico.
Asparagina. Funcin: Interviene especficamente en los procesos metablicos del Sistema Nervioso
Central (SNC).
Acido Asprtico. Funcin: Es muy importante para la desintoxicacin del Hgado y su correcto
funcionamiento. El cido L- Asprtico se combina con otros aminocidos formando molculas capases de
absorber toxinas del torrente sanguneo.
Citrulina. Funcin: Interviene especficamente en la eliminacin del amonaco.
Cistina. Funcin: Tambin interviene en la desintoxicacin, en combinacin con los aminocidos
anteriores. La L - Cistina es muy importante en la sntesis de la insulina y tambin en las reacciones de
ciertas molculas a la insulina.
Cisteina. Funcin: Junto con la L- cistina, la L- Cisteina est implicada en la desintoxicacin,
principalmente como antagonista de los radicales libres. Tambin contribuye a mantener la salud de los
cabellos por su elevado contenido de azufre.
Glutamin. Funcin: Nutriente cerebral e interviene especficamente en la utilizacin de la glucosa por el
cerebro.
Acido Glutminico. Funcin: Tiene gran importancia en el funcionamiento del Sistema Nervioso Central y
acta como estimulante del sistema inmunologico.
Glicina: Funcin: En combinacin con muchos otros aminocidos, es un componente de numerosos
tejidos del organismo.
Histidina. Funcin: En combinacin con la hormona de crecimiento (HGH) y algunos aminocidos
asociados, contribuyen al crecimiento y reparacin de los tejidos con un papel especficamente relacionado
con el sistema cardio-vascular.
Serina. Funcin: Junto con algunos aminocidos mencionados, interviene en la desintoxicacin del
organismo, crecimiento muscular, y metabolismo de grasas y cidos grasos.
Taurina. Funcin: Estimula la Hormona del Crecimiento (HGH) en asociacin con otros aminocidos, esta
implicada en la regulacin de la presin sanguinea, fortalece el msculo cardiaco y vigoriza el sistema
nervioso.
Tirosina. Funcin: Es un neurotransmisor directo y puede ser muy eficaz en el tratamiento de la
depresin, en combinacin con otros aminocidos necesarios.
Ornitina. Funcin: Es especfico para la hormona del Crecimiento (HGH) en asociacin con otros
aminocidos ya mencionados. Al combinarse con la L-Arginina y con carnitina (que se sintetiza en el
organismo, la L-Ornitina tiene una importante funcin en el metabolismo del exceso de grasa corporal.
Prolina. Funcin: Est involucrada tambin en la produccin de colgeno y tiene gran importancia en la
reparacin y mantenimiento del msculo y huesos.
Los 8 esenciales
Isoleucina. Funcin: Junto con la L-Leucina y la Hormona del Crecimiento intervienen en la formacin y
reparacin del tejido muscular.
Leucina. Funcin: Junto con la L-Isoleucina y la Hormona del Crecimiento (HGH) interviene con la
formacin y reparacin del tejido muscular.
Lisina. Funcin: Es uno de los ms importantes aminocidos porque, en asociacin con varios
aminocidos ms, interviene en diversas funciones, incluyendo el crecimiento, reparacin de tejidos,
anticuerpos del sistema inmunolgico y sntesis de hormonas.
Metionina. Funcin: Colabora en la sntesis de protenas y constituye el principal limitante en las
protenas de la dieta. El aminocido limitante determina el porcentaje de alimento que va a utilizarse a
nivel celular.
Fenilalanina. Funcin: Interviene en la produccin del Colgeno, fundamentalmente en la estructura de
la piel y el tejido conectivo, y tambin en la formacin de diversas neurohormonas.
Triptfano. Funcin: Est inplicado en el crecimiento y en la produccin hormonal, especialmente en la
funcin de las glndulas de secrecin adrenal. Tambin interviene en la sntesis de la serotonina,
neurohormona involucrada en la relajacin y el sueo.
Treonina. Funcin: Junto con la con la L-Metionina y el cido Asprtico ayuda al hgado en sus funciones
generales de desintoxicacin.
Valina. Funcin: Estimula el crecimiento y reparacin de los tejidos, el mantenimiento de diversos
sistemas y balance de nitrgeno.
Debemos recordar que, debido a la crtica relacin entre los diversos aminocidos y los aminocidos
limitantes presentes en cualquier alimento. Solo una proporcin relativamente pequea de aminocidos
de cada alimento pasa a formar parte de las protenas del organismo. El resto se usa como fuente de
energa o se convierte en grasa si no debe de usarse inmediatamente.
Productos naturales que contienen las cantidades medias de aminocidos que se usan en realidad a nivel
celular
Cantidades en gramos
Almendras (1 taza) 1.00 gr.
Semillas de girasol crudas (1 taza) 1.28 gr.
Arroz Integral (1 taza) 0.47 gr.
Cebada (1 taza) 0.90 gr.
Guisantes (1 taza) 0.27 gr.
Habichuelas rojas (1 taza) 0.85 gr.
Semillas de Ajonjol (1 taza) 0.89 gr.
Pan integral (1 rebanada) 0.14 gr.
Spaghetti Harina Integral (1 taza) 0.65 gr.
Todos los dems vegetales (1 taza) 0.27 gr.
Productos aminales que contienen las cantidades medias de aminoacidos que se usan en realidad a nivel
celular
Cantidades en gramos
Leche (1 taza) 0.29 gr.
Una clara de huevo 1.63 gr.
Huevo completo (aminocidos limitantes) 0.70 gr.
Pescado (1/4 libra) 0.21 gr.
Hgado (1/4 libra) 0.78 gr.
Queso blanco (1/4 taza) 0.26 gr.
Carne de res (1/2 libra) 1.49 gr.
Carne de cerdo (1/4 libra) 0.69 gr.
Pavo (1/4 libra) utilizacin muy limitada de aminocidos. gr.
Pollo (1/4 libra) 0.95 gr.
Cordero o Cabro (1/2 libra) 1.54 gr.
Para saber la cantidad media de aminocidos que necesitamos al da, se multiplica el peso corporal en kilos
(1000 gramos) 0.12 %.
La libra americana es de 450 gramos. Si el peso son 146 libras multiplica por 450 gramos y luego los divide
por 1000 da el peso en kilos.
Ejemplo: una persona que pesa 146 libras americanas, lo multiplicado por 450 gramos es igual a 65700 y lo
dividimos por 1000 es igual a 65.70 kilos.
146 x 450 = 65.700 gramos
65.700 - 1000 = 65.70 kilos.
Valor biolgico de las protenas
El conjunto de los aminocidos esenciales slo est presente en las protenas de origen animal. En la
mayora de los vegetales siempre hay alguno que no est presente en cantidades suficientes. Se define el
valor o calidad biolgica de una determinada protena por su capacidad de aportar todos los aminocidos
necesarios para los seres humanos. La calidad biolgica de una protena ser mayor cuanto ms similar sea
su composicin a la de las protenas de nuestro cuerpo. De hecho, la leche materna es el patrn con el que
se compara el valor biolgico de las dems protenas de la dieta.
Por otro lado, no todas las protenas que ingerimos se digieren y asimilan. La utilizacin neta de una
determinada protena, o aporte proteico neto, es la relacin entre el nitrgeno que contiene y el que el
organismo retiene. Hay protenas de origen vegetal, como la de la soja, que a pesar de tener menor valor
biolgico que otras protenas de origen animal, su aporte proteico neto es mayor por asimilarse mucho
mejor en nuestro sistema digestivo.
Necesidades diarias de protenas
La cantidad de protenas que se requieren cada da es un tema controvertido, puesto que depende de
muchos factores. Depende de la edad, ya que en el perodo de crecimiento las necesidades son el doble o
incluso el triple que para un adulto, y del estado de salud de nuestro intestino y nuestros riones, que
pueden hacer variar el grado de asimilacin o las prdidas de nitrgeno por las heces y la orina. Tambin
depende del valor biolgico de las protenas que se consuman, aunque en general, todas las
recomendaciones siempre se refieren a protenas de alto valor biolgico. Si no lo son, las necesidades
sern an mayores.
En general, se recomiendan unos 40 a 60 gr. de protenas al da para un adulto sano. La Organizacin
Mundial de la Salud y las RDA USA recomiendan un valor de 0,8 gr. por kilogramo de peso y da. Por
supuesto, durante el crecimiento, el embarazo o la lactancia estas necesidades aumentan, como reflejan la
tabla de necesidades mnimas de protenas.
A TENER EN CUENTA: Las raciones, expresadas como ingestas diarias a lo largo del tiempo, estn
destinadas a cubrir las variaciones individuales entre la mayora de las personas normales, que viven en
Estados Unidos en condiciones de estrs ambiental habitual. La composicin de aminocidos tenida en
cuenta para estos clculos es la tpica de la dieta media de los Estados Unidos, que puede ser igualmente
aplicable a la dieta de los espaoles.
El mximo de protenas que podemos ingerir sin afectar a nuestra salud, es un tema an ms delicado. Las
protenas consumidas en exceso, que el organismo no necesita para el crecimiento o para el recambio
proteico, se queman en las clulas para producir energa. A pesar de que tienen un rendimiento energtico
igual al de los hidratos de carbono, su combustin es ms compleja y dejan residuos metablicos, como el
amoniaco, que son txicos para el organismo. El cuerpo humano dispone de eficientes sistemas de
eliminacin, pero todo exceso de protenas supone cierto grado de intoxicacin que provoca la destruccin
de tejidos y, en ltima instancia, la enfermedad o el envejecimiento prematuro. Debemos evitar comer
ms protenas de las estrictamente necesarias para cubrir nuestras necesidades.
Por otro lado, investigaciones muy bien documentadas, llevadas a cabo en los ltimos aos por el doctor
alemn Lothar Wendt, han demostrado que los aminocidos se acumulan en las membranas basales de los
capilares sanguneos para ser utilizados rpidamente en caso de necesidad. Esto supone que cuando hay
un exceso de protenas en la dieta, los aminocidos resultantes siguen acumulndose, llegando a dificultar
el paso de nutrientes de la sangre a las clulas (microangiopata). Estas investigaciones parecen abrir un
amplio campo de posibilidades en el tratamiento a travs de la alimentacin de gran parte de las
enfermedades cardiovasculares, que tan frecuentes se han vuelto en occidente desde que se generaliz el
consumo indiscriminado de carne.
Protenas de origen vegetal o animal?
Puesto que slo asimilamos aminocidos y no protenas completas, el organismo no puede distinguir si
estos aminocidos provienen de protenas de origen animal o vegetal. Comparando ambos tipos de
protenas podemos sealar:
Las protenas de origen animal son molculas mucho ms grandes y complejas, por lo que contienen mayor
cantidad y diversidad de aminocidos. En general, su valor biolgico es mayor que las de origen vegetal.
Como contrapartida son ms difciles de digerir, puesto que hay mayor nmero de enlaces entre
aminocidos por romper. Combinando adecuadamente las protenas vegetales (legumbres con cereales o
lcteos con cereales) se puede obtener un conjunto de aminocidos equilibrado. Por ejemplo, las protenas
del arroz contienen todos los aminocidos esenciales, pero son escasas en lisina. Si las combinamos con
lentejas o garbanzos, abundantes en lisina, la calidad biolgica y aporte proteico resultante es mayor que
el de la mayora de los productos de origen animal.
Al tomar protenas animales a partir de carnes, aves o pescados ingerimos tambin todos los desechos del
metabolismo celular presentes en esos tejidos (amoniaco, cido rico, etc.), que el animal no pudo
eliminar antes de ser sacrificado. Estos compuestos actan como txicos en nuestro organismo. El el
metabolismo de los vegetales es distinto y no estn presentes estos derivados nitrogenados. Los txicos de
la carne se pueden evitar consumiendo las protenas de origen animal a partir de huevos, leche y sus
derivados. En cualquier caso, siempre sern preferibles los huevos y los lcteos a las carnes, pescados y
aves. En este sentido, tambin preferiremos los pescados a las aves, y las aves a las carnes rojas o de cerdo.
La protena animal suele ir acompaada de grasas de origen animal, en su mayor parte saturadas. Se ha
demostrado que un elevado aporte de cidos grasos saturados aumenta el riesgo de padecer
enfermedades cardiovasculares.
En general, se recomienda que una tercera parte de las protenas que comamos sean de origen animal,
pero es perfectamente posible estar bien nutrido slo con protenas vegetales. Eso s, teniendo la
precaucin de combinar estos alimentos en funcin de sus aminocidos limitantes. El problema de las
dietas vegetarianas en occidente suele estar ms bien en el dficit de algunas vitaminas, como la B12, o de
minerales, como el hierro.
You might also like
- Leccion 8Document26 pagesLeccion 8Bruno Vega ChicomaNo ratings yet
- Articulo Materias PrimasDocument7 pagesArticulo Materias PrimasBruno Vega ChicomaNo ratings yet
- Materiales para La DegustaciónDocument5 pagesMateriales para La DegustaciónBruno Vega ChicomaNo ratings yet
- Proyecto de Mermelada de NaranjaDocument20 pagesProyecto de Mermelada de NaranjaBruno Vega Chicoma60% (10)
- La Regla de Tres SimpleDocument8 pagesLa Regla de Tres SimpleHanai KishimotoNo ratings yet
- Pescados de Rio - NutricionDocument9 pagesPescados de Rio - NutricionBruno Vega ChicomaNo ratings yet
- Informe de HidrobiológicosDocument13 pagesInforme de HidrobiológicosBruno Vega ChicomaNo ratings yet
- 19 Regla de Tres Compuesta para Estudiantes de Segundo de SecundariaDocument7 pages19 Regla de Tres Compuesta para Estudiantes de Segundo de SecundariaBruno Vega ChicomaNo ratings yet
- NTP Arroz PiladoDocument3 pagesNTP Arroz PiladofiorellabpNo ratings yet
- Certificado de HorasDocument1 pageCertificado de HorasBruno Vega ChicomaNo ratings yet
- 5refrig y Cong de Frutas y HortalizasDocument23 pages5refrig y Cong de Frutas y HortalizasBruno Vega ChicomaNo ratings yet
- Evaluación Sensorial Sentido Del TactoDocument6 pagesEvaluación Sensorial Sentido Del TactoBruno Vega ChicomaNo ratings yet
- La EmpresaDocument9 pagesLa EmpresaBruno Vega ChicomaNo ratings yet
- Marketing - AdministracionDocument8 pagesMarketing - AdministracionBruno Vega ChicomaNo ratings yet
- Cata de Cafe. Analisis SensorialDocument24 pagesCata de Cafe. Analisis SensorialDaniel Bran100% (8)
- Direcccion - Proceso AdministrativoDocument5 pagesDirecccion - Proceso AdministrativoBruno Vega ChicomaNo ratings yet
- Administracion TrabajoDocument12 pagesAdministracion TrabajoBruno Vega ChicomaNo ratings yet
- Evaluación Sensorial Del Cafe - TecnoDocument10 pagesEvaluación Sensorial Del Cafe - TecnoBruno Vega ChicomaNo ratings yet
- ANOVA de Un Factor GraficosDocument4 pagesANOVA de Un Factor GraficosBruno Vega ChicomaNo ratings yet
- Pescados de Rio - NutricionDocument9 pagesPescados de Rio - NutricionBruno Vega ChicomaNo ratings yet
- Ejercicios de Mate IIIDocument27 pagesEjercicios de Mate IIIBruno Vega ChicomaNo ratings yet
- La EmpresaDocument9 pagesLa EmpresaBruno Vega ChicomaNo ratings yet
- Tecnología de Los AlimentosDocument2 pagesTecnología de Los AlimentosBruno Vega ChicomaNo ratings yet
- IPQ Balance de Materia Procesos Reactivos (1) 132-141Document10 pagesIPQ Balance de Materia Procesos Reactivos (1) 132-141kevin15vhNo ratings yet
- Solucionario de Dennis G Zill - Ecuaciones DiferencialesDocument86 pagesSolucionario de Dennis G Zill - Ecuaciones Diferencialesdesigniusk84% (88)
- Solucionario 2º Bachillerato. Física. Unidad 10.Document20 pagesSolucionario 2º Bachillerato. Física. Unidad 10.Fer HouseNo ratings yet
- Capítulo 9 Teoría Microbiología GeneralDocument19 pagesCapítulo 9 Teoría Microbiología GeneralMarianoo Montalvo FonsecaNo ratings yet
- Estructuras de Las ProteínasDocument9 pagesEstructuras de Las ProteínasBruno Vega ChicomaNo ratings yet
- Estructuras de Las ProteínasDocument11 pagesEstructuras de Las ProteínasBruno Vega ChicomaNo ratings yet
- Lanzaderas Malato-AspartatoDocument10 pagesLanzaderas Malato-AspartatoPaola MichaelNo ratings yet
- Control médico preventivo frente a exposición de bencenoDocument18 pagesControl médico preventivo frente a exposición de bencenodocfon100% (1)
- Biosintesis de Aminoacidos en Escherichia ColiDocument15 pagesBiosintesis de Aminoacidos en Escherichia ColiPilar HerreraNo ratings yet
- Orson Scott Card - Un Planeta Llamado TraicionDocument185 pagesOrson Scott Card - Un Planeta Llamado TraicionIvone ConstanzaNo ratings yet
- Histología: Tejido EpitelialDocument3 pagesHistología: Tejido EpitelialLizeth Olivares VelasquezNo ratings yet
- Contenido de Instrumental Por Canastas o EquiposDocument3 pagesContenido de Instrumental Por Canastas o EquiposErik LlanesNo ratings yet
- Tubos de MuestraDocument8 pagesTubos de MuestraELIZABETH DEL ROSIO MARISCAL OLAYANo ratings yet
- Texto de Parasitología IDocument39 pagesTexto de Parasitología IJamie Jayjay MartinezNo ratings yet
- Introducción A La HistologíaDocument30 pagesIntroducción A La HistologíaRomiglio AlejandroNo ratings yet
- Renal NormalDocument87 pagesRenal NormalErika MelendezNo ratings yet
- Jiu Jitsu de Hoy Vol 1-2Document90 pagesJiu Jitsu de Hoy Vol 1-2pockeraul100% (1)
- Especialidad de InsectosDocument6 pagesEspecialidad de Insectoskesler YosNo ratings yet
- CARILLASDocument3 pagesCARILLASGregory UcvNo ratings yet
- Oxalato CarbonatoDocument1 pageOxalato Carbonatonathy00015No ratings yet
- Metodología del entrenamiento pliométricoDocument4 pagesMetodología del entrenamiento pliométricoanttuane100% (1)
- Fisiología de Los Cloroplastos y FotosíntesisDocument31 pagesFisiología de Los Cloroplastos y FotosíntesisLALUKISNo ratings yet
- Tiens AcumagicDocument59 pagesTiens Acumagicelizabeth1199100% (3)
- RESIDENTESSSSSSSSSSDocument38 pagesRESIDENTESSSSSSSSSSDenise RomeroNo ratings yet
- Manual de fichas técnicas JUNAEBDocument91 pagesManual de fichas técnicas JUNAEBPublihuella LtdaNo ratings yet
- Fermentacion Bioquimica InformeDocument5 pagesFermentacion Bioquimica InformeAndrés FelipeNo ratings yet
- Protocolo Evaluación Clinica Del HABLADocument7 pagesProtocolo Evaluación Clinica Del HABLAMatias OlguinNo ratings yet
- Presión Venosa CentralDocument8 pagesPresión Venosa CentralMonserrat Gomez100% (1)
- Evaluación neurológica completa en niñosDocument16 pagesEvaluación neurológica completa en niñosMaría Fernanda Solís SáurezNo ratings yet
- "Intervención Deglutoria en Población Pediátrica": Rodrigo Morales FernándezDocument30 pages"Intervención Deglutoria en Población Pediátrica": Rodrigo Morales FernándezLisbeth Herrera CofréNo ratings yet
- Tesis AcupunturaDocument71 pagesTesis AcupunturaLorenaNo ratings yet
- Refuerzo Tema 3 Las Funciones VitalesDocument3 pagesRefuerzo Tema 3 Las Funciones VitalesEva LoureiroNo ratings yet
- Alteraciones Viso-Espaciales y Viso-MotorasDocument20 pagesAlteraciones Viso-Espaciales y Viso-MotorasDaniel Cortes100% (1)
- Músculos Del RostroDocument8 pagesMúsculos Del RostroJacqueline Steffi Monterroso0% (1)
- Hematopoyesis Morfo 2Document46 pagesHematopoyesis Morfo 2Ely CadenasNo ratings yet
- OSTEOLOGIA Unidad 3Document86 pagesOSTEOLOGIA Unidad 3ANGIE VALENTINA GUERRERO JAIMESNo ratings yet