Professional Documents
Culture Documents
Determinación de Ácido Ascórbico Por Potenciometria
Uploaded by
Ronald67%(6)67% found this document useful (6 votes)
1K views3 pagesOriginal Title
Determinación de ácido ascórbico por potenciometria.docx
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
67%(6)67% found this document useful (6 votes)
1K views3 pagesDeterminación de Ácido Ascórbico Por Potenciometria
Uploaded by
RonaldCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 3
DETERMINACIN DE CIDO ASCRBICO POR POTENCIOMETRA
Ronald Quispe Lipa, Liz Angela Huallpara
Laboratorio de Qumica Analtica IV
Campus Universitario, Cota-Cota. Calle Nro.27
Telfono 591 2 795878 , Fax 591 2 772269
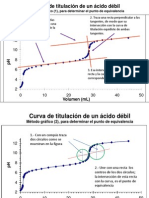
punto mximo (punto de inflexin), valor que se toma
como el punto final de la titulacin. Es claro que tambin
RESUMEN
se puede obtener el punto final de la titulacin a partir de
En el presente trabajo se determina la concentracin de la representacin grfica de 2 /2 en funcin del
cido ascrbico presente en pastillas farmacuticas con volumen promedio del titulante. En este caso, se toma
cido ascrbico (Vitamina C) mediante titulaciones como punto final de la titulacin a la interseccin de la
potencio mtricas acido-base, midiendo el pH a cada curva con eje de los volmenes agregados.
adicin de base. A partir de estos datos, procedemos a
El punto del punto final se encuentra entre los volmenes
calcular el punto equivalente de la reaccin por mtodos
donde la primera derivada tiene un valor mximo. La
grficos de la primera y segunda derivada. Al aplicar estos
segunda derivada presenta un cambio de signo en este
conceptos de clculo del unto equivalente, se encuentra la
mismo punto y para calcular el punto de equivalencia se
cantidad de cido ascrbico presente en la pastilla de
aplica la siguiente interpolacin:
10000 cuya concentracin es:
= + ( ) ()
+
INTRODUCCIN
Los valores de las segunda derivada se toman en valor
Valoraciones potencio mtricas acido-base. - Las
absoluto, adems, de que es el incremento entre punto
valoraciones de este tipo consisten en medir el pH de la
y punto, convenientemente debe ser constante cerca del
solucin por medio de un pH metro, a medida que se va
punto final
aadiendo el titulante. En el primer instante, el valor de
pH lo dar al analto, a medida que se agregue la cantidad
de titulante, los protones presentes en la muestra se van
cido ascrbico. - La vitamina C debe su acidez a los
neutralizando con los iones OH- del titulante. Cuando
disminuye la concentracin de protones en la muestra, el grupos -OH prximos al doble enlace. Uno de estos, el
que se encuentra sobre el carbono ms alejado del grupo
valor de pH va aumentando, este fenmeno puede ocurrir
carbonilo, forma un doble enlace con el carbono prximo
de manera drstica, o de manera suave, de acuerdo a las
especies en cuestin. (carbono gamma) cediendo un par de electrones, y
convirtindose en un grupo oxonio (=OH+).
Determinacin del punto equivalente. - Para poder Simultneamente, el doble enlace C=C se mueve hacia el
determinar el punto final de la valoracin se puede usar carbono del grupo ester de la lactona, y
los mtodos grficos o tambin llamados analticos. Entre consecuentemente, el par de electrones del doble enlace
estos mtodos se encuentra el mtodo directo, que es la carbonilo (C=O) se transfieren al tomo de oxgeno para
representacin directa del pH en funcin del volumen de formar un enolato (C-O-). Una vez formada, la especie
titulante (base) agregado. Para estimar el punto final de oxonio-enolato se desprotona dando a un carbonilo en el
por este mtodo, se toma el punto medio de la porcin carbono gamma; este protn es el causante de la acides
ascendente de la curva, y este valor es el punto final dela del cido ascrbico. Este enolato resultante entra en
titulacin. Otra forma de ser ms preciso es el de realizar resonancia con la espacie oxonio-enolato, lo cual le da
un grafico / (cambio de pH con el incremento de gran estabilidad.
volumen de titulante) en funcin del volumen valorante.
En la representacin de esta curva se nos presente un
Para el clculo del volumen final de la titulacin, usamos
la ecuacin (1), y reemplazando datos, se tien:
4,00
= 8 + 0,5 ( )
4,00 + 3,06
= , mL
PARTE EXPERIMENTAL
Para determinar la cantidad de cido ascrbico en una V vs. pH
pastilla farmacutica, de marca Kirkland, se pes y
13.00
procedi a triturar la misma y disolvindolo y aforndolo
con 100mL agua destilada. Se prepar una solucin de 11.00
NaOH 0,1M y estandarizndolo con HCL estandarizado. 9.00
Para medir el pH de la solucin en estudio utilizamos un 7.00
pH metro digital marca HANNA modelo HI 98185.
5.00
DATOS Y DISCUSIONES 3.00
0 1 2 3 4 5 6 7 8 9 10 11 12
Masa de la pastilla: 1,417g, 100mg Vit C/pastilla.
Grafica 1.- V vs. pH
En la siguiente tabla se muestran los datos obtenidos en
la prctica, adems de los valores de la primera y
segunda derivada. / vs. V
0.60
VNaOH
(mL) pH 0.50
(, ) / / 0.40
(, )
0.30
0,00 3,41
0.20
1,00 3,95 1,00 0,54 0,54
0.10
2,00 4,22 2,00 0,27 0,14 1,00 -0,27 -0,27
0.00
3,00 4,43 3,00 0,21 0,07 1,00 -0,06 -0,06
-0.10 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
4,00 4,64 4,00 0,21 0,05 1,00 0,00 0,00
5,00 4,83 5,00 0,19 0,04 1,00 -0,02 -0,02 Grafico 2.- Grafica de la primera derivada
6,00 5,12 6,00 0,29 0,05 1,00 0,10 0,10
6,50 5,29 6,50 0,17 0,03 0,50 -0,12 -0,24 / vs. V
7,00 5,59 7,00 0,30 0,04 0,50 0,13 0,26
6.00
7,50 6,29 7,50 0,70 0,09 0,50 0,40 0,80
4.00
8,00 8,99 8,00 2,70 0,34 0,50 2,00 4,00
8,50 10,16 8,50 1,17 0,14 0,50 -1,53 -3,06 2.00
9,00 10,80 9,00 0,64 0,07 0,50 -0,53 -1,06 0.00
9,50 10,75 9,50 -0,05 -0,01 0,50 -0,69 -1,38 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
-2.00
10,00 10,86 10,00 0,11 0,01 0,50 0,16 0,32
11,00 11,04 11,00 0,18 0,02 1,00 0,07 0,07 -4.00
12,00 11,15 12,00 0,11 0,01 1,00 -0,07 -0,07 Grafico 2.- Grafico de la segunda derivada.
13,00 11,26 13,00 0,11 0,01 1,00 0,00 0,00
14,00 11,35 14,00 0,09 0,01 1,00 -0,02 -0,02
15,00 11,42 15,00 0,07 0,00 1,00 -0,02 -0,02 La concentracin del NaOH a partir de la concentracin
16,00 11,48 16,00 0,06 0,00 1,00 -0,01 -0,01 estandarizada del HCl, es igual a:
17,00 11,53 17,00 0,05 0,00 1,00 -0,01 -0,01
[] = ,
A partir del volumen calculado calculamos la variacin en nuestros resultados, posiblemente se deba a
concentracin del cido ascrbico en la solucin. datos errneos tomados en laboratorio. Sin embargo, las
grficas entres si, se asemejan entre s para dar un
resultado similar entre s.
8,28 0,0957
= = , BIBLIOGRAFA
12,5
J.G.Dick, QUMICA ANALTICA, Edit. El Manual
0,0634 176 1000
100 Moderno S.A. Mexico, 1979.
1000 1 1
= , Arze Landivar, Carlos Enrique, EQUILIBRIO
Este resultado, es la cantidad de cido ascrbico presente QUMICO, Producciones Cima, La Paz Boliva.
en la pastilla. Chang. R. QUIMICA, Ed. Mc Graw-Hill,
Pero es resultado es muy elevado con relacin a la 10ma edicin, Mexico 2010
concentracin reportada por la fbrica, que es de 100mg
de cido ascrbico por pastilla. Si consideramos este
resultado y hallamos el porcentaje de cido ascrbico
presente en la pastilla.
1,1158
% = 100% = , %
1,4170
De acuerdo con la tabla 1, entre los valores del cociente
de la segunda derivada tomamos en cuenta el valor ms
grande, norponiente a 8mL de la solucin de NaOH,
aplicando la ecuacin (1) podemos calcular el volumen
del punto final.
En la grfica 2 se puede observar que evidentemente
existe una relacin con los valores calculados con la
anterior ecuacin, existe una pequea variacin, pero
evidentemente tomamos como valor prximo a la
exactitud el calculado con la ecuacin (1) basndonos en
conceptos tericos.
La grafica de la segunda derivada no coincide con los
valores calculados, la curva de la ecuacin que atraviesa
al eje de los volmenes es menor a 8mL.
CONCLUCIONES
El porcentaje de cido ascrbico en una pastilla
farmacutica tiene un 78,74% de cido ascrbico.
La tcnica de potencio mtrica es favorable al momento
de analizar soluciones turbias, y no as necesariamente
incoloras, por tanto, no es necesario realizar un
tratamiento fino a la matriz de nuestros analto, adems
horrarnos tiempo.
Las tcnicas de determinacin de punto final de una
titulacin acido base, son relativamente ms exactas,
tericamente, aunque en nuestro caso, posee una gran
You might also like
- Análisis Cuantitativo de Analitos Con Base en Equilibrios RedoxDocument7 pagesAnálisis Cuantitativo de Analitos Con Base en Equilibrios RedoxDiego Emilio MorettNo ratings yet
- Informe No. 5 Determinacion de Calcio en Suplementos Vitamínicostónica Método Absorción Atómica PDFDocument23 pagesInforme No. 5 Determinacion de Calcio en Suplementos Vitamínicostónica Método Absorción Atómica PDFCeleste UrzúaNo ratings yet
- Practica No8 Reflejos en El Humano.-.Document14 pagesPractica No8 Reflejos en El Humano.-.Leion UchihaNo ratings yet
- Cuantificación de Cianuro de Hidrógeno, Como Tóxico Volátil, A Partir de Glucósidos CianogénicosDocument10 pagesCuantificación de Cianuro de Hidrógeno, Como Tóxico Volátil, A Partir de Glucósidos CianogénicosSilvia García0% (1)
- Ejercicios Ácidos Polipróticos y ComplejosDocument22 pagesEjercicios Ácidos Polipróticos y ComplejosSantiago100% (2)
- Informe Pka Rojo de MetiloDocument8 pagesInforme Pka Rojo de MetilomichNo ratings yet
- VOLUMETRÍA REDOX: Determinación de Peróxido de Hidrógeno y Vitamina C en Muestras ComercialesDocument4 pagesVOLUMETRÍA REDOX: Determinación de Peróxido de Hidrógeno y Vitamina C en Muestras ComercialesJessika ArguelloNo ratings yet
- Obtención de 1,4 Dihidropiridina 1Document21 pagesObtención de 1,4 Dihidropiridina 1AxelWarnerNo ratings yet
- Titulaciones AmperometricasDocument3 pagesTitulaciones AmperometricasJuzif AltairNo ratings yet
- Instrumentaciòn de Fluorescencia y FosforescenciaDocument47 pagesInstrumentaciòn de Fluorescencia y FosforescenciaAlex Heredia100% (3)
- Cuestionario Previo Práctica 1Document4 pagesCuestionario Previo Práctica 1Ricardo MarquezNo ratings yet
- Reporte de Complejos LecheDocument9 pagesReporte de Complejos LecheDaniel Díaz díaNo ratings yet
- Ejercicio Resuelto - Complejos-AcidezDocument4 pagesEjercicio Resuelto - Complejos-AcidezFernanda Castillo ÜNo ratings yet
- MEZCLA DE ÁCIDOSDocument8 pagesMEZCLA DE ÁCIDOSGeraldiine RamirezNo ratings yet
- Ápendice 1. Practica 1.toxicologíaDocument7 pagesÁpendice 1. Practica 1.toxicologíaAkai Tsuki0% (1)
- TP06 - Titulacion A de ParacetamolDocument3 pagesTP06 - Titulacion A de ParacetamolGustavo Hilario Gonzalez50% (4)
- Determinación Gravimétrica de Niquel en Una AleaciónDocument7 pagesDeterminación Gravimétrica de Niquel en Una Aleaciónjohinis100% (1)
- Valoracion EspectrofotometricaDocument9 pagesValoracion Espectrofotometrica.:("*"BLacK BuLLeT"*"):.100% (3)
- Informe de Gravimetria de CalcioDocument5 pagesInforme de Gravimetria de Calcioandres guerrero100% (1)
- DEBER 4 Analitica Jaime PérezDocument4 pagesDEBER 4 Analitica Jaime Pérezjaime perezNo ratings yet
- COMPLEXOMETRÍA PARTE II Determinación de La Dureza Total, CálcicaDocument9 pagesCOMPLEXOMETRÍA PARTE II Determinación de La Dureza Total, CálcicaGaby BenavidesNo ratings yet
- Practica 7 Normalizacion HCL NaOHDocument22 pagesPractica 7 Normalizacion HCL NaOHWENDY GUAMAN MENDOZA100% (1)
- Cuestionario CafeinaDocument3 pagesCuestionario CafeinaFernando GA100% (1)
- Analisis Espectros EsteresDocument3 pagesAnalisis Espectros EsteresIsadora PazNo ratings yet
- Informe Punto Isosbestico.Document13 pagesInforme Punto Isosbestico.Jesus Gerardo Lopez ColmanNo ratings yet
- Informe ClorurosDocument6 pagesInforme ClorurosKarol Lancheros CondeNo ratings yet
- Examen Parcial Prácticas 1-5 QuímicaDocument3 pagesExamen Parcial Prácticas 1-5 QuímicajimenaNo ratings yet
- Experimento 3 Sintesis Del BenzopinacolDocument4 pagesExperimento 3 Sintesis Del BenzopinacolBrandon CaballeroNo ratings yet
- Error de Valoración Debido Al IndicadorDocument2 pagesError de Valoración Debido Al IndicadorMaría Alejandra MaidanaNo ratings yet
- Determinación Espectrofotométrica de Hierro en Tabletas de Vitamina de Sulfato FerrosoDocument8 pagesDeterminación Espectrofotométrica de Hierro en Tabletas de Vitamina de Sulfato FerrosoRobertIgnacioEscalonaNo ratings yet
- Pto de Equivalencia, Determinacion GraficaDocument3 pagesPto de Equivalencia, Determinacion Graficamanolete4321No ratings yet
- Análisis Cuantitativo de Analitos Con Base en Equilibrios de Formación de ComplejosDocument3 pagesAnálisis Cuantitativo de Analitos Con Base en Equilibrios de Formación de ComplejosGabriela Pietra Santa100% (1)
- Reporte 4. Punto Isoeléctrico de ProteínasDocument13 pagesReporte 4. Punto Isoeléctrico de ProteínasErick Enriquez BacilioNo ratings yet
- Práctica 1. Titulación Ácido-BaseDocument4 pagesPráctica 1. Titulación Ácido-BaseArturoNo ratings yet
- Guía Ley de RepartoDocument1 pageGuía Ley de RepartoCarolina RoblesNo ratings yet
- PDF Apendice 1 Practica 1toxicologia CompressDocument4 pagesPDF Apendice 1 Practica 1toxicologia CompressCarlos Romo MartinezNo ratings yet
- Cuestionario IRDocument10 pagesCuestionario IRCarolinaJacksonScruseNo ratings yet
- Informe Determinación Espectrofotométrica Del Pka de Un Indicador PDFDocument12 pagesInforme Determinación Espectrofotométrica Del Pka de Un Indicador PDFLuis Espinoza PortuguezNo ratings yet
- Al y MG en AntiácidoDocument16 pagesAl y MG en AntiácidoDayanara Maurin0% (1)
- Informe Practica 3Document13 pagesInforme Practica 3Jose David Perez NavarroNo ratings yet
- Caracteristicas de Patrones PrimariosDocument3 pagesCaracteristicas de Patrones PrimariosValeriita Marisol BasantesNo ratings yet
- Adicion EstandarDocument7 pagesAdicion EstandarLuis Atencio0% (1)
- Indicadores MetalocromicosDocument1 pageIndicadores MetalocromicosEnriqueNo ratings yet
- Práctica 8. Orgánica IIIDocument4 pagesPráctica 8. Orgánica IIIWendy Núñez BedollaNo ratings yet
- Complejos Ni-ligantesDocument7 pagesComplejos Ni-ligantesRene Axel HakenNo ratings yet
- Previo 1Document5 pagesPrevio 1Daniel ChavarriaNo ratings yet
- Química Cuantitativa - Titulacion de VinagreDocument10 pagesQuímica Cuantitativa - Titulacion de Vinagrephtalic100% (3)
- Práctica 5. Espectroscopia UV-Vis de Compuestos de CoordinaciónDocument7 pagesPráctica 5. Espectroscopia UV-Vis de Compuestos de CoordinaciónMarisol GH0% (1)
- Determinación de la densidad del aguaDocument10 pagesDeterminación de la densidad del aguaSabrina MarinNo ratings yet
- Potenciometria ResumenDocument3 pagesPotenciometria ResumenMachetin MachetinNo ratings yet
- Acido AceticoDocument14 pagesAcido AceticoReyes OdraNo ratings yet
- Cabadillacastillo Marianoadrian 2im40Document10 pagesCabadillacastillo Marianoadrian 2im40Mariano CastilloNo ratings yet
- Práctica 2. Mezclas Ácidas y Potenciometría// Química AnalíticaDocument22 pagesPráctica 2. Mezclas Ácidas y Potenciometría// Química AnalíticaRosmaira MartínezNo ratings yet
- Determinación potenciométrica de pHDocument17 pagesDeterminación potenciométrica de pHRenzo Acevedo Cano100% (1)
- Guia Potenciometria de LaboratorioDocument3 pagesGuia Potenciometria de Laboratoriomaría josé fernández50% (2)
- Informe #6. Titulacion - PotenciometriaDocument10 pagesInforme #6. Titulacion - PotenciometriaIcarusNo ratings yet
- PotenciometriaDocument14 pagesPotenciometriaMishel MijaresNo ratings yet
- Palacios - Uriel - & - Rodriguez - Irais - 1284 - Anteproyecto - Constante - de - Acidez - Del - Acido - AceticoDocument11 pagesPalacios - Uriel - & - Rodriguez - Irais - 1284 - Anteproyecto - Constante - de - Acidez - Del - Acido - Acetico40-irais Rodríguez RiveroNo ratings yet
- Informe de Quimica Numero 9 Neutralizacion de AcidosDocument17 pagesInforme de Quimica Numero 9 Neutralizacion de AcidosCasaverde Jimmy100% (1)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Vector EsDocument1 pageVector EsRonaldNo ratings yet
- Capacitaciones en LaboratorioDocument3 pagesCapacitaciones en LaboratorioRonaldNo ratings yet
- Notas Rec Tic QMCDocument1 pageNotas Rec Tic QMCRonaldNo ratings yet
- Notas Inic. Tic Lab QMCDocument1 pageNotas Inic. Tic Lab QMCRonaldNo ratings yet
- Noo Lo EntiendoDocument1 pageNoo Lo EntiendoRonaldNo ratings yet
- Practica QuimicaDocument2 pagesPractica QuimicaRonaldNo ratings yet
- Examen 4ºDocument2 pagesExamen 4ºRonaldNo ratings yet
- Lo Siento MuhoDocument1 pageLo Siento MuhoRonaldNo ratings yet
- Determinación de Ácido Ascórbico Por PotenciometriaDocument3 pagesDeterminación de Ácido Ascórbico Por PotenciometriaRonald67% (6)
- Determinación de Fosfatos en Bebidas de ColaDocument4 pagesDeterminación de Fosfatos en Bebidas de ColaRonaldNo ratings yet
- Mapa Conceptual Practica IIIDocument1 pageMapa Conceptual Practica IIIKaren Julieth DuarteNo ratings yet
- Producción mensual de motores por modelo y colorDocument29 pagesProducción mensual de motores por modelo y colorLuz OrtizNo ratings yet
- Trepanos de PerforacionDocument363 pagesTrepanos de PerforacionDavid Blancos50% (2)
- INFORME DE PRECALIFICACIÓN Pad - San PabloDocument7 pagesINFORME DE PRECALIFICACIÓN Pad - San PabloAngel yonel Coz floresNo ratings yet
- Alteraciones de La UñaDocument8 pagesAlteraciones de La Uñaanon-577281100% (6)
- Cuestionario de CondensadoresDocument2 pagesCuestionario de CondensadoresPaoloPorrasArrietaNo ratings yet
- Lectura 2. para Una Fundamentación (Ludojoski)Document11 pagesLectura 2. para Una Fundamentación (Ludojoski)Carmen TanasiNo ratings yet
- Libros FisicaDocument4 pagesLibros FisicaJuan GordilloNo ratings yet
- Modelamiento ContaminacionDocument46 pagesModelamiento Contaminacionserderez0150% (2)
- Protocolo de Rehabilitación para Pacientes Adultos Mayores Con Enfermedad de Parkinson PDFDocument12 pagesProtocolo de Rehabilitación para Pacientes Adultos Mayores Con Enfermedad de Parkinson PDFMARIANA LEIVA ZÚÑIGANo ratings yet
- Ludopatia Escuela PDFDocument100 pagesLudopatia Escuela PDFJoseph Alvarez OropezaNo ratings yet
- PalaciosPérezG 2012 MaunquelluevaDocument193 pagesPalaciosPérezG 2012 MaunquelluevaPaula Andrea DelgadoNo ratings yet
- Un Clavado A Tu CerebroDocument5 pagesUn Clavado A Tu CerebroRaul Jimenez100% (3)
- F-AND-SGI-02 Planilla Matriz IPERC BASE AlmacenDocument41 pagesF-AND-SGI-02 Planilla Matriz IPERC BASE AlmacenjanetNo ratings yet
- CB Que Es La Pintura PDFDocument1 pageCB Que Es La Pintura PDFyo_lobehotmailcomNo ratings yet
- Procedimiento Gestión Integral de ResiduosDocument17 pagesProcedimiento Gestión Integral de Residuose_castellanos4100% (1)
- ECOLADRILLOSDocument47 pagesECOLADRILLOSneriNo ratings yet
- Declaraciones juradas LongarDocument4 pagesDeclaraciones juradas LongarJulio Antonio Chapoñan TejadaNo ratings yet
- Presentación Giovanni Valencia PinzónDocument45 pagesPresentación Giovanni Valencia PinzónGiovanni Valencia PinzónNo ratings yet
- Enfermedades NeurodegenerativasDocument6 pagesEnfermedades NeurodegenerativasNaida Kamila Garay MachucaNo ratings yet
- La Reproducción HumanaDocument11 pagesLa Reproducción HumanamanolovaldefierroNo ratings yet
- TEMPERATURA y MATERIA 4toDocument5 pagesTEMPERATURA y MATERIA 4toElsa CortesNo ratings yet
- Plan de Cierre de Minas YanacochaDocument4 pagesPlan de Cierre de Minas YanacochaGuiselaCenteno100% (1)
- Impacto de la Revolución Verde en la agricultura ecológicaDocument2 pagesImpacto de la Revolución Verde en la agricultura ecológica6621910034 MARIA JOSÉMORELO WILCHES ESTUDIANTE ACTIVONo ratings yet
- CelulasDocument8 pagesCelulaszidanek69No ratings yet
- Practica 5 DesnsidadDocument8 pagesPractica 5 DesnsidadAida QMNo ratings yet
- Matriz Riesgo Proyecto InternadoDocument40 pagesMatriz Riesgo Proyecto InternadojuandescargotoNo ratings yet
- Monografía Cromo y CadmioDocument18 pagesMonografía Cromo y CadmioKarina Irigoín SánchezNo ratings yet
- Escala de Busqueda de SensacionesDocument2 pagesEscala de Busqueda de SensacionesEthel SpNo ratings yet
- Induccion SSTDocument29 pagesInduccion SSTemmanuelNo ratings yet