Professional Documents
Culture Documents
Informe 3 Estequiometria de Una Reaccion
Uploaded by
Modesto Enrrique0%(1)0% found this document useful (1 vote)
477 views6 pagesreaccion
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this Documentreaccion
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0%(1)0% found this document useful (1 vote)
477 views6 pagesInforme 3 Estequiometria de Una Reaccion
Uploaded by
Modesto Enrriquereaccion
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 6
ESTEQUIOMETRI DE UNA REACCION QUIMICA.
Modesto Branda, Francisco Prez, Guerlain Martnez, Krysna Samudio,
Hillary Vivies
Prof. Luz Pinzn
Licenciatura en Ingeniera Martima y Portuaria-Centro Regional de Chiriqu-Universidad Tecnolgica de Panam.
Resumen.- El presente informe de laboratorio tiene como finalidad conocer la
definicin de estequiometria, calcular terica y experimentalmente las cantidades
de las sustancias que participan en una reaccin qumica e identificar el reactivo
limitante de la reaccin estequiometria mediante el clculo de los reactantes.
Adems se relacionara el reactivo limitante con la coloracin de la solucin final.
Se realizar una investigacin experimental que nos facilitar reconocer la
reaccin qumica. Para ello, utilizaremos los instrumentos de laboratorio y
realizaremos clculos adecuadamente.
Por ltimo se plantearn las conclusiones generales en torno a nuestros
procedimientos y resultados.
Palabras claves- Concentracin, soluciones, reaccin, precipitado, reactivo.
Abstract - The present laboratory report aims to know the definition of
stoichiometry, to calculate theoretically and experimentally the quantities of the
substances involved in a chemical reaction and to identify the limiting reactant of
the stoichiometry reaction by calculating the reactants. In addition, the limiting
reagent will be related to the coloration of the final solution.
An experimental investigation will be carried out that will facilitate us to
recognize the chemical reaction. For this, we will use the laboratory instruments
and perform calculations properly.
Finally, the general conclusions about our procedures and results will be
presented.
Keywords - Concentration, solutions, reaction, precipitate, reagent.
del producto y las relaciones
cuantitativas entre los elementos y
I. Introduccin. los compuestos en una reaccin
En este tema que trata de qumica. La estequiometria se aplica
estequiometria de la reaccin se en muchas reas tanto industriales,
necesitan saber conceptos claves comerciales y en la vida cotidiana,
como son: los conceptos de mol, por esto es importante saber que este
relacin de masa-masa, masa- laboratorio nos permitir afianzar
volumen, entre otros. Conceptos que nuestros conocimientos y mejorar
nos ayudaran a entender este tema nuestras habilidades a la hora de
de gran Importancia, ya que, la trabajar con cualquier tipo de
estequiometria nos permite saber y reaccin.
obtener una determinada cantidad
II. Impacto social.
IV. Procedimiento.
En la actualidad, la industria y la
contaminacin se han relacionado
entre s y aceptado como un mal de
estos tiempos. Estas obras y rotular 9 tubos de ensayos
actividades son capaces de provocar llenar
cambios en el entorno, pero no por
con Cloruro de bario 0.5 M segn
ello debemos paralizar el desarrollo indica la tabla N1
ni eliminar la produccin, sino por el colocarlos
contrario, existen cada vez ms
medios desarrollados a su vez para en bao mara por unos minutos
permitir las actividades siendo bajar
respetuosos con el Medio Ambiente,
siendo uno de estos medios la la temperatura antes de que hierva
estequiometria ya que se encarga del esperar
estudio cuantitativo de los reactivos y
productos que participan en una 10 minutos y apagar
reaccin, es decir, la estequiometria
agregar
hace un balance de masas
indicndonos fielmente el costo y la a los 9 tubos lacantidad de
cromato de potasio 0.5M
ganancia a la que nos llevara la
segn
comercializacin de dicho producto,
lo cual es un principio bsico en indica la tabla N1
cualquier industria. En este proceso,
colocarlos
se optimizan las reacciones, y los
gastos para tener productos de en un vaso qumico con agua fria
los tubos
calidad.
observar
III. Material y reactivos.
Materiales: la formacin de presipitado
Tubos de ensayos esperar
Vasos qumicos
Mechero 20 minutos
Bureta de 100 ml medir
Gradilla la altura del presipitado de cada
Marcador tubo
Regla milimetrada registrar
Pinza para tubo de ensayo
en la tabla N1
Pipeta serolgica
Cinta adhesiva hacer
Reactivos: los clculos de la tabla N2
2
24
Resultados.
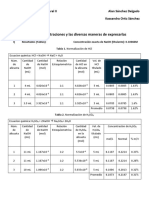
Tabla N1 estequiometria de una
reaccin
N de 1 2 3 4 5 6 7 8 9
tubos
BaCl2 1 2 3 4 5 6 7 8 9
0.5M
ml
K2CrO4 9 8 7 6 5 4 3 2 1
0.5M
ml
Altura 5 7 9 11 11.5 11 9 7 5
del
precitado
.
En mm.
Tabla N2 estequiometria de una
reaccin
V. Discusin.
Primero que nada hay que especificar
que es una reaccin y no es ms que
un proceso por el cual una o ms
sustancias, llamadas reactivos, se
transforman en otra u otras
sustancias con propiedades
diferentes, llamadas productos en
una reaccin qumica no
necesariamente se consume la
totalidad de los reactivos.
Generalmente alguno de ellos se
encuentra en exceso. El otro reactivo,
que es el que se consume totalmente
se conoce como reactivo limitante y
basta con que se agote para que la
reaccin termine.
Cualquier clculo
estequiomtrico que se lleve a cabo,
debe hacerse en base a una ecuacin
qumica balanceada, para asegurar
que el resultado sea correcto, en este
laboratorio en particular pudimos
observar como variaba la cantidad de
precipitado que se formaba al llevar a
cabo la reaccin entre el cromato de
potasio y el cloruro de bario, donde al
haber misma o similar cantidad de
reactivos ms producto se generaba
en otras palabras un mol de cloruro
de bario reacciona con un mol de
cromato de potasio y ambas
sustancial son de 0.5 mol por lo tanto
de tener 5 ml de cada uno esta
reaccionaria en su totalidad esto se
debe a que para que esta reaccin
ocurriese requera de una misma
cantidad de reactivos sea que si
agregbamos ms de uno de los
reactivos no se producira el mayor
rendimiento posible para esta
reaccin.
VI. Cuestionario.
1) Qu relacin existe entre la
coloracin de los tubos y la
altura del precipitado?
Identifique el reactivo
limitante con base a la
coloracin de la solucin.
4) Identifique las posibles
R= Al terminar el experimento nos
fuentes de error.
dio como resultado una solucin
amarilla que entre ms cromato de
potasio agregbamos se hara ms
claro. Del 1 al 4 fueron los colores R= Algunos posibles errores
ms puros sacamos en conclusin pudieron ser no tomar el tiempo
que es porque el reactivo limitante correcto que se indicaba en el
era el cloruro de bario. experimento. Utilizar instrumentos
incorrectos y sucios. Realizar
En el tubo nmero 5 el tubo un clculos inadecuados a la hora de las
momento de equivalencia ya que mediciones.
ambas cantidades tenan las mismas
medidas reaccionaron Problemas
perfectamente.
Del tubo 6 al 9 el color amarillo se
torna ms claro, supusimos que
ahora el reactivo limitante era el
cromato de potasio.
2) Grafique el nmero de moles
de reactivo (abscisa) vs altura
de precipitado (ordenada) en
un papel milimetrado. Haga
una grfica para cada reactivo.
En cada grafica busque el
punto de inflexin y
establezca a que valor de la
abscisa corresponde.
3) Escriba la ecuacin qumica
para la reaccin entre BaCl2 y
K2CrO4 y determine la
estequiometria de la ecuacin
VII. Conclusiones.
Culminada la experiencia pudimos
llegar a las siguientes conclusiones:
Relacionamos la concentracin
de las soluciones que
reaccionaron con el precipitado y
est de ms mencionar porque se
gener una mayor cantidad de
precipitado a medida que estos
tenan misma cantidad de
reactivos y es que cabe destacar
que un mol de cloruro de bario
reacciona con un mol de cromato
de potasio y ambas sustancial son
de 0.5 mol por lo tanto de tener 5
ml de cada uno esta reaccionaria
en su totalidad.
En una reaccin qumica que est
asociada con el rendimiento
siempre es de vital importancia
conocer los reactivos y basta con
tener una ecuacin balanceada
para saber cul se agotara
primero.
En todo tipo de ecuacin qumica
se presentan dos partes los
reactivos que son aquellas
sustancias las cuales van a
combinarse o a disociarse para
dar paso a nuevos elementos o
compuestos.
VIII. Referencia.
Qumica general II Folleto de
laboratorio para estudiantes de la
Facultad de Ingeniera Civil.
Brown, T. Lemay, L. 2014.
Qumica la ciencia central. 12va
edicin. Pearson education.
http://www.monografias.com/tr
abajos87/la-estequiometria/la-
estequiometria.shtml
https://es.wikipedia.org/wiki/Re
activo_limitante
https://www.clubensayos.com/C
iencia/Mediciones/2009312.htm
l
Chang, Raymond. Qumica, 6
edicin, Editorial Mc Graw Hill,
1999. Cap. 3
You might also like
- Estequiometria de Una ReacciónDocument7 pagesEstequiometria de Una ReacciónAna Cristina Pérez IsaacsNo ratings yet
- Lab.8. Estequiometría de Una ReacciónDocument7 pagesLab.8. Estequiometría de Una ReacciónOmar SanchezNo ratings yet
- Experimento N°6: Estequiometria de Una Reacción QuímicaDocument12 pagesExperimento N°6: Estequiometria de Una Reacción QuímicaHenry Molina100% (5)
- Estequiometria de Una ReaccionDocument7 pagesEstequiometria de Una ReaccionCristy ChacónNo ratings yet
- Laborotorio N°7 Ley de BoyleDocument9 pagesLaborotorio N°7 Ley de BoyleAlexisRai0% (1)
- Laboratorio Estequiometria de Una Reaccion QuimicaDocument8 pagesLaboratorio Estequiometria de Una Reaccion QuimicaEilith0% (1)
- Informe 7 Oxido ReduccionDocument11 pagesInforme 7 Oxido Reduccionpablobonds31No ratings yet
- Estequiometria de Una Reaccion QuimicaDocument16 pagesEstequiometria de Una Reaccion QuimicaOrlandoOmar100% (1)
- Informe de Laboratorio #3Document10 pagesInforme de Laboratorio #3lester11aaron43% (7)
- Laboratorio de Quimica 9Document24 pagesLaboratorio de Quimica 9Jonathan Chirú64% (14)
- Uso de Las Leyes de Los Gases en La Determinación de Hidrogenocarbonato de Sodio en Una Muestra de Alka-SeltzerDocument15 pagesUso de Las Leyes de Los Gases en La Determinación de Hidrogenocarbonato de Sodio en Una Muestra de Alka-SeltzerEnrique Rodriguez85% (13)
- Lab #7Document9 pagesLab #7Danny SantiagoNo ratings yet
- Determinación del porcentaje de ácido acético en vinagre mediante titulaciónDocument9 pagesDeterminación del porcentaje de ácido acético en vinagre mediante titulaciónsecNo ratings yet
- Laboratorio #6 Tipos de Reacciones QuimicasDocument8 pagesLaboratorio #6 Tipos de Reacciones QuimicasIsrael Murillo100% (1)
- Informe QuimicaDocument27 pagesInforme QuimicaDaves SanjurNo ratings yet
- Laboratorio N°8Document6 pagesLaboratorio N°8kewy1650% (2)
- Determinación Del Peso Molecular de La Acetona Por El Método de DumasDocument8 pagesDeterminación Del Peso Molecular de La Acetona Por El Método de DumasRuiz Herrera Elihu GerardoNo ratings yet
- Lab 3 Quimica General UtpDocument5 pagesLab 3 Quimica General UtpAdrian Concepcion100% (1)
- Informe Quimica 2 REDOX Parte 1 CuerpoDocument11 pagesInforme Quimica 2 REDOX Parte 1 Cuerpoluis vegaNo ratings yet
- Determinación de ácido acético en vinagreDocument8 pagesDeterminación de ácido acético en vinagreadalberto pittyNo ratings yet
- Contando AtomosDocument7 pagesContando AtomosGabriel Del RosarioNo ratings yet
- Laboratorio Determinación de La Acidez de Un Vinagre ComercialDocument13 pagesLaboratorio Determinación de La Acidez de Un Vinagre ComercialNemetNo ratings yet
- Informe de QuimicaDocument9 pagesInforme de QuimicaJOANNo ratings yet
- Reacciones redox laboratorio químicaDocument7 pagesReacciones redox laboratorio químicaAbelCastilloJp100% (5)
- Laboratorio 5 Oxido-Reduccion CompletoDocument6 pagesLaboratorio 5 Oxido-Reduccion CompletoDanelis AnethNo ratings yet
- Diagramas de fases de sistemas binariosDocument14 pagesDiagramas de fases de sistemas binariosChristian RodríguezNo ratings yet
- Informe 13Document6 pagesInforme 13Ale GaskarthNo ratings yet
- 2 Port 1 Ex QGP I1 Sem 2020Document4 pages2 Port 1 Ex QGP I1 Sem 2020Diego Vásquez100% (1)
- Evaporación, Calor y Tranf. de Energía (Alcohol - Papel Toalla)Document3 pagesEvaporación, Calor y Tranf. de Energía (Alcohol - Papel Toalla)Danelis Aneth33% (3)
- Informe de Lab.3 EstequiometriaDocument7 pagesInforme de Lab.3 EstequiometriaAlberto HenriquezNo ratings yet
- Laboratorio Nro.7 Quimica IDocument13 pagesLaboratorio Nro.7 Quimica Iyui50% (2)
- Practica 7, EstequiometriaDocument5 pagesPractica 7, EstequiometriaCuellarMartinezNo ratings yet
- Elementos electrónicos básicos: símbolos, diagramas y utilidadDocument4 pagesElementos electrónicos básicos: símbolos, diagramas y utilidadStacy ArauzNo ratings yet
- Informe 1 EXPERIMENTO N 2 Contando ÁtomosDocument4 pagesInforme 1 EXPERIMENTO N 2 Contando ÁtomosFernando CanoNo ratings yet
- Quimica Lab 3Document7 pagesQuimica Lab 3jeremy mendoza almanzaNo ratings yet
- Laboratorio No 3 QuimicaDocument10 pagesLaboratorio No 3 QuimicaFher RojasNo ratings yet
- Ejercicio Entalpia de VaporizaciónDocument6 pagesEjercicio Entalpia de VaporizaciónNERY ABRAHAM LOPEZ JAIMES100% (2)
- Preparación de Disoluciones y Determinación de La Concentración de Una Disolución Por Medio de Una ValoraciónDocument2 pagesPreparación de Disoluciones y Determinación de La Concentración de Una Disolución Por Medio de Una ValoraciónDaniela EsperanzaNo ratings yet
- Práctica 6 Propiedades Coligativas. Soluciones de Noe y Electrolitos Cuestionario PrevioDocument9 pagesPráctica 6 Propiedades Coligativas. Soluciones de Noe y Electrolitos Cuestionario PrevioKazuyaUedaTatsuyaNo ratings yet
- Vinagre Concentración Ácido AcéticoDocument6 pagesVinagre Concentración Ácido AcéticoAnaid CordobaNo ratings yet
- Cuestionario de AplicaciónDocument2 pagesCuestionario de AplicaciónKeitlyn Anahí Martínez0% (1)
- Formulario Equilibrio y CinéticaDocument4 pagesFormulario Equilibrio y CinéticaAlicia MartinezNo ratings yet
- Informe de Laboratorio n#4Document13 pagesInforme de Laboratorio n#4lester11aaron60% (5)
- Experimento #13Document8 pagesExperimento #13JuanC27No ratings yet
- Lab Propiedades Coligativas UtpDocument6 pagesLab Propiedades Coligativas UtpRoger Yves Concepción VíquezNo ratings yet
- Practica 02 FQ 2018Document3 pagesPractica 02 FQ 2018juancalp81100% (1)
- Reporte 3 Analisis CualitativoDocument20 pagesReporte 3 Analisis CualitativoPablo DLNo ratings yet
- Previo 5Document4 pagesPrevio 5Brenda CoronandoNo ratings yet
- Pract. 3 QuimicaDocument6 pagesPract. 3 QuimicaYli S'cNo ratings yet
- Informe de Quimica 1 Acidos y BasesDocument16 pagesInforme de Quimica 1 Acidos y BasesLuis Alberto Vega GuerraNo ratings yet
- Tarea 3 EnlaceDocument13 pagesTarea 3 EnlaceCORDOVA PEREZ MAYLI JHEOMARA100% (1)
- Péndulo simple: Teoría y experimentoDocument16 pagesPéndulo simple: Teoría y experimentoNataniel AdamesNo ratings yet
- Identificación de sustancias ácidas, básicas o neutras mediante experimento de magnesioDocument2 pagesIdentificación de sustancias ácidas, básicas o neutras mediante experimento de magnesioHumber Leon100% (1)
- Practica N°9Document19 pagesPractica N°9Jorge Frias100% (1)
- Practica 7 Equivalencia Calor TrabajoDocument5 pagesPractica 7 Equivalencia Calor TrabajoElusaNo ratings yet
- Practica 2Document5 pagesPractica 2Alex RamosNo ratings yet
- Tarea1 FISICA II 2022 2Document8 pagesTarea1 FISICA II 2022 2David RomeroNo ratings yet
- Informe 3 Estequiometria de Una ReaccionDocument6 pagesInforme 3 Estequiometria de Una ReaccionK u r i s u t e r uNo ratings yet
- P-10 Calculos EstequiometricosDocument7 pagesP-10 Calculos Estequiometricosjose david de arco de avilaNo ratings yet
- Practica N °2Document6 pagesPractica N °2mijaheel ferrufinoNo ratings yet
- Anteproyecto de EconomíaDocument4 pagesAnteproyecto de EconomíaModesto EnrriqueNo ratings yet
- Propiedades PeriódicasDocument7 pagesPropiedades PeriódicasModesto EnrriqueNo ratings yet
- Determinación de La Acidez de Un VinagreDocument6 pagesDeterminación de La Acidez de Un VinagreModesto Enrrique100% (2)
- EnlacesQuímicos: CaracterísticasIónicoCovalenteDocument8 pagesEnlacesQuímicos: CaracterísticasIónicoCovalenteModesto EnrriqueNo ratings yet
- EnlacesQuímicos: CaracterísticasIónicoCovalenteDocument8 pagesEnlacesQuímicos: CaracterísticasIónicoCovalenteModesto EnrriqueNo ratings yet
- Reacciones QuímicasDocument10 pagesReacciones QuímicasModesto EnrriqueNo ratings yet
- Conta ProyectoDocument4 pagesConta ProyectoModesto EnrriqueNo ratings yet
- Ley de HookeDocument5 pagesLey de HookeModesto EnrriqueNo ratings yet
- Segunda Ley de NewtonDocument3 pagesSegunda Ley de NewtonModesto EnrriqueNo ratings yet
- Cálculos y ResultadosDocument6 pagesCálculos y ResultadosModesto EnrriqueNo ratings yet
- Hiperboloide de RevoluciónDocument9 pagesHiperboloide de RevoluciónModesto EnrriqueNo ratings yet
- Propiedades PeriódicasDocument1 pagePropiedades PeriódicasModesto EnrriqueNo ratings yet
- Coeficiente de FriccionDocument6 pagesCoeficiente de FriccionModesto EnrriqueNo ratings yet
- Coeficiente de FriccionDocument6 pagesCoeficiente de FriccionModesto EnrriqueNo ratings yet
- Movimiento Circular UniformeDocument8 pagesMovimiento Circular UniformeModesto EnrriqueNo ratings yet
- Determinación de La Acidez de Un VinagreDocument6 pagesDeterminación de La Acidez de Un VinagreModesto Enrrique100% (2)
- Movimiento Circular UniformeDocument4 pagesMovimiento Circular UniformeModesto EnrriqueNo ratings yet
- Movimiento RectilíneoDocument6 pagesMovimiento RectilíneoModesto EnrriqueNo ratings yet
- Reacciones QuímicasDocument10 pagesReacciones QuímicasModesto EnrriqueNo ratings yet
- Proyecto de Quimica LabDocument29 pagesProyecto de Quimica LabModesto EnrriqueNo ratings yet
- Propiedades PeriódicasDocument7 pagesPropiedades PeriódicasModesto EnrriqueNo ratings yet
- Quimica Decimo A, B, C, D, F Tercer PeriodoDocument10 pagesQuimica Decimo A, B, C, D, F Tercer PeriodoLuis fernando AriasNo ratings yet
- LaboDocument5 pagesLaboJohnjairo Edu Romero EspinoNo ratings yet
- Quimica 101-200Document100 pagesQuimica 101-200juan colqueNo ratings yet
- Silabo Quimica General (2022 A) Zunilda LuzDocument11 pagesSilabo Quimica General (2022 A) Zunilda LuzCARLOS GONZALO MAMANI QUISPENo ratings yet
- Balanceo de Ecuaciones QuimicasDocument12 pagesBalanceo de Ecuaciones QuimicasKevin AjilaNo ratings yet
- Tipos diagramas procesos químicosDocument28 pagesTipos diagramas procesos químicosJesús García100% (1)
- Metodos CineticosDocument21 pagesMetodos CineticosReynel A. LugoNo ratings yet
- Guia EstequiometriaDocument3 pagesGuia EstequiometriaRamón Diaz0% (1)
- Cesar Arturo Sopla Rivera - Tarea Individual 7 - Reacciones QuimicasDocument3 pagesCesar Arturo Sopla Rivera - Tarea Individual 7 - Reacciones QuimicasJimena Jimenez AlvitesNo ratings yet
- Problemas Q Inorganica 2007-08Document15 pagesProblemas Q Inorganica 2007-08Victor Sabrera ChiaNo ratings yet
- Ley de La Conservación de La MateriaDocument17 pagesLey de La Conservación de La MateriaDANIELA SOFIA ANGEL ESCOBARNo ratings yet
- Definiciones y conceptos básicos de gases, estequiometría, catalizadores y leyes químicasDocument4 pagesDefiniciones y conceptos básicos de gases, estequiometría, catalizadores y leyes químicasALEXANDRA IRENE DEL AGUILA MENDOZANo ratings yet
- Caracterizacion Quimica ArrozDocument6 pagesCaracterizacion Quimica ArrozSil RamírezNo ratings yet
- Actividades de Aprendizaje Química BalanceoDocument8 pagesActividades de Aprendizaje Química Balanceomceres.calidadNo ratings yet
- Taller EstequiometriaDocument2 pagesTaller EstequiometriaJuan De La HozNo ratings yet
- BALANCEDocument3 pagesBALANCELuis CarrilloNo ratings yet
- Combustion de Gas 1Document15 pagesCombustion de Gas 1Ivonne Yadira Caracusma CondoriNo ratings yet
- Consulta #3Document8 pagesConsulta #3Joselyn Nicole Noguera ZambranoNo ratings yet
- Practica 7, EstequiometriaDocument5 pagesPractica 7, EstequiometriaCuellarMartinezNo ratings yet
- Programa de QUÍMICA II BachilleratoDocument28 pagesPrograma de QUÍMICA II Bachilleratoakuma3621No ratings yet
- Consulta EstequiometríaDocument11 pagesConsulta EstequiometríaLuis MuñozNo ratings yet
- Reporte 4 LabQuiDocument12 pagesReporte 4 LabQuiPablo Andres Salazar SabillonNo ratings yet
- Cuestionario Practica 6Document5 pagesCuestionario Practica 6luis caisaluisaNo ratings yet
- Unidad 2 - Carmen PuertaDocument10 pagesUnidad 2 - Carmen PuertabuhodecadizNo ratings yet
- Jueves de Prueba Septimo QuimicaDocument7 pagesJueves de Prueba Septimo QuimicaMiguel Lemus GuzmánNo ratings yet
- Unidad2 BalancedemateriayenergiaDocument99 pagesUnidad2 BalancedemateriayenergiaRockdrigo ArellanoNo ratings yet
- F ESTEQUIOMETRIA-MICROBIANA-1.pdf 24589438 CompressedDocument10 pagesF ESTEQUIOMETRIA-MICROBIANA-1.pdf 24589438 CompressedJesús MonterrozaNo ratings yet
- Rendimiento de una reacción química: Práctica No8Document4 pagesRendimiento de una reacción química: Práctica No8Enigma -100% (1)
- Quimica Ii 2Document33 pagesQuimica Ii 2Elizabeth ReyesNo ratings yet
- BarniDocument29 pagesBarniBryt SotoNo ratings yet