Professional Documents
Culture Documents
Fisiologia y Fisiopatologia II Apuntes Completos Temas 1 40
Uploaded by
Yesica StCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Fisiologia y Fisiopatologia II Apuntes Completos Temas 1 40
Uploaded by
Yesica StCopyright:
Available Formats
lOMoARcPSD|2558484
Fisiología Y Fisiopatología II - Apuntes completos. Temas 1 -
40.
FISIOLOGÍA HUMANA (Universidad de Salamanca)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
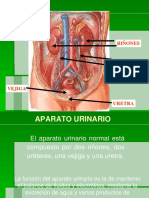
TEMA 1: ORGANIZACIÓN ESTRUCTRAL Y FUNCIONAL DEL SISTEMA RENAL
1. FUNCIONES DEL RIÑÓN
La orina se produce mediante filtración de una gran cantidad de fluido en el glomérulo, y
resorción y secreción de agua y solutos en el túbulo renal.
En cuanto a sus funciones:
- Regular el volumen y la composición del líquido extracelular (plasma y fluido
intersticial) mediante la formación de orina.
o Función fundamental
- Regular el volumen de plasma sanguíneo
o Regula la presión arterial y la función cardiovascular
- Eliminar productos de desecho del metabolismo
o Urea (nitrogenada), ácido úrico (purinas), creatinina (músculo)
- Regular la concentración plasmática de electrolitos
o Na+, K+, HCO3- y otros iones
- Regular la concentración de H+ (ph) , equilibrio ácido-base
- Producir o activar hormonas o precursores (eritropoyetina, renina, vitamina D)
- Eliminar fármacos y compuestos extraños o tóxicos.
2. SISTEMA URINARIO / ESTRUCTURA DEL RIÑÓN
Consta de dos riñones perfundidos por la vena cava renal. Tienen un punto de salida, uréter,
que lleva la orina hacia la vejiga urinaria. La estructura de los riñones (corte longitudinal) parte
de la corteza renal y hacia el interior la
médula renal (pirámides renales) hay
dos: una interna y la otra externa, la
punta de las pirámides se denomina
pupila. Dichas pirámides desembocan
a los cálices renales, que se distinguen
entre mayor y menor y de ahí al
uréter.
3. CIRCULACIÓN RENAL
Una rama de la arteria aorta irriga a los riñones, las arterias segmentarias se ramifican en una
arteria lobular y después forman las arterias arciformes que cada poco espacio forma ya las
arterias interlobulares, que se convierte en arteria aferente llega al glomérulo y cuando sale
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
del glomérulo forman los vasas rectas que se recomponen de nuevo en la vena interlobular y
vuelve hacer el mismo recorrido pero al revés.
4. NEFRONA
En los lóbulos están las nefronas, son las unidades estructurales, cada riñón tiene un millón de
nefronas, pero se van perdiendo a lo largo del tiempo. Las que se van perdiendo “pasan su
responsabilidad” a las que se quedan (se reduce con la edad se adaptan las restantes)
La nefrona consta de vasos sanguíneos (arterias/venas, capilares peritubulares, vasos rectos) y
de túbulos (proximal, asa de Henle, Distal, Colector)
Tipos de nefronas: se clasifican en función de la localización en el riñón y de la localización
también del glomérulo.
- NEFRONAS CORTICALES (superficiales) son aproximadamente el 85%, glomérulos
superficiales, están íntegramente en la corteza
- NEFRONAS YUXTAMEDULARES: glomérulos más profundos, asas de Henle penetran en
la médula, es más largo y la orina más concentrada que las nefronas anteriores.
5. GLOMÉRULO
Forma de globo formado por muchos capilares en su interior que se reordenan y salen por la
arteria aferente. Envuelta por una capa que es la cápsula de Bowman y la parte más interna es
la capa visceral. La capsula de Bowman está formada por un epitelio plano rodean al ovillo
capilar glomerular (red capilar que se deriva de la arteriola aferente y se reúne en la arteriola
eferente) y se continua con el túbulo proximal.
6. MEMBRANA DE FILTRACIÓN GLOMERULAR
La membrana basal glomérulo está formado por todos los componentes químicos que van a
dar estructura como por ejemplo: colágeno, laminina, heparin sulfato (ácidos ciánicos).
La membrana de filtración glomerular está compuesta por endotelio fenestrado, membrana
basal y pericitios (podocitos seudópodos que se dilatan de los cuales dejan filtrar la sangre)
con sus pedicelos. En el diafragma hay nefrina y podocina que forman una membrana que
selecciona las sustancias que van a filtrar a través del glomérulo. Entre toda esta estructura
está el mesangio glomerular, compuestos por las células mesangiales y la matriz mesangial,
que permite una mayor contracción, tiende a expandirse.
El liquido filtrado pasa a través desde la luz capilar al espacio de Bowman. Es 100-400 veces
más permeable al plasma, H2O y solutos cristaloides que los capilares del músculo esquelético.
Los poros evitan el paso de células, plaquetas y macromoléculas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La sangre filtrada en el glomérulo avanza por el tubo cortoneado este tubo está formado por
muchas macrovellosidades que hace que aumente mucho la superficie de absorción además
tiene muchas mitocondrias y muchos lisosomas, de lo que se filtra hay varias moléculas
fundamentales pero debido al tamaño se filtran otras y puede aparecer en la orina como por
ejemplo la glucosa, por ello hay unos mecanismo en los cuales en condiciones normales se
reabsorbe (trabajo extra que lo aporta las mitocondrias, interesa reabsorber todas esas
sustancias que se filtran). En la parte gruesa del asa de Henle la estructura cambia, pierden
intensidad debido a que tienen menos mitocondrias, es decir a medida que nos alejamos
disminuye la cantidad de mitocondrias, lisosomas… las células tienen un metabolismo menos
activo. Hay células escamosas en las ramas ascendentes y descendentes del asa de Henle. En el
tubo distal no lleva tampoco mucha reabsorción y el tubo colector tiene lugar la hormona anti
diurética. Hay una zona en la que el tabulo contorneado distal y la nefrona aferente coincide y
es ahí donde el aparato yuxtaglomerular. Las células yuxtaglomerulares forman el aparato
yuxtaglomerular son células lisas modificadas en la pared de la arteriola aferente que no solo
forman renina sino también la eritropoyetina (ayuda a la maduración de GR)
Otra estructura que se forma en el túbulo contorneado distal es la mácula densa formada por
células modificadas del túbulo distal y regulan la secreción de renina también. Y las células
mesangiales extraglomerulares se encuentran entre arteriolas aferentes y eferentes, y actúan
como soporte físico del aparato yuxtaglomerular.
SEGUNDA PARTE DEL TEMA 1: ORGANIZACIÓN ESTRUCTURAL Y FUNCIONAL DEL
SISTEMA RENAL
1. LOS URÉTERES
Son túbulos de músculo liso revestidos de un epitelio (urotelio cuando pasa orina el uréter
se acomoda perfectamente al cambio de volumen). Van desde la pelvis renal a la vejiga. Tienen
inervación simpática y parasimpática más plexo intramural de neuronas y fibras nerviosas.
Circulación: La orina en la pelvis produce una distensión que despolariza el músculo liso
visceral provocando ondas peristálticas (3cm/seg) aumentando así la presión intrauretral (50-
100mmHg) y por ultimo provoca el desplazamiento de orina a la vejiga.
La estimulación simpática disminuye la frecuencia de ondas, en cambio la estimulación
parasimpática aumenta la frecuencia de ondas.
Al hacer un corte transversal podemos distinguir 3 capas: la más interna que es la capa
mucosa, a continuación hay un musculo liso que puede ser longitudinal y circular que hace que
se produzcan las ondas peristálticas y la más externa la de tejido conectivo.
2. LA VEJIGA URINARIA
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Las paredes formadas por músculo liso visceral (músculo detrusor) revestidas de urotelio. Son
el reservorio para el almacenamiento de orina y la contracción del músculo detrusor vacía la
vejiga.
Se compone de varas partes: la más amplia es el cuerpo (trígono) y al final hay una estructura
en forma de triangulo (trigo) donde desembocan los uréter. Es como una solapa que permite el
paso pero impide el retroceso. Continúa con el cuello (uretra posterior), el esfínter uretral
interno y la uretra. Termina en el esfínter uretral interno que controla el vaciamiento de la
vejiga. Al hacer un corte trasversal en la vejiga se distingue: en capa mucosa (muy plegada),
músculo defrusor que es músculo liso y puede ser longitudinal y media, y por ultimo capa
visceral de tejido conectivo (envuelve a todas las estructuras)
En cuanto a su inervación:
- SN Parasimpático (nervios pélvicos) S2, S4 Cuerpo y cuello
- SN Simpático (nervio hipogástrico) L2 Cuerpo y cuello
- Fibras motoras (nervios pudendos) esfínter externo
Las terminaciones nerviosas reciben más señales propiocepticas. El órgano tendioso de Golgi y
el tubo muscular puede haber también sensaciones térmicas.
3. LA URETRA
La uretra va desde la vejiga urinaria al exterior del cuerpo, atraviesa el diafragma urogenital
(esfínter externo). Está formada por una capa mucosa y una capa de musculo liso (longitudinal
y circular)
Difiere en longitud y función en hombres y en mujeres. En el caso de los hombres a la salida
del esfínter externo está la parte prostática. Es de musculatura estriada por lo tanto es
voluntaria. Y en el caso de mujeres es más corta los esfínter externo y interno están más cerca
por lo tanto menos posibilidad de contraer la orina.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 2: FORMACIÓN DE LA ORINA I. FILTRACIÓN GLOMERULAR
1. FILTRACIÓN GLOMERULAR
Formación de una gran cantidad de ultrafiltrado a través de los capilares glomerulares hacia el
espacio de Bowman. Se produce por la elevada presión hidrostática del interior de los capilares
y la baja presión en el espacio de Bowman en un proceso similar al de otros lechos capilares.
La Tasa de Filtración Glomerular (TFG) es el volumen de filtrado producido por los dos riñones
por unidad de tiempo. Hay un promedio de 115mL/min (165 L/día) en mujeres; 125 mL/min
(180 L/día) en hombres.
La barrera de filtración limita el paso según el tamaño de las moléculas. Limitan los poros
capilares. Y según la carga eléctrica las macromoléculas cargadas negativamente (como las
proteínas plasmáticas) se repelen. Limitan las membranas de los podocitos.
Tipos de presiones:
- Presión hidrostática glomerular de la sangre que circula por los glomérulos (Pg) es el
factor más importante
- Presión hidrostática capsular (Pc) presión del liquido una vez filtrado, es
relativamente constante. En el caso de que aumente (HIDRONEFROSIS: es el líquido
que debería circular por el túbulo contorneado. Si hay alguna obstrucción impide que
avance por la que aumenta la presión y dificulta el paso, por ejemplo cuando hay una
obstrucción en las vías urinarias por un cálculo renal haciendo que aumente la orina)
se reduce el FG. Si disminuye aumente el FG
- Presión coloidosmótica del plasma (πg) aumenta a lo largo del capilar glomerular. Al
inicio del capilar 20 mmHg, al final del capilar 45 mmHg, media del capilar 32
mmHg. La elevada presión oncótica justifica la reabsorción en los capilares
peritubulares.
- Presión coloidosmótica capsular (πc) sin importancia fisiológica.
Resumiendo: el fluido cruza la barrera de filtración en respuesta a la presión hidrostática de la
sangre que circula por los glomérulos (Pg) y contra la presión hidrostática capsular (Pc) y la
presión coloidosmótica (fuerza osmótica) del plasma (πg)
o Presión hidrostática neta (P) = Pg – Pc
o Presión de filtración (PF) = P – πg
o Filtración glomerular: PF x Kf
Kf = coeficiente de filtración que depende del área capilar total (A) disponible para la filtración
y de la permeabilidad (P) de dicha área = A x P. El kf renal es de 400 veces mayor que en otros
capilares, es el más alto de todos los capilares del organismo.
2. REGULACIÓN DE FILTRACIÓN GLOMERULAR
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Va a depender del grado de contracción/relajación de las arteriolas. La vasocontricción o la
vasodilatación de las arteriolas aferentes y eferentes afectan al flujo sanguíneo real y,
secundariamente a la TFG.
Los mecanismo que regulan la TFG son (participan directamente) el sistema nervioso simpático
y la autorregulación. En cuanto a los cambios en el diámetro de las arteriolas ocurren por
mecanismos extrínsecos (por ejemplo dependen del volumen que haya) e intrínsecos (por
ejemplo la temperatura)
Constricción arteriola aferente: disminuye la presión del capilar por lo tanto disminuye
la GFR
Constricción arteriola eferente: aumenta la presión del capilar por lo tanto aumenta la
GFR
3. AUTOREGULACIÓN (autorregulación miógena) DEL FILTRADO GLOMERULAR
El riñón tiene capacidad para mantener una FG constante a pesar de los cambios sistémicos en
presión arterial. La autorregulación miógena cuando la PA cae por debajo de 70 mmHg, la
arteriola aferente se dilata y cuando la PA sube, la arteriola aferente se contrae.
Retroalimentación túbulo-glomerular: cuando aumenta el flujo tubular en las células de la
mácula densa, se envían señales constrictoras a la arteriola aferente.
La zona de autoregulación es fundamental para la regulación del organismo por parte de los
riñones. La presión glomerular se mantiene constante a 180 mmHg por día.
4. ACTIVACIÓN SIMPÁTICA
La activación simpática va a producir una contracción de la arteriola aferente lo que va a
provocar una disminución del FG y cambia la distribución intrarenal del flujo.
Además estimula la liberación de renina por el aparato yuxtaglomerular que modifica el
filtrado glomerular y aumenta la presión arterial debida a la liberación de renina.
5. MEDIADORES QUÍMICOS Y HORMONAS
ANGIOTENSINA II: actúa sobre arteriolas eferentes. Disminuye el flujo de capilares
peritubulares y aumenta la reabsorción
ADRENALINA Y NORADRENALINA: vasoconstricción aferente y eferentes disminuye
filtración y escasa influencia salvo situaciones extremas: hemorragias grave, en situaciones
extremas se activa el proceso vasoconstrictor
ENDOTELINA: vasoconstricción renal, disminuye FG
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
VASODILATADORES: PG, acetilcolina, bradiquinina, histamina que amortiguan los efectos del
simpático o angiotensina II que produce vasodilatación aferente y eferente y produce un
aumento de la filtración. El óxido nítrico favorece la excreción de Na y agua.
6. EL FLUJO SANGUÍNEO RENAL
El riñón es un órgano altamente vascularizado que recibe un 20% del gasto cardiaco,
aproximadamente unos 1200 mL/min. Si se tiene en cuenta el peso (300g) recibe 4 mL/g/min,
lo que significa una de las perfusiones más altas del organismo.
Aunque la sangre que sale del riñón contiene una presión parcial de oxígeno bastante alta, el
consumo de oxígeno por el riñón es muy elevado (alrededor de 17 mL/min) Casi todo el
oxígeno consumido por el riñón se utiliza para procesos de transporte tubular. La filtración y la
secreción solamente aclaran moléculas disueltas en el plasma.
No toda la sangre que llega al glomérulo se filtra a través de la membrana de filtración, de
hecho la mayor parte de la sangre sale por la arteriola eferente y se filtra un 20% del plasma
que pasa por los glomérulos (y la mayor parte de sus componentes vuelven a la circulación)
Flujo sanguíneo renal = PAH clearance (aproximadamente 1350 mL/min.) no toda sustancia
pasa por el glomérulo una parte de PHA se filtra sale por la arteriola eferente, y el resto es
secretado hacia el tubo. Esa cantidad nos indica la cantidad de sangre que ha pasado por el
riñón.
7. MEDIDA DEL FLUJO PLASMÁTICO RENAL
Hay substancias de la sangre no filtrada que son secretadas a los túbulos mediante transporte
activo (PAH) . Este aclaramiento de PAH puede ser usado para medir el flujo plasmático renal,
aproximadamente 740 mL/min. Para calcular el flujo sanguíneo renal hay que tener en cuenta
la cantidad de sangre ocupada por eritrocitos (hematocrito mide la concentración de células
que hay en la sangre). Si el hematocrito es 45%, 45% de la sangre son glóbulos rojos, 55%
plasma.
8. ACLARAMIENTO RENAL
Se puede calcular la tasa a la que una substancia se filtra en el glomérulo (siempre que sea
libremente filtrada):
CANTIDAD FILTRADA = TFG x P
CANTIDAD EXCRETADA = V x U
En condiciones normales, la cantidad filtrada es igual a la cantidad excretada.
El aclaramiento renal de una substancia libremente filtrada, que no se reabsorba ni se secrete,
mide la tasa de filtración glomerular.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El aclaramiento renal mide la capacidad de riñón para eliminar moléculas del plasma y
excretadas en la orina.
DEFINICION: Aclaramiento renal de CIX: volumen de plasma completamente limpiado de la
substancia X por unidad de tiempo.
- Si la substancia se filtra y se reabsorbe: CIX < TFG (lo que se ha filtrado en algún sitio se
ha reabsorbido)
- Si la substancia se filtra y se secreta: CIX > TFG (si se excreta en algún punto esa
substancia se ha añadido más)
9. OTROS TIPOS DE ACLARAMIENTOS
ACLARAMIENTO DE INULINA:
- Es un polisacárido de fructosa (5200 pm) que no se une a proteínas plasmáticas, está
disuelta en plasma. No la produce el organismo y se filtra libremente. No es
catabolizada por células tubulares, es decir no sufre ningún proceso metabólico a lo
largo del paso de los túbulos por lo que metemos es que sale, dicho de otra manera,
recogemos en orina el 100% de lo que metemos
ACLARAMIENTO DE GLUCOSA
- Un 100% de glucosa se absorbe por lo que las personas normales no tienen glucosa en
orina a diferencia de las personas diabéticas que tienen alto contenido de glucosa en
orina
ACLARAMIENTO DE PENICILINA
- La penicilina tanto se reabsorbe como se secreta, por ello al realizar su función en el
organismo se secreta por orina.
TEMA 3: NEFROPATÍAS GLOMERULARES
NEFROPATÍAS GLOMERULARES. GLOMERULOPATÍAS. GLOMERULONEFRITIS: patologías renales cuyo
mecanismo fisiopatológico se centra en el glomérulo.
GLOMERULONEFRITIS PRIMARIAS: el factor causante está en el glomérulo renal, la causa está
en el riñón. Dentro de las glomerulonefritis primarias se encuentran las glomerulopatías
nefríticas y las glomerulopatías nefróticas.
GLOMERULOPATÍAS NEFRÍTICAS: manifestaciones clínicas por inflamación del corpúsculo
renal. Aguda, reducción de la TFG.
Hay diferentes tipos de glomerulonefritis
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TIPOS DE GLOMERULONEFRITIS:
• Según la distribución de los glomérulos afectados: pueden ser DIFUSAS que afecta a la
mayor parte de glomérulos o FOCALES cuando afecta a un grupo limitado de
glomérulos.
• Según la extensión de la lesión glomerular: pueden ser GENERALIZADAS todo el
glomérulo o SEGMENTARIAS sólo una parte del glomérulo.
• Según el tipo de lesión: de cambios mínimos o proliferativos: endoteliales
(intracapilar), epiteliales (extracapilar, semilunas), mesangiales.
GLOMERULONEFRITIS PRIMARIAS:
MECANISMOS Y CAUSAS:
- Por inmunocomplejos formados in situ. Algunas partes de la membrana se
transforman en antígenos, o porque se hayan fijado algunos antígenos externos.
- Por inmunocomplejos formados en la circulación sanguínea, formando un tapón.
- Una agresión inmunológica de tipo celular, ya sea por antígenos exógenos (bacterias,
virus) o por antígenos endógenos (ADN nativo, autoAg, MBQ, tumorales)
CONSECUENCIAS:
- Reducción de la velocidad de Filtración Glomerular, porque cuando los capilares están
obstruidos la presión hidrostática capilar (PHC) disminuye y en algunos casos forman
esclerosis ( se establece un tejido fibroso que produce que no se puedan estirar los
tejidos)
o Reducción PHC: oclusión capilar, esclerosis
o Reducción Kf: disminuye la superficie filtrante
- Aumento permeabilidad Membrana Basal Glomerular (MBG) a proteínas y otros
compuestos (hay algunos poros que se hacen más grandes)
- Incremento de la reabsorción tubular de agua y sodio
MANIFESTACIONES
- Oliguria (poca orina) o anuria (no hay orina) Esto se produce porque al producirse la
reabsorción de sodio y agua (consecuencia) se va a producir la ausencia de orina.
- Proteinuria, la presión oncótica en los capilares es menor.
- Hematuria (GR en sangre(
- Leucocitaria
- Cilindruria (cilindros: restos de membrana de células que estallan)
- Azotemia (mayor contenido de compuestos nitrogenados)
- Hipertensión arterial, aumenta el volumen de sangre
- Edema, la presión en los capilares es menor, y sale más liquido de los capilares al
espacio intestinal. Esto provoca los edemas.
EXPLORACIÓN MICROSCÓPICA
- Lesión glomerular aparente
- Proliferación de la membrana
- Infiltraciones de leucocitos, macrófagos
ALTERACIONES FUNCIONALES
- Aclaramiento de Creatinina disminuido: FG
- Excreción fraccional de sodio baja: aumento reabsorción agua
Dos ejemplos:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
♥ GLOMERULONEFRITIS AGUDA POSTINFECCIOSA (GNAP)
Deposito en la cara epitelial de la membrana basal de inmunocomplejos
Ag: bacterianos: streptococo, neumococos, estafilococos
Víricos: sarampión, hepatitis B, parotiditis, varicela
Parásitos: treponema, toxoplasma, rickettsia
Ac: IgG
MECANISMO: el depósito provoca activación del complemento, polimorfonucleares, fibrina,
vasoactivas proteinoliticas.
FISIOPATOLOGÍA: comienzo brusco (oliguria, hematuria, proteinuria), de 1-2 semanas después
de la infección. Si hay un buen pronóstico la curación es espontánea
♥ GLOMERULONEFRITIS DE PROGESIÓN RÁPIDA (GNPR)
Conduce rápidamente a una insuficiencia renal terminal. Si hay un mal pronóstico de la
enfermedad no hay curación espontánea.
GNPR extracelular o proliferativa: proliferación epitelial, al microscopio se ven como
semilunas que tienen que sobrepasar el 50% de afectación glomerular para que pueda llegar a
considerarse.
GNPR intracapilar: aumenta tamaño núcleo células endoteliales y mesangiales.
GLOMERULOPATÍAS NEFRÓTICAS
Más frecuente que el nefrítico. Se produce un aumento de la permeabilidad de la membrana
filtrante a las proteínas hipoproteinemia (los niveles de proteínas en sangre son muy bajos,
es la característica principal)
MECANISMOS Y CAUSAS
- Alteración de la permeabilidad: barreras mecánicas, eléctricas o ambas
- Acumulación de sustancias en glomérulo (diabetes, amiloidosis) Amiloidosis: proteína
amiloide se deposita en el glomérulo, el Alzheimer es una acumulación de esta
proteína en la neurona.
- Alteraciones estructurales: primarias o secundarias (infecciones, fármacos, tumores)
CONSECUENCIAS
- Provoca hiperproducción de proteínas por los hepatocitos
- Edemas por hipoalbuminemia
MANIFESTACIONES
- Proteinuria, para que sea considerada tiene que ser > 3,5 g/día
Por aumento del tamaño de los poros: nefropatía diabética (no selectiva)
Por pérdida de la barrera eléctrica: GN cambios mínimos (selectiva)
- Hipoproteinemia y disproteinemia (la dispersión de proteínas en sangre también está
alterada, es decir la relación de proteínas con la sangre son diferentes a las demás)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Edema intenso: por disminución de la P.O. plasma
- Hiperlipemia como señal de los hepatocitos es que hay menos cantidad de
proteínas y produce un aumento en la síntesis de lípidos (hipercolesterolemia) e
hiperlipiduria
- Otras:
o Trombosis renal: factores coagulación, viscosidad de la sangre
o Infecciones: pérdida urinarias de IgG
o Osteomalacia: vitD (por la pérdida de proteína que transporta la vitD)
o Anemia ferropénica: eritropoyetina y transferrina
Dos ejemplos de síndromes nefróticos son:
♥ NEFROPATÍA DE CAMBIOS MÍNIMOS
Proteinurias importantes con histología renal normal (cambios mínimos). No se encuentran
depósitos de Inmunocomplejos en el glomérulo. Afecta a niños (2-6 años). Supone un 80% de
síndromes nefróticos.
♥ GLOMERULONEFRITIS EXTRAMEMBRANOSA
Deposito de IgG en la cara epitelial de la membrana basal glomerular. Afecta a adultos
mayores de 30 años, supone solo un 30% de insuficiencia renal.
Inmunocomplejos circulantes:
Ag oligovalente bajo pm: endógeno o exógeno (virus, bacterias)
Ac (IgG) baja afinidad
Por causas desconocidas o infecciones, sistemáticas, neoplásicas, hereditarios benigna, buen
pronóstico.
GLOMERULONEFRITIS SECUNDARIAS A ENFERMEDAD SISTEMÁTICAS
♥ NEFROPATÍA DIABÉTICA
Diabetes mellitus
Microalbuminemia en estado precoz
Proteinuria intensa 15-20 años
Evolución rápida a insuficiencia renal terminal
♥ GOTA
El ácido úrico se acumula en las articulaciones >7mg/dl. También se pueden acumular en el
glomérulo
En ausencia de alfa-globulina y albúmina
♥ LUPUS ERITEMATOSO
Enfermedad autoinmune frecuentes
Hiperactividad linfocitos B
Disminución linfocitos T supresores: provoca proliferación de Ac contra núcleo,
lisosomas, mitocondrias. Proliferan complejos en riñón
Factores genéticos, edad, raza
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
♥ PÚRPURA ANAFILACTOIDE
Erupción cutánea purpúrica
Inmune
Hematuria, síndrome nefrítico y/o nefrótico, insuficiencia renal
TEMA 4: FORMACIÓN DE LA ORINA II. PROCESAMIENTO TUBULAR DEL FILTRADO
GLOMERULAR
1. REABSORCIÓN Y SECRECIÓN DE SUSTANCIAS ORGÁNICAS
A) Azucares
GLUCOSA
Los niveles de glucosa en condiciones normales es de 80mg/100mL para estos valores
normales la tasa de filtración glomerular es de 100 mg/min. Esta glucosa se filtra en el túbulo
contorneado proximal (la mayor parte de ella). Se reabsorbe por el sistema de trasporte activo
secundario dependiente de sodio por gradiente a través de la Na-K-ATPasa en la membrana
basal. (Explicación: en la membrana basal está la bomba ATPasa Na/K, la glucosa entra gracias al
gradiente y el transporte secundario va aprovechando del primario)
Transporte máximo (Tm): Este sistema de captación no es ilimitado dependiendo todo lo que
se filtra se capta. Es decir el transporte máximo es la capacidad que tiene el transporte de
captar una determinada sustancias. El umbral está en 200mg/100mL, para hombres 375mg/mL
y en mujeres 300mg/mL
- D-glucosa (solo captan al isómero D)
- Estequiometrías sodio-glucosa
o Baja afinidad y alta velocidad (1 Na: 1 glu)
o Alta afinidad y baja velocidad (2 Na: 1 glu)
- Transportador proteica
- Metabolizada
- Devuelta a la circulación
MEMBRANA BASAL gradiente de concentración
TRANSPORTE MÁXIMO (Tm)
La glucosa y los aminoácidos filtrados son normalmente reabsorbidos por los túbulos
renales.
- En el túbulo proximal la reabsorción ocurre por transporte activo secundario utilizando
cotransportadores con sodio.
o Los transportadores presentan:
Capacidad de saturación
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Tm. Las moléculas transportadas necesitan saturar su transportador
para alcanzar su transporte máximo.
Umbral renal de transporte.
- Concentración plasmática mínima de una substancia que da lugar a su aparición en la
orina
o Umbral renal para glucosa = 180-200 mg/100Ml
Llega un momento en el que
se satura por lo que por mas
glucosa que se filtre ya no se
va a recaptar más el nivel de
umbral a partir de ese nivel
el exceso de glucosa se va a
eliminar en orina.
La línea roja de puntos indica
la capacidad de glomérulo
para filtrar la glucosa. Toda
la glucosa se filtra hasta un
cierto límite, es decir hasta una concentración de 300mg/100mL a partir de ahí no se absorbe.
Esa glucosa que no se filtra empieza aparecer en orina. En condiciones normales los niveles de
glucosa en plasma son entre 100-200mg/100mL toda la glucosa que se filtra se reabsorbe.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Solo captan al isómero D-glucosa. En la primera
parte del túbulo contorneado es un sistema de
baja afinidad y alta velocidad, con una
estequiometria de 1Na:1Glu. Sin embargo
conforme avanzamos por el túbulo es decir ya en
la 2º parte, el sistema de captación es de alta
afinidad y de baja velocidad y en este caso la
estequiometria es de 2Na:1Glu. Es un sistema
saturable.
Una vez que está la glucosa en el interior de la
célula, como las células requieren mucha energía, esta glucosa se va a metabolizar y producir
ATP, también otra parte de ella vuelven a la circulación por lo que en la membrana basal va
haber un gradiente de concentración desde el interior de las células capilares hacia los
capilares sanguíneos.
LACTATO
También en el túbulo contorneado proximal, con un transporte activo secundario dependiente
de sodio. Tiene un umbral más bajo de 60mg/mL. También se utiliza como sustrato de energía
en el citoplasma y sintetiza glucosa que vuelve a la circulación.
B) Sustancias proteicas
PROTEINAS
Enzimas: ribonucleasa, lisozima
Inmunoproteinas: inmunoglobulinas, beta microglobulina
Hormonas peptídicas: insulina, crecimiento, paratiroidea
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Túbulo contorneado proximal
- Muchas de ellas son hidrolizadas por una serie de enzimas llamadas peptidasas
produciendo la micropinocitosis
- Ó no hidrolizadas, es decir sin hidrólisis produciendo vesículas endociticas
- Hay también una serie de receptores de proteínas que las engloban por un proceso
llamada endocitosis (se rompe la vesícula y sale al exterior)
- Vesículas catabolizadas por lisosomas incorporadas al pool devueltas a la
circulación.
PEPTIDOS
También en el túbulo contorneado proximal. Presentan en la membrana luminal una enzima
específica llamada Dipeptidil peptidasa IV la cual pasa de péptidos a dipeptidos. En el caso del
túbulo contorneado superior hay pocos dipeptidos y tripeptidos porque en esa primera parte
hay poca cantidad de dicha enzima, pero
conforme avanzamos por el túbulo hacía abajo ya
hay más cantidad de di y tripeptidos.
Tienen un transporte activo terciario
- Intercambiador Na-H
- Di y tripeptidos-H
AMINOÁCIDOS
También en el túbulo contorneado proximal con un transporte activo secundario de sodio. En
este caso solo reconocen la estequiometria L de los aminoácidos.
Hay una serie de aminoácidos, para cada grupo de ellos hay un sistema específico de
transporte: cistina/cisteína, aa ácidos, aa básicos, aa neutros, iminoácidos, beta aa
Cuando entran en el citoplasma se pueden utilizar para la síntesis de proteínas, como sustratos
metabólicos ó devueltos a la circulación a la sangre que se utilizará para la síntesis de proteínas
de cada individuo.
C) Otras sustancias nitrogenadas
CREATININA
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Secretada túbulo proximal por transporte activo
UREA
Participa en la osmolaridad específica del riñón, la cantidad de urea que se excreta es mínima.
Se filtra fácilmente y lo que queda hay una parte que se filtra entre el espacio que hay entre
las nefronas y de ahí al asa de Henle otra vez
- Reabsorbe en el túbulo colector proceso pasivo (agua)
- Penetra en nefrona por segmento descendente y ascendente del asa de Henle a favor
de gradiente
ÁCIDO ÚRICO
- Metabolismo final bases púricas
- Túbulo contorneado proximal
- Secretado al espacio tubular
- Reabsorbido en el túbulo colector
D) Sustancias lipídicas
ÁCIDOS GRASOS, CUERPOS CETÓNICOS
Se eliminan por el hígado. El más importante de ellos es el TAUROCOLATO, en el túbulo
contorneado proximal y lleva a cabo un transporte activo secundario dependiente de sodio
E) Vitaminas Hidrosolubles
Túbulo contorneado proximal, transporte activo secundario dependiente de sodio con una
estequiometria de 2 sodios: 1vitamina. Se disuelve fácilmente en el plasma.
2. BALANCE DE ELECTROLITOS
Los electrolitos son fácilmente filtrados, los riñones regulan la excreción de Na+, K+, H+, Cl-,
HCO3- y PO-4
- Uno de los más importantes es el Na+ plasmático en la regulación del volumen y la
presión sanguínea
- También el K+ es importante para mantener la función adecuada en los músculos
cardiaco y esquelético
o La eliminación urinaria es igual a la ingesta
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
2.1 Reabsorción de Na+
El 90% del sodio filtrado se reabsorbe en el túbulo
proximal. Cuando hay ausencia de aldosterona, el
80% de sodio restante se reabsorbe en el túbulo
distal.
La concentración de sodio en la orina final se controla
en el túbulo colector por la aldosterona. Y cuando la
aldosterona se secreta en cantidades máximas todo el
Na+ se reabsorbe en el túbulo distal y túbulo
contorneado.
2.2 Balance de K+
El mantenimiento de los niveles normales del potasio
es fundamental para la función de los tejidos
excitables. La mayor parte del K+ del cuerpo se
localiza en el LIC (98%) ya que la concentración intracelular de K+ es elevada (>150Mm)
mientras que la extracelular es baja (4,5 Mm) debido a la bomba de sodio.
Un pequeño desplazamiento de K+ hacia el interior o exterior de las células produce grandes
cambios en la concentración extracelular de K+
La ingestión de K+ en la dieta es muy variable, por lo que el riñón debe ajustar muy bien su
eliminación.
2.3 Manejo renal de K+
El 90% K+ filtrado se reabsorbe en el túbulo proximal. La secreción ocurre en el túbulo
contorneado.
- La cantidad de potasio secretado va a depender de la cantidad de sodio que llega
- Cantidad de aldosterona
o Si hay niveles altos de aldosterona se reabsorbe mucho sodio, la luz tubular
por lo tanto se hace con cargas negativas y eso produce que salga mucho
potasio es decir que se excrete
o En el caso de que no hay aldosterona no se
secreta potasio.
o Cuando hay altos niveles de angiotensina II
(recordamos que actuaba en el
mecanismo de regulación de la presión
arterial) en el riñón estimula la liberación
de aldosterona y por lo tanto se secreta
potasio
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
o Concentración de potasio alta, Concentración de sodio baja o alta angiotensina
II estimula la secreción de aldosterona.
2.4 Reabsorción y secreción de electrolitos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 5: FORMACIÓN DE LA ORINA III. PROCESAMIENTO TUBULAR DEL AGUA.
MICCIÓN
1. BALANCE DE AGUA EN EL
ORGANISMO
El balance de agua en el organismo
generalmente están equilibrados los
niveles de entrada/salida de agua. La
entrada se produce durante las comidas
y bebidas, tiene una entrada
aproximadamente 2,2L/día más la
producida por el metabolismo que serían
2,5L/día. La salida se produce por la
orina, las heces… (También es de
2,5L/día por lo que se mantiene el
equilibrio)
La osmolaridad de la orina baja mucho
cuando bebemos mucha agua pero en el
caso de la sangre no se va a licuar. El
flujo de orina es muy grande hasta que se elimina todo el agua
2. GRADIENTE DE CONCENTRACIÓN
Hay un gradiente mayor desde la corteza hasta la médula, en las nefronas yuxtaglomerular
(tienen el glomérulo en la separación entre la corteza y la medula y el asa de Henle es más
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
profundo) Conforme va avanzando se hace muy concentrada y cuando asciende por el asa de
Henle.
La formación de orina concentrada exige la existencia de un gradiente de concentración
osmótica entre la corteza (isoosmótica) y la médula y papila (hiperosmótica, 4 veces la
osmolaridad plasmática) por acumulación en esta última de grandes cantidades de ClNa y urea
A lo largo de la nefrona lo que se filtra se reabsorbe casi todo el Na+, K+ y el agua, conforme
baja por el asa de Henle (permeable al agua pero casi no hay electrolitos) se va aumentando la
concentración, y cuando sube por el asa ascendente (permeable al agua y también hay
electrolitos) por lo que se produce la salida de electrolitos, se produce una disolución y cuando
entran en el túbulo colector dependiendo de los niveles osmóticos habrá una orina más o
menos concentrada, que va a depender de la hormona antidiurética que va hacer que se
reabsorba agua o no.
Este gradiente se crea y se mantiene por mecanismo de contracorriente puesto que en el
túbulo ascendente es permeable al agua y en el túbulo descendente es no permeable. Un
mecanismo de contracorriente es aquel que aumenta y disminuye, explicado en la vida diaria
por un sistema de intercambio.
En la fase 1 no ha ocurrido nada pero sabemos que hay 300mOsm en todo el entorno del asa
de Henle, la ascendente es impermeable al agua por lo que salen electrolitos y aumenta la
concentración, en el tercer paso hay intercambio de agua que sale hasta equilibrar la
concentración conforme pasa por el asa 1.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
3. MECANISMO DE CONTRACORRIENTE
Resulta del hecho de que la estructura de los túbulos permite la interacción entre segmentos
ascendentes y descendentes. Está formado por un multiplicador de contracorriente que
forma el gradiente (requiere transporte activo) y un intercambiador de contracorriente que lo
mantiene (no requiere transporte activo)
4. MULTIPLICADOR DE CONTRACORRIENTE
Multiplica la concentración de solutos en el fluido
intersticial medular y en el asa descendente.
Aprovecha el flujo en direcciones opuestas y la
cercanía de ambas ramas.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
5. RECICLADO DE UREA
Contribuye a la osmolaridad total del fluido
intersticial medular. El asa ascendente de
Henle y el túbulo colector terminal son
permeables a la urea. La urea difunde al
exterior del túbulo colector (acompañando al
agua). La urea se recicla y ayuda al gradiente
de concentración.
6. INTERCAMBIADOR-VASOS RECTOS
Aquí los vasos rectos son los intercambiadores de
contracorriente. Entra la sangre en los vasos rectos
con una concentración de 300mOsm/L cuando
asciende cada vez está más concentrada y cuando sale
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
va saliendo los solutos y entrando el agua 350mOsm/L.
Recicla NaCl y urea en la médula (flechas negras) y evita que abandonen la médula. Transporta
agua desde el fluido intersticial y evita que llegue a la médula de forma que no diluya el exceso
de solutos
Amarillo (asa de Henle) las flechas van en el sentido ( ) y vasas rectos (rojo) las flechas van
()
El agua que sale del asa de Henle va hacia los vasos rectos (permeable) y cuando asciende
(impermeable) sale al espacio intersticial y penetra en la sangre por lo que la sangre va
teniendo una mayor concentración y como consecuencia de ese aumento de la osmolaridad de
la sangre aumenta su concentración y la circulación es más lenta que favorece así los sistemas
de intercambio.
7. EFECTO DE ADH
Todo se regula por una hormona liberada en el hipotálamo. Hay unos osmoreceptores que
regulan la osmolaridad de la sangre (ej.: cuando se producen quemaduras) todo estos estimula
la liberación de la hormona antidiurética en la parte posterior de la hipófisis a nivel del túbulo
colector que ayuda a la absorción o liberación de agua. Si no hay ADH no se abren los canales
de agua y la osmolaridad de los túbulos colectores es la misma de la que sale por la orina.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La vasopresina (ADH) pasa a los túbulos donde se une a los receptores de membrana y activa
así al 2ºmensajera cAMP que activa a unas células llamadas acuaporina que activan a la
vesícula que se unen a la membrana apical abriéndose unos poros por lo que entra agua y es
ahí donde se reabsorbe la ADH.
8. LIBERACIÓN DE ADH
El mecanismo fundamental que regula la liberación de ADH es la osmolaridad del plasama. La
osmolaridad la detectan unas neuronas en el hipotálamo que actúan como osmoreceptores, y
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
que activan la secreción de ADH. Existe una relación directa entre osmolaridad plasmática y
ADH.
También se libera ADH cuando disminuye la presión arterial o el volumen sanguíneo que
produce la estimulación del hipotálamo, estimula la hipófisis se libera la ADH lo que provoca
un aumento de absorción de agua, esto está mediado por los receptores de distensión
auriculares y por los baroreceptores del seno aórtico y el arco carotídeo. Parte de la
señalización es directa y parte se hace a través de angiotensina II.
EL SISTEMA URINARIO
1. FISIOLOGÍA DE LA MICCIÓN
La micción es un mecanismo complejo y muy bien regulado tanto por el sistema nervioso
autónomo como por el sistema nervioso voluntario, ya que ha de tener en cuenta no solo el
volumen de orina acumulado sino las condiciones necesarias para poder llevar a cabo la
micción.
2. REFLEJO DE MICCIÓN
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El acto de orinar viene coordinado por el reflejo de micción:
- Se inicia por receptores de
distensión en la pared
- Requiere el acoplamiento del
reflejo de micción (contracción del
músculo detrusor) con la relajación
esfínter uretral externo.
En las paredes de la vejiga hay unos
receptores sensibles a la micción. Cuando la
vejiga está vacía no hay ningún estímulo, conforme se va llenando la vejiga se va estimulando
los receptores sensoriales que produce un arco reflejo en los músculos de la vejiga,
contracción del esfínter interno, cuando se va llenando un poco más cada vez aumentan un
poco más las contracciones y el arco reflejo por los nervios pélvicos va adaptando el volumen
de la vejiga a la presión.
En la segunda fase la distención (el llenado ya lo percibimos como incomodidad, dolor…) ya es
muy grande.
En la médula hay un estímulo de los nervios pélvicos para la contracción del músculo liso que
envían unas señales motoneuronas inhibitorias hasta el esfínter externo, para que se relaje y
salga la orina. Desde el puente o desde la corteza cerebral mandamos señales por los nervios
pudendos para que se contraiga. Lo que ocurre son dos fuerzas opuestas.
Si la cosa se pone grave se puede dar lugar a la contracción muscular elevador de ano y así se
controla mejor el esfínter.
• Estiramiento progresivo estímulo de terminales sensoriales del cuerpo visceral
nervios pélvicos S2-S3 estímulo aferente parasimpático nervios pélvicos
contracción: contracciones de micción
• Sistema autoregenerativo: se va potenciando cada vez más aumentan las
contracciones de micción
• Si no hay relajación del esfínter externo (control motor central) y no se supera la
capacidad contráctil de éste fatiga muscular y fatiga del reflejo inhibición de las
contracciones de micción (minutos – horas) tono basal
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
• Si sigue aumentando el llenado contracciones de micción más fuertes y sostenidas
presión intravesical supera resistencia del cuello vesical
• Se envía señales al SNC que son percibidas como llenado vesical, incomodidad, dolor..
• Comienza segunda parte del reflejo de micción
REFLEJO DE MICCIÓN. SEGUNDA PARTE
• Distensión del cuello activación de receptores sacro nervios pudendos
inhibición del esfínter externo
• Al mismo tiempo desde el encéfalo señales voluntarias contracción del esfínter
externo
• Balance activación/inhibición micción o no
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
3. CONTROL ENCEFÁLICO DE LA MICCIÓN
• Mantiene inhibido el reflejo de micción excepto en el momento de orinar.
• Impide la micción, incluso cuando se ha activado la segunda parte del reflejo ya
que mantiene contracción activa del esfínter externo.
• Induce la micción facilitando los centros sacros e inhibiendo el esfínter externo.
4. MICCIÓN VOLUNTARIA
• Se puede inducir la micción voluntaria incluso sin llegar a la segunda parte del
reflejo de micción
• Contracción voluntaria de las paredes abdominales aumento de presión
intravesical contracción refleja aumento de presión distensión del cuello
activación del esfínter externo + inhibición central del esfínter externo
micción
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 6: NEFROPATÍAS TUBULARES
NEFROPATÍAS TUBULARES
Trastornos poco frecuentes, hereditarios o adquiridos. Alternan funciones de reabsorción o
secreción (pérdidas o retenciones anormales)
SÍNDROMES TUBULARES PROXIMALES
Glucosuria renal: hay perdida de glucosa en orina pero secreta glucosa incluso cuando los
niveles de esta son normales (normoglucemia) porque hay una mutación en cotrasportador
sodio-fosfato 2, es hereditaria. Presenta los mismos síntomas que una persona diabética:
deshidratación, poliuria, polidipsia (sed)
Fosfaturia renal: mutación en el cotransportador sodio-fosfato2 en TCP, se pierde fosfato por
orina (hipofosfatemia). La consecuencia de la pérdida de fosfato por orina estimula la vitD y
hace que se absorba Ca y fosfato con lo cual el fosfato equilibra los niveles por el Ca aumenta
provocando: hipercalciuria.
Aminoacidurias: anomalías específicas o generalizadas. Pueden ser de origen renal que afecta
el proceso de reabsorción activa de aminoácidos o de origen prerrenal que aumenta la
producción metabólica.
Síndrome de Fanconi: disfunción generalizada del túbulo colector proximal, afecta a todas las
sustancias reabsorbidas (aa, glucosa, fosfato, bicarbonato, etc…) , es esporádica y puede ser
por:
- Errores congénitos: cistinosis, glucogenosis, galactosemia, tirosemia
- Intoxicación por metales pesados: Hg, Pb, Cd
Produce la implantación del síndrome nefrótico.
Acidosis tubular proximal: es un fallo en la reabsorción del bicarbonato, el TCD no absorbe y
pasa a la orina. Provoca la secreción de potasio (hipopotasemia). Se produce por tres
mutaciones:
- Cotransportador Na-HCO3
- Transportador Na/H
- Anhidrasa carbónica
SÍNDROMES TUBULARES DEL ASA DE HENLE
Alterada absorción conjunta de Na, Cl y K en rama ascendente. Llega más Na al TD que es
reabsorbido por K. Hipopotasemia e hipernatriuria.
SÍNDROMES TUBULARES DISTALES
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Alteración en el cotransportador Na-Cl. Llega más sodio y agua al TC se produce una
disminución del volumen sanguíneo que estimula a la secreción de angiotensina (estimula
SRAA) y alcalosis hipotasémica.
SÍNDROME DELT ÚBULO COLECTOR
Acidosis tubular distal: incapacidad para eliminar protones a la orina, no se acidifica la orina y
el pH está siempre > 5,5. Como consecuencia hay un defecto en el contratansportador Cl-HCO3
y bomba H-ATPasa
Seudo-hipo-aldosteronismo: aldosterona normal pero menos absorción de sodio y menos
perdida de potasio, lo que produce pérdida renal de Na, estimula SRAA, hiperpotasemia y
acidosis
Seudo-hiper-aldosteronismo: excesiva absorción Na y aumento pérdida K, aldosterona
disminuida. Expansión de volumen, hipertensión, inhibición SRAA, hipopotasemia alcalosis.
Diabetes insípida renal: tiene todos los síntomas de la diabetes mellitus pero sin glucosa. No
concentra orina con ADH normal o alta. Defecto del receptor de ADH y se producen
alteraciones hereditarias de acuoporina.
NEFROPATÍA INTERSTICIAL
Inflamación del intersticio medular o sistema tubular. Asociada a lesión tubular y de los vasos
renales.
MECANISMO Y CAUSAS
Aguda: brusca en corto periodo de tiempo. Hipersensibilidad a fármacos (muchos
fármacos producen lesiones renales)
Crónica: más a largo plazo
Factores físicos y ambientales: radiaciones
Trastornos inmunológicos hay una reacción anticuerpos con antígenos
tubulares
Tóxicos exógenos (analgésicos) o endógenos (ácido úrico)
Neoplasias: aparición de tumores dentro del riñón
Infecciones bacterianas (pielonefritis)
Metabólicos: hipercalcemia e hiperuricemia.
CONSECUENCIAS
Trastorno de la reabsorción de Na
Alteración de la acidificación
Alteración respuesta a ADH
Incapacidad concentrar-diluir orina
MANIFESTACIONES
Poliuria (pérdida de más agua por lo tanto polidpsia más sed)
Proteinuria
Leucocituria, hematuria, y cilindruria
Polidipsia
Depleción de Na
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Acidosis metabólica: H por HCO3
NEFROPATÍAS TÓXICAS
Alteraciones causadas por productos químicos o biológicos directamente o a través de
metabolitos inhalados, ingeridos, inyectados, absorbidos o producidos por el organismo.
MECANISMO
Consecuencia de la citotoxicidad sobre las poblaciones celulares del riñón.
Actúan sobre:
Flujo sanguíneo renal: tetraciclinas, antiinflamatorios, ciclosporina A
Glomérulo: hipersensibilidad (sulfamidas), glomerulonefritis (oro)
TCP: síndrome de Fanconi, Hg, Pb, Cd, tetraciclinas caducadas
TCD: necrosis tubular, anfotericina B
TC: diabetes insípida (Li, metoxiflurano), obstrucción (cristales urato) intersticio
medular
TOXICIDAD POR FÁRMACOS
Antibióticos: aminoglicósidos, cefalosporinas, penicilina, sulfamidas
Analgésicos y antiinflamatorios: salicilatos, paracetamol
Antiinflamatorios no esteroides: indometacina, fenilbutazona
Antineoplásicos: cisplatino
Otros: ciclosporina (inmunosupresor), captopril (hipotensor)
NEFROPATÍAS DE ORIGEN VASCULAR
Por oclusión o estenosis de la vasculatura renal extrínseca o intrínseca. Arterioesclerosis,
trombosis, embolias
Trastornos por obstrucción crónica de las arterias renales:
- Lesiones ateromatosas hipertensión vasculorrenal
- Bilateral hipertensión grave y refractaria
Trastornos tromboembólicos de los vasos extrarrenales:
Arterias renales:
Traumatismos, estenosis, aneurisma, inflamatorios (sífilis)
Infarto renal
Dolor lumbar, hematuria, proteinuria, leucocitosis, necrosis (LDH, GOT)
Venas renales:
Tromboflebitis de vena cava
Traumatismos o lesiones
Glomerulopatías
Proteinuria, escasa hematuria
Enfermedades vasculares de la microcirculación:
Hipertensión arterial
Envejecimiento
LITIASIS RENAL
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Formación de cálculos en las vías urinarias, puede ser de origen
- Endógeno: genéticos o metabólicos (cistinuria, uricosuria, hiperparatiroidismo)
- Exógeno: dieta, aguas duras, infecciones
Cálculos por sobresaturación de solutos:
Concentración
Actividad iónica
pH urinario
Hidratación corporal
Hábitos dietéticos
Oxocálcicas: países occidentales
Úricas: mediterráneos
Infecciosas: mujeres
Dolores espasmódico muy intenso 15-30 minutos. Naúseas y vómitos. Cólico nefrítico.
ALTERACIONES DE LA MICCIÓN
- Vejiga no refleja: se altera el arco reflejo de la micción
- Vejiga paralítica sensitiva: lesión fibras sensitivas. No hay reflejo, rebosamiento. No
hay deseo o necesidad de orinar
- Vejiga paralítica motora: lesión fibras motoras. Rebosamiento. Si se siente deseo de
orinar
- Vejiga autónoma: afectado centro sacro o fibras sensitivas y motoras. Contracción
vesical débil y descoordinada: rebosamiento. Ausencia deseo de orinar
- Vejiga refleja: arco reflejo intacto. Alterada conexión SNC
- Vejiga automática: lesión vías conexión medula y corteza, aferente y eferente. No hay
deseo ni control (reprimir o provocar), el reflejo automático. La vejiga se vacía de
forma activa
- Vejiga desinhibida: lesión fibras descendentes. Hay deseo de orinar pero incapacidad
de reprimir.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 7: INSUFICIENCIA RENAL
La insuficiencia renal hace referencia a un fracaso renal, ya sea brusco o gradual, donde las
funciones renales son deprimidas o anuladas
INSUFICENCIA RENAL AGUDA (IRA o FRA): deterioro brusco de la función excretora renal
por reducción de la TFG. Se produce: azotemia aguda (uremia) aumento en sangre de urea y
creatinina, olugira no obligatoria, sobrecarga circulatoria aumento de colemia
insuficiencia cardiovascular, edema pulmonar..
INSUFICIENCIA RENAL AGUDA PRERENAL:
Hipoperfusión renal caída en la TFG
Hipotensión arterial o insuficiencia cardiovascular: cae GC
Hipovolemia: hemorragias agudas: quirúrgicas, traumáticas, digestivas
Depleción del LEC: vómitos, diarrea, quemaduras
Estados edematosos: hipoalbuminemia
Mecanismo compensador: barorreceptores, SRAA, SNV simpático, retención agua
Riñón: relajan AA, prostangladinas vasodilatadores y ON, angII
INSUFICIENCIA RENAL AGUDA O PAREQUIMATOSA:
Lesiones intrínsecas en parénquima renal o sus vasos sanguíneos. No es reversible de forma
inmediata. Está asociada a las siguientes patologías:
Vascular (trombosis), glomerular (GN agudas)
Tubulointersticial (pielonefritis, obstrucción, rechazo)
Necrosis tubular aguda:
Isquemia renal
Hipoperfusión renal isquemia células túbulos proximales
Mayores necesidades de oxigeno
Permite fugas de solutos filtrados
Células se descaman
Agentes nefrotóxicos: función reabsortiva
Naturaleza tóxico, concentración, duración, susceptibilidad
INSUFICIENCIA RENAL AGUDA POSTRENAL:
Dificultad de eliminar al exterior la orina:
Uréteres: obstrucción intrínseca (litiasis), extrínseca (tumores)
Vejiga: hipertrofia, carcinoma, disfunción neurógena
Uretra: traumático
INSUFICIENCIA RENAL CRÓNICA (IRC): deterioro persistente (+3 meses) de TFG y del
aclaramiento de solutos. Sustitución progresiva del tejido parenquimatosos renal por tejido
conjuntivo.
CAUSAS:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Agresión difusa y generalizada del parénquima: isquemia, nefrotoxicidad,
inmunológica
- Lesiones focales: inflamaciones, infiltraciones tumorales
- Glomerulonefritis
- Enfermedades tubulointersticiales y vasculares
- Pielonefritis
- Nefropatía diabética
FISIOPATOLOGÍA Y MANIFESTACIONES
- Reducción del número de nefronas
- Hipertrofia compensadora
- Cuando la TFG < 20-25% síndrome urémico
o Aumenta uremia y uricemia
o Hipertensión arterial
o Anemia
o No concentra orina poliuria y nicturia
o Acidosis metabólica
o Aumento volemia
SÍNDROME URÉMICO: Estadio final de la IRC
CAUSAS:
Destrucción del parénquima
Retención de sustancias tóxicas
MANIFESTACIONES
Del balance hidroelectrolítico: hipernatremia, hipercalemia
Del metabolismo de glúcidos, lípidos y proteínas
Cardiovasculares: hipertensión arterial
Gastrointestinales: anorexia, hemorragias, estomatitis, gingivitis
Neurológicas: demencia
Hematológicas: anemia
Respiratorias: edema, pleuritis
Endocrinas: insulina, glucagón, GH, PTH, aldosterona, gastrina
Dermatológicas: piel seca
TEMA 8:FISIOLOGÍA Y FISIOPATOLOGIA DEL EQUILIBRIO ÁCIDO-BASE
EQUILIBRIO ÁCIDO-BASE
Nuestro metabolismo está continuamente produciendo ácido (H+) viene básicamente de la
respiración celular.
Ácido: molécula capaz de liberar H+ (dador de protones)
Base: molécula capaz de aceptar H+ (receptor de protones)
También ácido láctico etc… (No volátiles porque no podemos expulsarlos por respiración) Por
lo que necesitamos unos buenos sistemas para mantener el Ph. <6,9 o > 7,8 incompatible
con la vida.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Existen 3 mecanismos para regular el pH:
1. Los sistemas tampón o amortiguadores de la sangre
2. La actividad del sistema respiratorio, que elimina el ácido volátil
3. La actividad del sistema renal, que excreta los ácidos no volátiles.
SISTEMA TAMPÓN DE LA SANGRE Y LOS FLUIDOS
Primera línea de defensa frente a variaciones del pH. Son tres:
1. Sistema tampón ácido carbónico-bicarbonato. La concentración plasmática de CO2,
ácido carbónico y bicarbonato están en equilibrio según ésta ecuación. Pka = 6,1. El
más importante ya que podemos regular la concentración de HCO3 y de CO2
CO2 + H2O
H2CO3
HCO-3 + H+
Según la ecuación de Henderson-Hasselbach:
pH = pka + log [HCO-3] / [CO2]
2. Sistema tampón fosfato, formado por H2PO4- y HPO42-
H2PO4-
HPO42- + H+
No muy importante en el líquido extracelular, pero sí es importante en el líquido
intracelular. pKa=6.8
3. Sistema tampón de las proteínas. A ph fisiológico la mayoría de las proteínas se
encuentran en forma aniónica, lo que permite aceptar protones. Aceptor de H+ que se
producen en el metabolismo mantienen el pH. Las proteínas son muy distintas por
lo que hay un gran intervalo de pka. Tiene importancia sobre todo a nivel intracelular.
PAPEL DEL PULMÓN EN EL EQUILIBIO ÁCIDO-BASE
Segunda línea de defensa frente a cambios del pH. Elimina el ácido volátil.
El PULMÓN: permite eliminar el CO2. Los quimiorreceptores responden a aumento de la
presión CO2 o aumento de la concentración de H+ o disminuye el pH(centrales)
El centro respiratorio es sensible a variaciones de Pco2 y pH sanguíneo:
Puede tardar incluso horas en regular el pH, y no puede eliminar los ácidos no volátiles.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El RIÑÓN: permite de manera efectiva los ácidos volátiles en la orina. (pH de la orina suele ser
ácido)
Los H+ se producen en las células de los túbulos de las nefronas por hidratación del CO2
(anhidrosa carbónica) H2CO3 HCO-3 vuelve a la sangre y los protones van a la orina.
Los protones salen por:
- La mayoría de las células tubulares se intercambian por Na+ (transporte activo 2º). La E
se debe al gradiente de Na+/K+ de la otra membrana.
- En el túbulo distal y túbulos colectores, transporte activo 1º, elimina H+ fuera de las
células muy en contra de gradiente de concentración. pH mínimo de la orina aprox 4,5.
Estamos recuperando bicarbonato por lo que evitamos su pérdida en orina. En la luz tubular,
los protones reaccionan con el HCO3- que se ve filtrado en el glomérulo (se unen por la
anidrasa carbónica del borde en cepillo de las células tubulares) CO2 que vuelve a la célula.
H+ con fosfatos filtrado hidrógeno fosfato
H+ con amoniaco NH4+ (principal forma de eliminar ácidos no volátiles)
Tarda varios días, pero es lo más eficaz.
ALTERACIONES DEL EQUILIBRIO
Normalmente se determinan 2 de ellos y la otra se calcula
- Sí disminuye el pH acidosis
- Si aumenta el pH alcalosis
Cada una:
- Sí se debe a un problema respiratorio (PCo2) : respiratoria
- Si se debe a una modificación [HCO-3]: metabólica
Acidosis respiratoria: pCO2 aumenta (hipercapnia). Suele ser un problema crónico (no
supone síntomas, salvo que pCO2 suba mucho, pues afectaría al SNC). Bronquitis
crónica y enfisema (EPOC): ligera acidosis sin síntomas. La compensación nunca va a
poder ser respiratoria; será renal y por tampón.
Acidosis metabólica: disminuye la concentración de [HCO3-] El pulmón intenta
compensarlo produciéndose hiperventilación. Depresión del SNC. Al disminuir
aumenta el potasio produciéndose también hiperpotasemia.
Aumenta el ácido por lo que consume mucho HCO-3 (disminuye HCO-3)
(superproducción de ácido)
Alcalosis respiratoria: aumento de pH por disminución de pCO2 en plasma
(hipocapnia). Si es aguda hiperexcitación del SN
Alcalosis metabólica: aumenta el ph a la vez que aumenta la concentración de [HCO-3]
TEMA 9: INTRODUCCIÓN A LA ENDOCRINOLOGÍA
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Concepto de HORMONA: producidas por células especializadas (células endocrinas) aisladas o
formando glándulas (glándulas endocrinas, carentes de conductos). Son secretadas a los
fluidos corporales (sangre, linfa, líquido intersticial) que generalmente a bajas
concentraciones llevan su mensaje químico a células diana con receptores específicos para
unirse a la hormona y activar una respuesta.
MECANISMO DE COMUNICACIÓN INTERCELULAR: a través de las jap junctions por
comunicación por contacto directo mediado por conexinas que forman canales intercelulares
para el paso de mensajeros intracelulares.
MECANISMO DE COMUNICACIÓN INTERCELULAR: UTILIZACIÓN DE MENSAJEROS QUÍMICOS
- Hormonas Autocrinas
- Hormonas Paracrinas
- Hormonas Endocrinas
o Hormonas Neuroendocrinas: sintetizada por hormas
o Citoquinas
Interleucinas (linfocinas)
Adipocinas (leptina)
- Neurotransmisores (Sinapsis)
Diferencias del sistema endocrino comparado con el sistema nervioso:
1. Mayor lentitud de la respuesta
2. Mayor duración de la respuesta
PAPEL FISIOLÓGICO DE LAS HORMONAS
Crecimiento y desarrollo:
- Crecimiento y proliferación celular (GH, insulina, IGFs, PDGF, EGF, NGF)
- Maduración del SNC (Tiroideas)
- Muda, metamorfosis, pigmentación (Tiroxina, glucocorticoides, melatonina)
Reproducción:
- Gametogénesis (FSH, LH, esteroides)
- Dimorfismo sexual (Andrógenos, estrógenos, progesterona)
- Conducta (oxitocina)
Producción, utilización y almacenamiento de energía:
- Glucogenogénesis, glucogenolisis, movilización de ácidos grasos, etc. (insulina,
glucagón, glucocorticoides, adrenalina)
Mantenimiento de la constancia de medio interno:
- Líquidos corporales y su contenido electrolítico (ADH, aldosterona)
- Presión sanguínea y frecuencia cardíaca (Tiroideas)
- Equilibrio ácido-base (Aldosterona)
- Temperatura corporal (Tiroideas)
- Masa ósea, muscular y adiposa (calcitonina, PTH, GH, testosterona)
Acción Motora (catecolaminas, acetil-colina, oxitocina)
CLASIFICACIÓN QUÍMICA DE LAS HORMONAS
- Péptidos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Glicoroteínas
- Esteroides
- Derivados de aminoácidos
- Otros (prostaglandinas, NO, Adenosina, etc)
PRECURSORES DE HORMONAS PEPTÍDICAS
• Pro-hormonas: es un producto químico de cadena más larga que se corta para generar
la hormona
• Pre-pro-hormona: es una molécula más grande precursora de la prohormona
• Pre-hormona: la molécula secretada por las glándulas endocrinas que es inactiva hasta
que se transforma en hormonas por las células diana.
SÍNTESIS DE HORMONAS PEPTÍDICAS
1. Unión del ribosoma al codón inicial AUG
2. Síntesis del péptido señal (PS)
3. Unión a la nucleoproteína citosólica PRS (Partícula de Reconocimiento de la Señal)
4. Unión de la PRS a su receptor en el retículo endoplasmatico rugoso.
5. Unión de GTP
6. Hidrólisis de GTP
7. Liberación de la PRS y apertura del poro del receptor
8. Internalización de la proteína naciente en el retículo endoplasmático rugoso.
9. Corte por enzimas del REr similares a la tripsina
10. PRE-hormona = PS –PRO-hormona
11. Maduración de la PRO-hormona a una única hormona madura o a varias formas
activas
12. Paso al Aparato de Golgi
13. Modificaciones del péptido antes de su secreción (glicosilación)
14. Empaquetamiento y almacenamiento.
HORMONAS ESTEROIDES
Los esteroides son lípidos sintetizados a partir del colesterol son lipofilicos.
Síntesis:
los esteroides se sintetizan a partir de colesterol exógeno o sintetizado de novo.
Intervienen en reacciones de:
1. Modificación de anillo A (instauración…
2. Modificación del anillo B (saturación)
3. Acortamiento de la cadena lateral
4. Grupos OH o ceto en diferentes posiciones
Intervienen enzimas localizadas en:
1. Citosol
2. REI
3. Mitocondrias
Secreción:
No se almacenan
Su liberación se produce por difusión
La secreción es proporcional a la tasa de síntesis
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
HORMONAS CATECOLAMINAS
Síntesis:
Las catecolaminas se sintetizan en el citoplasma
Se empaquetan en gránulo cuando ya están maduras.
Secreción:
Las reservas existentes son de varios días
Cuando llega la señal adecuada se produce la apertura de canales de Ca2+
La consecuencia es un aumento de los niveles de Ca2+ citosólico
Gracias a la existencia de proteínas contráctiles los gránulos se digieren hacia la
membrana plasmática donde vierten su contenido hacia el exterior celular por
exocitosis.
CONCENTRACIÓN PLASMÁTICA DE LA HORMONA
Pueden encontrarse en sangre de forma libre o unidas de forma reversible a proteínas
plasmáticas mediante:
1. Unión específica (aumenta la afinidad y baja la capacidad)
2. Unión inespecífica (disminuye la afinidad y aumenta la capacidad)
La forma activa es la forma libre, también es la forma degradable.
TRANSPORTE EN SANGRE
Papel de la unión a proteínas plasmáticas:
1. Favorece la solubilización
2. Es una reserva hormonal que no es activa pero tampoco metabolizable
3. Amortiguación de actividad en las variaciones debidas a los pulsos secretores
4. Facilitación de la unión de la hormona a su receptor en la célula diana.
(La globulina transportadora de cortisol –CBG- y la de hormonas sexuales –SHBG- tienen puntos en
unión con la membrana de las células diana y son internalizadas por éstas)
Peptídicas y catecolamianas: generalmente disueltas en el plasma
Esteroides y tiroideas:
Unidas a globulinas específicas (con alta afinidad y baja capacidad)
Unidas de forma inespecífica a la prealbúmina y la albúmina (con baja afinidad y alta
capacidad de unión)
El porcentaje de unión varía entre el 98% para la testosterona y el estradiol hasta sólo
el 50% para aldosterona.
INACTIVACIÓN Y ELIMINACIÓN
Lugar: hígado y riñón (en menor medida)
Mecanismo de inactivación: proteólisis, procesos de fase I (oxidación/reducción) y procesos
de Fase II (conjugación)
Vías de eliminación: Bilis y orina.
REGULACIÓN DE LAS SECRECIONES HORMONALES
Niveles de regulación:
- Síntesis
- Proceso de secreción
- Factores de liberación
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Sistemas de Control de Retroalimentación o Feed-Back
Positiva (glucosa ++ insulina)
Negativa (testosterona -FSH)
Sistemas de control según los elementos
Simples (Calcio + Calcitonina)
Complejos o en cascada (LHRH +FSH +testosterona -FSH, -LHRH)
Factores reguladores:
- Nerviosos
- Humorales
- Ambientales (físicos y químicos)
Biorritmos:
- Horas: GH, Prolactina
- Días: Cortisol
- Semanas: hormonas ováricas durante el ciclo ovárico
- Meses: variaciones estacionales de las hormonas tiroideas
- Años: variaciones asociadas a las etapas de la vida
MECANISMOS DE ACCIÓN HORMONAL
Etapas:
1) Reconocimiento
2) Activación Celular
Receptores hormonales: elementos celulares capaces de reconocer específicamente a una
molécula reguladora y desencadenar una acción específica, que reúne las siguientes
propiedades:
1. Alta afinidad de unión (acción a baja concentración 10-6 a 10-12 M)
2. Número limitado de lugares de unión, es decir, unión saturable
3. Unión rápida y reversible
4. Acción biológica proporcional a la magnitud de la unión
Tipos de receptores:
a) Intracelulares
b) De membrana
Mecanismo de acción:
DE HORMONAS CON RECEPTORES INTRACELULARES
1. Entrada por difusión pasiva a través de la membrana
2. Unión a receptores citosólicos
3. Activación del receptor
4. Traslocación hacia el núcleo
5. Activación de síntesis de proteínas de respuesta rápida o primaria
6. Síntesis de proteínas de respuesta secundaria
DE HORMONAS CON RECEPTORES DE MEMBRANA
1. Receptores con actividad tirosina kinasa
2. Receptores acoplados a proteínas G (GPCR, G-protein coupled receptors)
3. Existencia de segundos mensajeros
SEGUNDOS MENSAJEROS
El sistema AMPc-Proteína kinasa A (PKA)
El calcio (LEC= > 10-3 mientras que en el LIC= < 10-7)
Mecanismos reductores del calcio citosólico:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Extrusión, almacenamiento (retículo sarcoplasmico, calciosomas),
tamponamiento en mitocondrias.
Acciones: activación de enzimas, activación de proteínas contráctiles, activación de
proteína kinasa C (PKC) unión a calmodulina.
Fosfolípidos de membrana:
PIP2 IP3 + DAG
IP3 Ca2+
DAG +PKC
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 10: INTEGRACIÓN NEUROENDOCRINA. FISIOPATOLOGÍA DE LA
NEUROHIPÓFISIS
El hipotálamo son un conjunto de núcleos que se conectan con la hipófisis por el tallo…
Estimuladores de la liberación:
- LHRH /GnRH: hormona liberadora de LH u hormona liberadora de gonadotropinas
- GHRH: Hormona liberadora de GH u hormona de crecimiento
- TRH: hormona liberadora de la hormona estimulante del tiroides.
- PRH: hormona liberadora de la prolactina
- CRH: hormona liberadora de la hormona corticoestimulante.
Inhibidores de la liberación:
- GHIH o SS: hormona inhibidora de la secreción de GH o Somatostatina
- PIH / PIF: Hormona / factor inhibidora de la liberación de prolactina = dopamina
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
EL SISTEMA HIPOTALÁMOHIPOFISARIO
Hipófisis posterior = neurohipófisis; hipófisis anterior = adenohipófisis
Un hecho único en el SNC es la ausencia en el hipotálamo de la barrera hematoencefálica (hay
capilares fenestrados que permiten el paso de hormonas hipopsiotrópicas en la sangre)
- HIPOTÁLAMO: acceso de sustancias a las neuronas sensoras ( neuronas secretoras de
hormonas hipofisiotrópicas)
- PLEXO CAPILAR PRIMARIO (eminencia media): acceso de hormonas circulatorias a las
neuronas (las neuronas liberan péptidos). En cuanto a sus funciones:
o Aporte de oxigeno y nutrientes
o Recogida de desechos
o Recogida de hormonas hipopsiotrópicas.
- VASOS PORTALES LARGOS: liberación a la sangre de péptidos hipotalámicos.
- PLEXO CAPILAR SECUNDARIO (adenohipófisis): En cuanto a sus funciones:
o Aporte de oxígeno y nutrientes
o Recogida de desechos
o Liberación de hormonas hipopsiotrópicas (dan la señal)
NEUROPÉPTIDOS HIPOTALÁMICOS
Neuropéptidos: controlan la función del adenohipófisis.
El hipotálamo libera (RH) una hormona, llega a la hipófisis y la estimula para que produzca TSH,
llega al tiroide y inhibe el hipotálamo.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La neurohipófisis está conectada por estímulos nerviosos (núcleo supraóptico y
paraventricular)
Las neuronas magnocelulares son muy grandes y mandan el tallo hasta llegar al plexo
hipofisario, no están mielinizadas liberan oxitocina y ADH.
HORMONA ANTIDIURETICA (ADH) Y OXITOCINA: en primer lugar decir que son muy parecidas
y son nonapéptidos.
Se originan en los núcleos hipotalámicos supraóptico y paraventricular:
Núcleo supraóptico: ADH/oxitocina (6:1)
Núcleo paraventricular: Oxitocina / ADH (6:1)
Estructura: Pm=1,200, tanto del ADH como Oxitocina:
9 aminoácidos (solo se diferencian en 2 aminoácidos)
5 de ellos forman un anillo por la existencia de un puente de disulfuro entre los
aa 1 y 6
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Ambas proceden de una hormona común primitiva aún existente en peces y anfibios la
VASOTOCINA. Este nonapéptido se diferencia en el aminoácido 3 de la ADH y en el aminoácido
8 de la Oxitocina.
Se sintetiza unidas a unos péptidos mayores (10 kDa) o neurofisinas que se secretan junto a las
hormonas (neurofisinas I sirven como proteína de unión)
La función de las neurofisinas es favorecer el transporte axonal de las hormonas.
Catabolismo: son degradadas en el hígado y en el riñón. Vida media corta (5-10 min)
Transporte y secreción de ADH y oxitocina junto a sus neurofisinas:
1. 40% en línea de disparo
2. 60% en reservorios
hormonales intracelulares
o cuerpos de Herring
3. El transporte axonal de los
gránulos de secreción
desde los núcleos
hipotalámicos hasta la
neurohipófisis dura = 2
horas.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
FISIOLOGÍA Y FISIOPATOLOGÍA DE LA OXITOCINA
Acciones sobre la glándula mamaria:
1. Se libera la neurofisina I y se une a los
receptores en las células mioepiteliales
2. Se produce un incremento del calcio
intracelular
3. Estimula la contracción de las células
mioepiteliales que favorece la eyección de la
leche
4. El efecto es inhibido por la adrenalina por
vasoconstricción que impide la llegada de
oxitocina al tejido glandular
5. Además la adrenalina inhibe la liberación de
oxitocina por la neurohipófisis
6. Las emociones intensas, la ansiedad o el dolor
agudo mantenido pueden interferir con una
lactancia normal por descender los niveles de
oxitocina y antagonizar su efecto.
La adrenalina inhibe la secreción y no deja que la oxitocina llegue a las glándulas
mamarias.
Acciones sobre el útero:
1. Inhibe la Ca2+-ATPasa dependiente de Mg2+ que se encarga
de expulsar Ca2+ fuera de la célula, además de aumentar la
permeabilidad para el Ca2+ extracelular.
2. Contrae la musculatura lisa del útero durante el parto.
3. Incrementa la síntesis de prostaglandinas F2a que pueden
colaborar en los procesos de contracción
4. Los niveles aumentan durante la gestación. No participa en
el desencadenamiento del parto sino en su desarrollo.
5. Su acción sobre el útero depende parcialmente de los
niveles de estrógenos y progesterona.
a) Los estrógenos aumentan la
efectividad de la oxitocina al aumentar sus
receptores en el endometrio.
b) La progesterona ejerce una acción
opuesta.
CONTROL DE LA SECRECCIÓN DE OXITOCINA
Estimulan:
1. Arcos reflejos, neuroendocrinos desencadenados por la estimulación táctil de las
mamas, útero o genitales externos.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
2. También pueden activar la secreción de oxitocina los estímulos olorosos o sonoros
procedentes de las crías
3. Los estrógenos
4. La acetil-colina estimula la liberación de oxitocina mientras que los antagonistas
nicotínicos bloquean la liberación
Inhiben:
1. Los reflejos de estimulación son abolidos por el estrés, que provoca una caída de los
niveles de oxitocina. La adrenalina activa receptores β-adrenérgicos para inhibir la
secreción de oxitocina
2. Los péptidos opioides
3. La progesterona
ADH: HORMONA ANTIDIURÉTICA
EFECTOS DE LA ADH
Sobre el sistema cardiovascular (receptores V1):
Tiene efecto vasopresor (vasopresina) lo que reduce el volumen del lecho vascular y
compensa de forma rápida la falta de fluido hasta que éste se compense debido a su
acción renal ADH más lenta.
Tras hemorragia o deshidratación se disparan los niveles de ADH.
No todos los vasos son igualmente sensibles a la ADH, lo que supone que se produce
un reajuste del flujo sanguíneo además de la vasoconstricción.
Tiene acción sinérgica con la adrenalina, de manera que pequeñas cantidad de ADH
potencian considerablemente el efecto vasopresor de la adrenalina.
Sobre el riñón (Receptores V2 = reduce la filtración glomerular):
Activa la reabsorción tubular (túbulos colectores) de agua
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La unión de la ADH al receptor aumenta la actividad de un adenilato ciclasa que a su
vez activa una proteína kinasa que fosforila canales de membrana para el agua (APQ2)
aumentando la permeabilidad de ésta al agua.
También activa el bombeo de sodio en el asa de Henle y disminuye la velocidad del
flujo sanguíneo en la médula renal.
Ambos fenómenos contribuyen a mantener la elevada osmolaridad en el intersticio
renal necesario para la reabsorción de agua.
Sobre el hígado (Receptores V1 = contribuye a que le llegue sangre enriquecida al cerebro):
Activa la glucogenolisis
Aumenta la liberación de glucosa desde el hígado
Sobre el hipotálamo / adenohipófisis (Receptores V3 = favorece que el individuo se quede
con el agua)
Estimula la secreción de CRH y ACTH, respectivamente.
CONTROL DE LA SECRECIÓN DE ADH
Estimulan:
Deshidratación, sobrecarga salina, ejercicio, hemorragias
Aumenta de osmolaridad (actúa sobre el SNC). Un cambio de osmolaridad plasmática
de tan solo 1% es suficiente para multiplicar la secreción de ADHH
Disminución del volumen (actúa sobre receptores de la cavidad torácica)
Angiotensina: la angiotensina II estimula la liberación de ADH.
Temperatura: las temperaturas altas y los procesos febriles la activan
Inhiben:
Sobrecargas acuosas, alcohol. Se orina mucho y sufrimos deshidratación (neuronas)
Temperatura: la baja temperatura inhibe la liberación de ADH, mientras que las altas
temperaturas ambientales y los procesos febriles la activan.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
SECRECIÓN INAPROPIADA DE ADH:
Causas de niveles anormalmente elevados de ADH
Trastorno neurológico central (lesión hipotalámicas)
Trastornos neurológicos periféricos
o Pseudosindrome de Scwartz-Bartter (debido a alteraciones neurológicas que
acompañan al mixedema, las porfirias, etc.
o Polineuropatía del síndrome de Guillain-Barré
Fuente ectópicas (Síndrome Scwartz-Bartter por carcinoma brocogénico)
Consecuencias
Baja diuresis y elevada retención de líquido. Hipervolemia + hipoosmolaridad
Hipervolemia estimulación de la eliminación de Na hiponatremia (poco Na+ en
sangre)
Hiponatremia hiperhidratación celular y alteraciones electrolíticas (las células se
llenan de agua)
Las neuronas son especialmente sensibles cefaleas, náuseas, vómitos, confusión,
convulsiones, coma.
HIPERNATREMIA NEUROGENA (ESENCIAL)
- La respuesta de los túbulos colectores renales a la ADH es normal
- La secreción de ADH en respuesta a estímulos volumétricos es normal.
- Existe una alteración en los receptores del núcleo supraóptico y paraventricular que
determina una secreción de ADH:
o Correcta en respuesta a estímulos volumétricos
o Incorrecta en respuesta a estímulos osmóticos
- Aparece elevación a los niveles plasmáticos de sodio SIN hipovolemia
- Hipodipsia (ausencia o deficiencia de sed apropiada) (beben poco)
Niveles normales y patológicos de Na+
< 150 mM: no existen alteraciones
160-170 Mm: debilidad, fiebre, hipersensibilidad muscular y calambres, que evoluciona hacia
un cuadro de fatiga y ataxia, e incluso mioglobinuria (debido a la hipopotasemia consecuencia
y lesión muscular) Puede aparecer disfunción mental como letargia, anorexia, depresión e
irritabilidad.
>180 mM: pacientes confusos o estuporosos, pudiendo llegar al coma e incluso a la muerte.
DIABETES INSIPIDA
Frecuencia: 1-2/10.000
Aparecen entre los 15 y los 30 años
Más frecuente en hombres
EXPLORACIÓN:
Prueba de la sed: la orina normal debe ser concentrada y escasa tras la restricción de la
ingesta de agua.
Determinación de niveles de ADH por RIA tras inyección de suero hipertónico
Respuesta de ADH exógena: menor cantidad de orina con menor concentración.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TIPOS DE DIABETES INSIPIDA
NEFROGÉNICA: se produce falta de sensibilidad tubular a la ADH por deficiencia
tubular (tubulopatía) adquirida o heredada.
NEUROGÉNICA: existe una deficiencia de secreción de ADH
1. Lesión de los núcleos supraóptico y paraventricular
a. 50-60% tumores
b. 20-30% inflamaciones
c. 10-20% traumatismos, isquemias
2. Lesión en la neurohipófisis
Puede no presentar manifestaciones si se debe a lesión hipofisaria pero el muñón
asume la función de liberar hormonas.
Destacar que no todas las lesiones de la neurohipófisis lleva a una lesión diabetes
insípida.
VALORES NORMALES:
Poliuria >3000 ml/día
Diuresis normal 500-1800 ml/día
Oliguria <400-600 ml/día
Anuria < 100 ml/día
Manifestaciones de la Diabetes Insípida Neurogénica:
1. Poliuria. Normalmente 5-10 litros día, puede llegar a 43 l/día
2. Hipovolemia junto a hipernatremia (mucho sodio) e hipoosmolaridad
3. Polidipsia compensadora.
4. Otras secreciones están disminuidas (saliva, sudor)
5. Riesgo grave de deshidratación, aunque no suelen aparecer alteraciones circulatorias
6. Existen niveles discordantes de alta osmolaridad y baja concentración de ADH
7. Prueba de la ADH positiva. En caso contrario es una tubulopatía
8. Pruebas de la sed y de la administración de suero salino hipertónico negativo
9. Pueden aparecer alteraciones de la visión si se deben a lesiones estructurales que
también afectan al quiasma óptico
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
MELATONINA(secretada por la glándula pineal, la glándula pineal está formada por
células grandes protectoras por las células de la glía de soporte)
NAT (N-acetil transferasa) enzima que se regula, es decir si se expresa mucho NAT se produce
mucha melatonina, llega al hígado y hay una inactivación se produce una oxidación de Fase I y
una conjugación de Fase II y luego el riñón acaba eliminando por orina.
La síntesis de melatonina se
sintetiza en diferentes sitios pero el
sito más importante es la glándula
pineal. La retina capta la luz, manda
inhibición el núcleo supraóptico y
activa el paraventricular que activa
al ganglio cervical superior. Se
produce la liberación de
Noradrenalina que aumenta la
expresión y actividad de la NAT por
lo que se libera más melatonina.
Cuando hay oscuridad el sistema
está activo y cuando hay luz
disminuye la secreción.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La luz azul activa unas células que tienen melonopsina (no llevan información de imágenes) va
a los núcleos, luego a la médula…. Libera Noradrenalina que activa el receptor β-adrenérgico,
se genera AMPc que activa una proteína kinasa A aumentando así la expresión de NAT y
aumentando los niveles de calcio y activan la NAT.
FACTORES QUE MODULAN LA SECRECIÓN DE LA MELATONINA
1. Ciclo de luminosidad ambiental
2. Cambios estacionales en la duración del día y la noche
3. Edad (baja capacidad)
4. Estímulos aversivos (estímulos peligrosos)
5. Hormonas. Es inhibida por los esteroides ováricos.
ACCIONES BIOLÓGICAS DE LA MELATONINA
1. SEÑANILAZIÓN TEMPORAL: medición de la duración de la noche mediante la
secreción de una señal química circulante (melatonina), con diferentes consecuencias
dependiendo de la especie.
2. REGULACIÓN DE RITMOS CIRCADIANOS: sincronización y acoplamiento de los
diferentes osciladores o marcapasos endógenos, adaptando el sistema circadiano del
individuo a las variaciones ambientales
3. SINCRONIZACIÓN MATERNA DE LOS RELOJES BIOLÓGICOS DEL FETO
4. REPRODUCCIÓN ESTACIONAL: adecuación de la actividad del sistema reproductor a
las condiciones ambientales y control del momento de maduración gonadal,
especialmente en las especial con fertilidad estacional
5. OTRAS POSIBLES ACCIONES DE LA MELATONINA:
a. Inmunomodulador
b. Antioxidante
c. Antienvejecimiento
d. Oncostático
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 11: FISIOLOGÍA Y FISIOPATOLOGÍA DE LA ADENOHIPÓFISIS
HORMONAS ADENHOHIPOFISARIAS
6 Hormonas peptídicas (que se acumulan en vesículas de secreción). Clasificación:
Clasificación según su forma de acción:
• Acción directa: PRL (prolactina)
• Acción directa y control de la secreción de hormonas (sobre tejidos diana como el
hígado y sobre otra hormona): GH (Hormona de crecimiento)
• Hormonas reguladoras de glándulas endocrinas (sobre tejido diana para que se secrete
otra hormona): ACTH (Hormona adrenocorticotropa o Corticotropina), TSH (hormona
estimulante de tiroides o Tirotropina)
Gonadotropinas: FSH (hormona estimulante de los folículos) y LH (hormona
luteinizante)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
PRODUCCIÓN DE HORMONAS POR LAS CÉLULAS DE LA ADENOHIPÓFISIS
Estructuralmente existen 3 familias de hormonas adenohipofisarias:
1. Proteínas formadas por una cadena única: GH y Prolactina
2. Péptidos pequeños sintetizados a partir de pro-opiomelanocortina (POMC)
un péptido de gran tamaño: ACTH, MSH (hormona estimulante de
melanocitos) y LPH (lipotropina)
3. Formadas por dos cadenas α y β. La cadena alfa es común para todas ellas y
está en exceso en la adenohipofisis, mientras que la cadena beta es propia
para cada hormona: TSH, FSH y LH
PROLACTINA. Cadena polipeptídica única de 198 aa.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
SECRECIÓN DE PROLACTINA: por células eosinófilas de la adenohipofisis que se denominan
mamotropas o lactotropas (aprox 20% variable 10-40% de las células adenohipofisarias) Se
sintetiza en forma de prohormona (preprolactina) de gran tamaño que se escinde para dar
lugar a cuatro variantes moleculares de prolactina.
CONTROL DE LA SECRECIÓN DE PROLACTINA
Inhibidora
Activadora 2 señales.
Prolactina estimula PIH que a su vez inhibe la prolactina.
Secreción pulsátil de diferentes cantidades
PROLACTINA EN PLASMA:
- La secreción es pulsátil y varía durante la vida
- Siendo mayor en la infancia y la vejez que en la edad adulta basal
- Está muy aumentada durante el embarazo y la lactancia
Valores normales determinados por radio-inmuno-ensayo (RIA):
• Hombres: 2 a 18 ng/ml
• Mujeres que NO están
embarazadas: 2 a 29 ng/ml
• Mujeres embarazadas: 10 a
209 ng/ml
EFECTOS DE LA PROLACTINA:
1. SOBRE LAS MAMAS
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El receptor TK (tirosina – kinasa): puede ser con actividad intrínseca y sin actividad intrínseca.
Cooperación de la prolactina y la oxitocina para la producción
de leche: la neurohipófisis libera oxitocina. El efecto sorbente
estimula la liberación de oxitocina. Mientras siga lactando por
vía nerviosa se estimula el HPT y este activa la prolactina y a la
neurohipófisis para que vacié la leche
2. SOBRE LA SECRECION DE GONODOTROFINAS
a. Inhibe la secreción de GnRH por el hipotálamo
gonadotrofinas
b. Reduce la secreción de gonadotrofinas
hipofisarias
c. Niveles elevados de prolactina reducen los de
hormonas sexuales
3. SOBRE CONDUCTA SEXUAL:
a. Relacionado con las sensaciones placenteras del orgasmo
b. Existe hiperprolactinemia en la fase refractaria tras el orgasmo
c. Tiene el efecto antagónico a la dopamina implicada en la erección
d. Hiperprolactinemia patológica induce pérdida de líbido e impotencia.
4. SOBRE EL SISTEMA INMUNITARIO:
a. Relación entre prolactina y enfermedad celíaca: hiperprolactinemia durante
las fases activas antes de la corrección de la dieta.
MECANISMO DE ACTIVACIÓN DEL RECEPTOR DE PROLACTINA
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
PRLR: el receptor de prolactina es un receptor transmembrana sin actividad intrínseca. Se
encuentra en hígado, riñón, cerebro, mama, ovarios, útero…. Fosforila al receptor y el R
fosforilado si tiene actividad kinasa.
HIPERFUNCIÓN DE LA PROLACTINA
Hiperprolactinemia = niveles superiores a los normales.
La prolactina generalmente se mide cuando se buscan tumores hipofisarios y la causa de:
- Producción de leche sin relación con un parto (galactorrea)
- Disminución del deseo sexual (libido) en hombres y mujeres
- Impotencia
- Infertilidad
- Períodos menstruales irregulares o ausentes (amenorrea)
Ej: hipotiroidismo, enfermedad renal. Enfermedades que dan mayores niveles son el
hipertiroidismo, enfermedades renales… Antidopaminérgicos ya que la dopamina inhibe la
prolactina por lo que se dispara su secreción.
HIPOFUNCIÓN DE LA PROLACTINA
Hipoprolactinemia: suele asociarse a la necrosis pituitaria del síndrome de Sheehan.
Manifestaciones: incapacidad de producir leche a corto plazo. Causa: hemorragias postparto.
Consecuencias: hipopituitarismo con déficit de TSM, ACTM, LM/PSH, GH y prolactina.
GH. HORMONA DEL CRECIMIENTO. Growth Hormon, hormona somatotropa o
somatropina
Prohormona de 217 aa que se excinde en una proteína de 191 aa. MW 22kDa,
- La
estructura
globular incluye
cuatro hélices
estabilizadas por
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
dos puentes de disulfuro entre ellas, necesarias para la interacción funcional con el
receptor de GH(GHR).
- El gen de la GH pertenece a una familia multigénica:
GH1, CSH-1, CHS1, GH2 Y CSH2.
CSHP es un pseudogen
Brazo largo del cromosoma 17
- Es importante en el crecimiento. No todo el crecimiento depende de la GH (pero si
sobre todo en el feto y en el neonato). No todos los efectos de la GH es sobre el
crecimiento (sigue secretándose y teniendo importancia psicológica cuando ya se ha
detenido el crecimiento)
- Presenta gran homología con la prolactina y el lactógeno placentario
- Su expresión se estimula por hormonas tiroideas.
Existen cuatro Insulina-Like Growth Factors (IGF-1-4 con 70% homología)
El IGF-1 o Somatomedina C es el más importante, es un péptido de 7,6 kDa similar a la insulina
(50% homología) con 70 aa en una sola cadena con tres puentes de disulfuro intramoleculares.
Se produce mayoritaria mayoritariamente en el hígado, pero también en placenta, corazón,
pulmón, riñón, páncreas, bazo, intestino delgado, intestino grueso, testículos, ovarios, cerebro,
hipófisis y médula ósea.
Estimulan la producción de IGF (lleva a cabo todas las acciones indirectas de la GH)
1. GH
Inhiben la producción:
1. Desnutrición
2. Falta de sensibilidad a la GH por defectos en el GHR (los fetos no tienen este receptor
todavía)
3. Defectos en la ruta de señalización post-GHR
El 98% del IGF-1 siempre está unido a una de 6 proteínas fijadoras (IGF-BP). El IGFBP3, es la
más abundante (80% de todas las uniones del IGF). El IGF-1 se une al IGFBP-3 en una
proporción molar 1:1
- El hígado promueve la existencia de glucosa en sangre debida a la GH
- La GH activa de manera inhibitoria sobre el HPT para la GH. Mientras que el HPT
también libera Somatostatina que va a estimular la secreción de GH.
- Los receptores tirosina-kinasa de la GH (GHR) requieren de la unión (sin actividad
intrínseca) e IGF-1 (IGF-1-R) se parece al receptor de insulina, tiene actividad
intrínseca llega la hormona y dimeriza el receptor.
ACCIONES DE LA GH:
Efectos estimulantes del crecimiento: 1. Reduce el consumo de
1. Aumenta la altura en niños y adolescentes glucosa.
2. Estimula el crecimiento de los órganos internos 2. Promueve la
3. Estimula la absorción intestinal de calcio glucogenogénesis.
3. Estimula la secreción
4. Favorece la retención renal de minerales
5. Estimula la mineralización de los huesos de IGF-1
6. Aumenta la masa muscular por hiperplasia sarcómera
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
7. Estimula el sistema inmune.
Incrementa la biosíntesis proteica y el depósito de proteínas:
1. Favorece la captación de aminoácidos
2. Aumenta la traducción de mRNA a proteínas
3. Aumenta la transcripción de DNA a mRNA
4. Inhibe el catabolismo proteico
Estimula la lipolisis y la utilización de grasa como fuente de energía:
1. Moviliza lípidos del tejido adiposo
2. Favorece la conversión de FFA en acetil Co-A
3. Favorece la utilización de acetil CoA como fuente de energía
4. Si se supera la capacidad del hígado para procesar acetilCoa
Conversión de acetoacético cetoacidosis (cuerpos cetónicos)
Acúmulo en hígado de FFA y TG esteatosis hepática
(Almacenes patológicos de grava) esteatosis no alcohólica cirrosis cáncer de
hígado.
Efecto hiperglucemiante (resistencia a la insulina)
1. Reduce el consumo de glucosa por el hígado
2. Disminuye la captación y el consumo de glucosa en el resto de tejidos, sobre todo
músculo y tejido adiposo
3. Se almacena la glucosa en el hígado en forma de glucógeno
4. Cuando se supera la capacidad glucogenogénica, aparece liberación hepática de
glucosa e hiperglucemia
5. Contribuye al mantenimiento y función de los islotes pancreáticos
6. Favorece la liberación de insulina.
• Secreción de GH pulsátil (que
evita la desensibilización y para
que los receptores no se
acumulen9 por células
eosinófilas somatotrofas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
• Con 5-8 picos diferente para cada sexo: (6-14; 13-72 ug/ml) La secreción es mayor
durante el crecimiento:
o 0.5-1 mg/día en niños y adolescentes
o 0.4 mg/día en adulto
• Aumenta durante el sueño profundo y ejercicio intenso.
ESTIMULACIÓN:
1. GHRH (somatocrinina) hipotalámica actúa sobre receptores GHRHR situados en las
células somatotropas adenohipofisarias
2. Sueño (SWS-III y SWS-IV)
3. Hipoglucemia
4. Descenso de FFA en sangre (ácidos grasos libres)
5. Inanición, especialmente con carencia de proteínas
6. Aumento de aa en sangre (arginina)
7. Estrés, traumatismo, excitación (estimulación alfa-adrenérgicos)
8. Ejercicio físico
9. Testosterona y estrógenos
10. Grelina
INHIBICIÓN:
1. Somatostatina
2. Somatomedinas
3. Hiperglucemia
4. Aumento de FFA en sangre (ácidos grasos libres)
5. Envejecimiento
INACTIVACIÓN
1. Hígado
2. Riñón
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
EXPLORACIÓN:
- Circula libre en sangre con una vida media de 20 min, mientras que la vida media de la
IGF-1 es de 20h
- Radioinmunoensayo (RIA) de GH o somatomedinas
- Prueba de estimulación:
o Directa (GHRH)
o Indirecta (hipoglucemia con insulina) Subiría la GH
- Prueba de supresión
o Hiperglucemia con glucosa. Bajaría la GH
HIPOFUNCION EN LA SECRECIÓN O ACCION DE LA GH
Causas:
1. Infarto: necrosis por isquemia
2. Tumor
3. Déficit congénito
4. Trastorno derivado de agresiones específicas a las células implicadas. Células
somatropas
Manifestaciones:
1. Bajos niveles circulantes de GH y/o somatomedinas (salvo en Enanismo de Laron)
2. Hipoglucemia
3. Enanismo armónico a partir del segundo año de vida.
<40% de la talla media
(1,45 cm en hombres y 1,35 en mujeres)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. Gerodermia (piel envejecida)
5. Acromicria (extremidades pequeñas)
6. Esplacnomicria (órganos internos pequeños)
7. Inteligencia normal
8. Trastornos psicológico
TIPOS DE ENANIMOS POR HIPOFUNCIÓN DE LA GH
1. ENANISMO HIPOTALÁMICO: para realizar la prueba inyectaríamos insulina y debería
de aumentar la concentración de GH pero en este caso no aumenta.
a. Lesión hipotalámica
b. Prueba de estimulación por GHRH positiva (la hipófisis si libera GH)
c. Prueba de estimulación indirecta (hipoglucemia) negativa porque el HPT no
responde, no secreta GH
2. ENANISMO HIPOFISARIO
a. Lesión de las células eosinófilas hipofisarias (no liberan GH)
b. Prueba de estimulación por GHRH negativa
3. ENANISMO HEPÁTICO O DE LARON: el eje hormonal está bien.
a. Falta de síntesis hepática o somatomedinas
SÍNDROME DE LARON: es un trastorno hereditario autosómico recesivo que afecta al gen GHR.
Se produce un retraso severo en el crecimiento, obesidad, trastornos del sueño, mandíbulas
pequeñas y frente prominente.
HIPERFUNCIÓN EN LA SECRECIÓN O ACCIÓN DE LA GH
Manifestaciones:
1. Elevadas concentraciones de GH y somatomedinas
2. Hiperglucemia
3. Gigantismo armónico surge en niños y jóvenes
4. Acromegalia surge en adultos
Causas:
1. Tumor funcionante de la hipófisis (adenoma eosinófilo) es un tumor en las células que
excretan GH
2. Secreción ectópica (tumores pancreáticos)
¡! Metaplasia: las células cambian funcionalmente.
ACROMEGALIA: (las zonas distales aumentan tamaño) adenosomas somatotrofos benignos de
crecimiento lento. Se suelen detecta en la 5º década de la vida. Si son grandes pueden causar:
dolores de cabeza, trastornos de visión por presión de los nervios ópticos o deficiencia de otras
hormonas hipofisarias.
El exceso prolongado de GH causa:
1. Aumento de tamaño en manos, pies, maxilar inferior (prognatismo) arcos cigomáticos,
labios, lengua, nariz y orejas, laringe (cambio de voz)
2. Visceromegalía (hígado, corazón, etc)
3. Crecimiento, engrosamiento y endurecimiento de la piel
4. Diastema (separación entre dientes, sobre todo en el maxilar inferior)
5. Sudoración excesiva.
6. Presión sobre nervios ( p.e, síndrome del túnel carpiano)
7. Debilidad muscular
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
8. Exceso de globulina fijadora de hormonas sexuales (SHBG)
9. Reducción de la función sexual
10. Resistencia a la insulina o incluso diabetes mellitus tipo 2.
PANHIPOPITUITARISMO (HIPOFUNCION ADENOHIPOFISARIA GLOBAL) no hay adenohipofisis
Causas:
1. Síndrome de Simmonds-Sheehan por hipertrofia hipofisaria + pérdida de sangre =
necrosis isquémica post-parto
2. Extirpación quirúrgica
3. Tumores
4. Procesos inflamatorios, etc
Gran reserva funcional: no aparecen síntomas hasta que no se ha perdido funcionalmente
>75% de la adenohipofisis
Manifestaciones:
1. Enanismo hipofisario con atrofia muscular y genital
2. Ausencia de bello púbico y axilar
3. Atrofia del pecho. Incapacidad de las mamas para producir leche
4. Decoloración de piel y pezones
5. Insuficiencia tiroidea, suprarrenal y gonadal (amenorrea y perdida de líbido e
impotencia)
6. Anemia
7. Hipotermia e intolerancia al frio
8. Hipofuncionamiento cardiaco
9. Hipoglucemia
10. Aparición de arrugas finas en la piel. Envejecimiento precoz.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
HIPOFUNCIÓN HIPOFISARIA GLOBAL POR LESIÓN HIPOTALÁMICA O HIPOFISARIA: lesión
tanto neuro como adenohipofisis.
TEMA 12: FISIOLOGÍA ÓSEA Y ARTICULAR
DISTRIBUCIÓN DEL CALCIO, DEL FÓSFORO Y DEL MAGNESIO EN EL ORGANISMO
Total corporal En el hueso (%) Extraóseo (%)
2+
Ca 1000-1200 g 98-99 1-2
Pi 600-650 g 80-85 15-20
Mg 22-25 g 60 40
Papel del Ca2+ , del Pi y el Mg2+ en el organismo:
1. Funciones mecánicas (esqueleto). Estructura ósea: cristales de hidroxiapatito: Ca2+ + Pi
y matriz colágena
2. Metabólicas.
CALCIO
Intervención del Ca2+ en procesos fisiológicos:
1. Transmisión nerviosa
2. Contracción muscular
3. Regulación de la permeabilidad de membranas celulares
4. Procesos de secreción
5. Actúa como segundo mensajero en señales hormonales
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
6. Coagulación sanguínea
7. Actúa como regulador de la actividad de enzimas
Hipocalcemia: tetania, alteración cardiaca, crisis epilépticas, laringoespasmo, muerte
Hipercalcemia: calcificación de tejidos blandos, formación de cálculos renales.
NIVELES DE CALCIO: No todo el calcio está de la misma manera. El 1% del Ca2+ es Extraóseo, y
la mayor parte es extracelular. En cuanto a la concentración libre en plasma oscila entre 1.2
mM y en el citosol 0,1 um. Concentrado (1mM) en estructuras intracelulares como
mitocondrias, retículo endoplasmático, calciosomas y vesículas de los fotorreceptores.
Modulación de los niveles de Ca2+ citosólico.
• Control de entrada: activación o inhibición de las Ca2+ -ATPasas, activación o
inhibición del intercambiador 2Na+/Ca2+ y permeabilización (canales de Ca2+
dependientes de voltaje o de ligando)
• Control de liberación desde depósitos intracelulares.
DINÁMICA DEL CALCIO EN EL ORGANISMO
Calcemia normal: 100 mg/L = 2.5 mM
98 mg/L en hombres (2.45 mM)
95 mg/L en mujeres (2.38 mM)
1.4 mM ultrafiltrable (1.2 libre + 0.2
formando complejos) + 1.0 mM no
filtrable unido a proteínas (80% a la
albúmina y 20% a globulinas)El
organismo no tiene acceso a regular
el calcio no filtrable.
Muy importante mantener la calcemia:
- Hipocalcemia: tetania, alteración
cardiaca, crisis epilépticas,
laringoespasmo, muerte.
- Hipercalcemia: calcificación de tejidos blandos, formación de cálculos renales.
Factores controladores:
1. Hormona paratiroidea (PTH). Regulación a corto plazo
2. Vitamina D. Regulación a largo plazo
3. Calcitonina
Órganos diana: hueso, riñón, intestino.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La ingesta de calcio debería de ser en torno a 1g (1000mg) al día, normalmente absorbemos
300mg y los 700 mg que no se absorben, se suman otros 100 (de vesículas, cálculos…) El riñón
filtra 7200 mg y se reabsorbe 7000mg por lo tanto eliminamos 200 mg. En el LEC
aproximadamente hay 900 mg y en el hueso alrededor de 1 kilo (es decir el 90%). Tenemos dos
casos de huesos:
1. En el hueso profundo que forma cristales (hidroxipatita) más lento
2. En el hueso no cristalino o también llamado amorfo hay un intercambio más rápido
(300mg/día)
Balance del calcio:
Absorción intestinal y pérdida por secreción y descamación. La absorción se produce
fundamentalmente en el duodeno. Factores que aumentan la absorción:
o pH intestinal bajo ácido
o Fosfatos orgánicos digeribles
o Vitamina D
o PTH
o GH
Factores que inhiben la absorción:
o Oxalatos
o Fosfatos
o Ácidos grasos no absorbibles
o Cortisol
o pH alcalino
Reabsorción renal: 96% a casi 100% en presencia de PTH
Intercambio de calcio con los tejidos (óseo “mayoría” , muscular, etc)
FÓSFORO INORGÁNICO (Pi)
La mayoría del Pi es óseo (95%). La mayor parte del Pi extraóseo se encuentra en el músculo
esquelético. (15%)
Intervención del Pi en procesos fisiológicos:
1. Forma parte del ADN
2. Nucleótidos energéticos o segundos mensajeros (ATP, AMPc)
3. Fosfolípidos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. Tampón intracelular (en forma de fosfato)
5. Tampón urinario (en forma de fosfato)
Se absorbe de forma pasiva o activa mediada por el CALCITROL fundamentalmente en
el yeyuno
Prácticamente todo el Pi plasmático puede filtrase. Importante esto para regular el
tampón urinario.
Su eliminación renal depende de la reabsorción tubular controlada por el Ph y por la
presencia de hormonas, como la PTH, ésta favorece que se elimine fosfato y así nos
quedamos con Calcio en solución (no se forma fosfato cálcico)
MAGNESIO (Mg)
EL 60% en hueso fácilmente intercambiable con el medio extracelular. La concentración
plasmática de Mg2+ es de 1.8-2 Mm (el 70% se encuentra en forma ultrafiltrable). A diferencia
del Ca2+, estas concentraciones son muy similares a las concentraciones citosólicas.
Intervienen en procesos fisiológicos:
1. Cofactor de aprox 300 reacciones
enzimáticas
2. Mantiene el orden estructural en
ribosomas
3. Mantiene el orden estructural de
membranas
4. Interviene en la trasmisión
nerviosa
5. Contracción muscular
6. Transporte de iones a través de
membrana
7. Control de liberación de PTH
Canal de volkman: canal vacío (arteriolas,
vénulas, venas..) a través de ellos se comunican canales de Havers.
FUNCIONES DEL HUESO
Mecánica: soporte, permite la locomoción y protege a órganos internos (pulmón, corazón,
médula y encéfalo)
Metabólica: homeostasis mineral (Ca2+, P, Mg)
COMPONENTES DEL HUESO
Hueso esponjoso (los que hay en la parte interna) : trabéculas (cavidades con estructuras
vasculares) y médula ósea
Hueso compacto (los que hay en la parte cortical) : OSTEONAS, canales (canales de Havers o
Herversianos – longitudinales-, canales de Volkmann –transversales-) vasos (arteriolas, vénulas
y vasos linfáticos) y ramas nerviosas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Células: células madre o Stem origen de las células ósea y hematopoyéticas, osteoblastos,
monocitos osteoclastos, macrófagos, adipocitos, células endoteliales, mastocitos.
Todo está recubierto por un tejido conectivo y irrigado periostio
¡! Posible pregunta examen. Otras células:
- OSTEOBLASTOS: se encargan de la
construcción es decir de la formación del hueso y su
regulación.
- OSTEOCITOS: mantenimiento y remodelado.
- OSTEOCLASTOS: demolición de hueso =
osteolisis.
Las señales que sale de los osteoblastos regulan todo
el proceso y se convierten en osteocitos
(mantenimiento y remodelado) además están en
contacto con osteoblastos y osteoclastos gracias a las
jap junctions por los canales calcóforos bañados por
un líquido llamado osteoplasma.
Si necesitamos calcio se lo pedimos a los osteocitos y si necesitamos más aún se lo
pedimos a los osteoblastos.
ESTRUCTURA DEL COLÁGENO
Colágeno tipo I = α1 + α1 + α2. Forman fibras gruesas de hasta 100 nm
Se sintetiza por fibroblastos, condroblastos y osteoblastos (¡! En el hueso el colágeno
lo forman los osteoblastos)
Lo encontramos en piel, tendones, cartílago y hueso
Su característica principal es la resistencia al estiramiento
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Importante en el colágeno hay un aminoácido que solo encontramos aquí Hidroxiprolina y
para ello necesitamos de la vitamina D.
Colágeno tipo II = α2 + α2 + α2. Forman fibras finas de 20 nm
Se sintetiza por condroblastos
Lo encontramos el cartílago
Su característica principal es la resistencia a la presión intermitente.
¡! Como hemos dicho más arribas el colágeno en los huesos es formado por los osteoblastos
que lo depositan siguiendo la línea de tensión (líneas de fuerza en la cabeza del fémur) el
sistema detecta estas líneas y deposita donde se necesita colágeno tipo I
EL HUESO POSEE:
1) Sustancia osteoide o matriz orgánica: representa el 35% del peso del hueso, formado
por colágeno de tipo I (90%) y por proteínas (10%): osteonectina, osteocalcina,
osteopontina, trombospondina, fibronectina, sialoproteínas, fosfoproteínas, albúmina,
proteoglicanos.
Función de las proteínas óseas:
En la mineralización:
1. Favorecer o inhibir el depósito de Ca2+, Pi, Mg2+
2. Favorecer o inhibir la maduración de los cristales de hidroxiapatito
3. Acción enzimática
En la reabsorción ósea:
1. Regulación de la actividad de los osteoclastos
2. Acción quimiotáctica
3. Función de reconocimiento
En la estructura de la matriz osteoide
1. Favorecer el anclaje de las células en la matriz
2. Formación de las estructuras de la matriz ósea
Otras:
1. Transporte de iones, hormonas, metales y metabolitos
2. Estimulación e inhibición de enzimas
2) Sustancia inorgánica (resistencia a la compresión)
Representa el 65% del peso seco del hueso
Se compone principalmente de hidroxipatita = fosfato básico de calcio
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
En presencia de pirofosfatos NO se forman cristales de hidroxipatita. El PIROFOSFATO
regula la formación de hidroxipatita ¡!
Cristales de pequeño tamaño (aprox 15x30x300 Ằ) y con gran asimetría tanto
estructural como electrostática, lo que les confiere gran capacidad de fijar en las
superficie del cristal otros iones:
o Mg2+, K+, Na+, Mn2+ y F- así como citratos y carbonatos
o Así como iones no habituales como Pb2+, Zn2+, Cd2+ y otros
o La exposición a elementos radiactivos (uranio, plutonio, etc) hace que se
peguen al hueso de forma duradera irradiación prolongada
osteosarcoma
OSTEOGENESIS Y OSTEOLISIS
OSTEOGENESIS, MOEDELADO Y REMODELADO ÓSEO.
1. Vertido de vesículas en la membrana en cepillo que es la parte más activa, que vierte
vesículas que contienen:
a. Enzimas líticas que digieren el material orgánico
b. Ácido cítrico y láctico que disuelven la materia inorgánica.
2. Fagocitosis de micropartículas de hueso
a. Digestión intracelular
b. Remodelado de componentes
Se puede llevar de varias maneras la formación de hueso:
1. Osificación Primaria o Intramembranosa: directamente a partir del tejido conjuntivo
embrionario
2. Osificación Secundaria o endocondral (dentro del cartílago): a partir de una base
cartilaginosa previa el cartílago es invadido por osteoclastos. La matriz cartilaginosa es
horadada simultáneamente en numerosos puntos, el camino dejado por los
osteoclastos es seguido por los osteoblastos que lo van rellenando con matriz
osteoide.
3. Crecimiento en longitud: en el cartílago de conjunción entre la epífisis y la diáfisis. A
los 20 años se pierde la sensibilidad a la IGP-1 y se produce el cierre de la epífisis.
Modelado continúo durante toda la vida
Unidades de remodelamiento
Osteoclastos osteolisis lagunas de remodelamiento o de Howship osteoblastos
sustancia osteoide mineralización (papel de las fosfatasas alcalinas en la hidrólisis del
pirofosfato que inhibe el depósito de minerales) transformación de osteoblastos en
osteocitos (prisioneros mantenedores de la estructura)
FACTORES QUE CONTROLAN LA DINAMICA DEL REMODELADO OSEA
1. Vascularización (flujo de perfusión ósea = 5% de la sangre)
2. Estímulos Mecánicos (prostaglandinas y colágeno)
3. pH del medio interno
4. Factores hormonales
5. Pirofosfato (inhibidor de la mineralización)
¡! Imp Hormonas principales: PTH, Calcitonina, Calcitrol o 1,2,5-dihidroxi-colecalciferol
Hormonas secundarias: insulina, tiroideas, glucocorticoides, sexuales (estrógenos y
progesterona), GH, Prostaglandina E2, VIP
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Factores de crecimiento: Somatomedinas, PDGF (factor de crecimiento derivado de plaquetas)
, FGF (factor de crecimiento fibroblástico) , EFG (factor de crecimiento epidérmico) , TGF
(factor de crecimiento transformante)
Citoquinas: IL-1, TNF, Interferón-ϒ
La calcitonina actúa cuando hay previsiones de que va hacer mucho calcio. Inhibe la reducción
de calcio del riñón y inhibe la osteolisis rápida de osteocitos y lenta de osteoblastos. Previene
de lisis. Los estrógenos inhiben la osteolisis.
Intervienen riñón, intestino y el
propio hueso. Los osteoclastos
tienen mayor capacidad de
hacer osteolisis.
Es importante la vitamina D para
la absorción intestinal del Calcio.
Si no hay síntesis de proteínas
no podemos hacer
osteogénesis. En la gestación la
progesterona inhibe los
glucocorticoides y favorece la
osteogénesis.
PTH: hormona rápida que previene la Hipocalcemia, activa osteodisis y osteolisis rápida de
osteocitos. Estimula al riñón que active VitD, a la vez que favorece la realizaciones renal de
Ca2+
Glándulas paratiroideas: son
cuatro glándulas situadas en la
parte posterior del tiroides.
ACCIONES DE LA PTH ENCAMINADAS A ELEVAR EL NIVEL DE CALCIO IÓNICO EN EL LEC
Estimula:
1. Movilización de calcio y fosfato del hueso (favorece osteolisis)
2. Reabsorción renal de calcio
3. Excreción renal de fosfato (fosfaturia)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. 1-hidroxilasa renal mayor formación de 1,25(OH)2D3
5. Absorción intestinal de Ca2+ a través de 1,25(OH)2D3
6. Excreción renal de bicarbonato (bicarbonaturia)
7. Reabsorción renal de magnesio
(CaSR) Receptor de Detección de
Calcemia:
1. El Ca2+ inhibe la secreción
de PTH
2. El 1,25(OH)2D3 inhibe la
síntesis de PTH
La calcitonina no es indispensable
para la vida. Es también un péptido
que se inhibe en la célula.
- El CaSR ( R) que cuando hay
Ca2+ activa una
señalización y se inhibe la
liberación de PTH
- PTH activa la síntesis de vit
D. Hay feed back E de
forma que si hay demasiada VitD se inactiva la producción (por la VDR)(en caso de que
haya piercalcemia)
ACCIONES DE LA CALCITONINA:
1. Inhibición de la reabsorción tubular de calcio
2. Inhibe la movilización del calcio óseo
Estabilización del calcio óseo, favorece la eliminación de calcio. Se secreta calcitonina cuando
hay calcio (es el estímulo). Para prevenir los picos de glucemia también se secreta calcitonina.
METABOLISMO DE LA VITAMINA D:
- El feed-back negativo del
25(OH)D3 regula la precisión los
niveles de 25(OH)D3
independientemente del
aporte de vitamina D.
- La vitamina D, pero no es el
25(OH)D3, se almacena bien en
el hígado durante meses.
- El 25(OH)D3 es mil veces menos
activa que el 1,25(OH)2D3
- La activación renal necesita la
PTH. En su ausencia casi no se
forma 1,25(OH)2D3.
El hígado lanza sangre 25-hidroxicolecalciferol y el riñón por PTH lo convierte en 1,25-
dihidroxicolecalciferol (forma activa).
Hay una hidroxilación en 24 y se inactiva la vit.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Transcalciferina: proteína que lleva en sangre a la vitD. Fuente de la mayor parte de
las proteínas plasmáticas.
Activación de la expresión de proteínas trasportadoras de Ca2+ en las células del epitelio
intestinal en respuesta a la vitD
Cuando suben los niveles de Ca2+ en sangre aumenta la calcitonina y baja el PTH. La vitamina
D es importante para la absorbencia de de calcio. Necesario tres proteínas: (se expresan con la
vitD.) :
- Canal de Ca2+ (TRPV6)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Calvindina (proteína de fijación de Calcio) que une calcio del canal y lo lleva al polo
basal.
- Bomba de Ca2+ con consumo de ATP y expulsa el Ca2+ fuera de la célula.
vitD2: ergocalciferol
vitD3: colecalciferol. Es la que el organismo usa más.
TIPOS DE CARTÍLAGO:
- Cartílago Hialino: formado principalmente por fibrillas de colágeno tipo II
- Cartílago Fibroso o fibrocartílago: formados por fibras de colágeno tipo I
- Cartílago Elástico: formado por colágeno tipo II y fibras elásticas.
Propiedades:
1. Elasticidad
2. Lubricación
3. Carente de vasos sanguíneos
Papel fisiológico:
1. Ajustar las superficies óseas en las articulaciones
2. Amortiguar los golpes al usar las articulaciones. Prevenir el desgaste por rozamiento
Células:
1. Condroblastos (forman cartílagos)
2. Condrocitos (cuando se quedan cartílagos)
3. Condroclastos (rompen cartílagos)
LAS ARTICULACIONES: definición: articulación es la
unión entre dos o más huesos, un hueso y cartílago
o un hueso y los dientes.
Tipos de articulaciones (fisiológicas):
1. Diartrosis: mayor amplitud o complejidad
de movimiento. Ej. hombro
2. Anfiartrosis: con movimiento muy
limitado. Ej. Vértebras.
3. Sinartrosis: no móvil. Ej. Huesos del
cráneo.
TEMA 13: FISIOPATOLOGÍA ÓSEA Y ARTICULAR
MÉTODOS DE EXPLORACIÓN
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Morfología y densidad ósea
Radiografía: útil para fracturas y deformaciones, pero debe reducirse al 30% la masa
ósea para que sea detectable una pérdida de densidad ósea.
Densitometría de absorción de fotones
TAC
Dinámica de remodelamiento óseo:
Fosfatasa alcalina: (isoenzima ósea) en plasma osteogénesis
Hidroxiprolina en plasma y orina implica osteolisis ya que se libera al hidrolizarse el
colágeno y no es reutilizado
Biopsia
Punción de la cresta iliaca –hueso de la cadera- da información sobre el número y
relación de células óseas. Si administra con cierta antelación tetraciclina este tiñe
selectivamente el frente de mineralización. Esto puede utilizarse para determinar la
velocidad de avance del proceso.
TRASTORNOS DE LA FORMACIÓN DEL HUESO
Malformaciones durante la ontogenia (ontogenia= desarrollo del individuo desde el momento en el que se
engendra)
Disostosis: osificación anormal del cartílago de conjunción que da lugar a malformaciones de
huesos aislados
Osteocondrodisplasias: malformaciones debidas al crecimiento descoordinado entre el
cartílago y el hueso
Exostosis: crecimiento morboso en un hueso. Se trata de una hipertrofia parcial y circunscrita
a la superficie de un hueso o diente.
OSTEOPOROSIS: Ostopenia o reducción de la masa de tejido óseo presente en la unidad
de volumen de hueso. Existe una pérdida paralela de matriz orgánica osteoide y de sustancia
inorgánica o mineral.
Causas:
Causas que depriman la osteogénesis:
Defecto hereditario: de la síntesis de colágeno tipo I (osteogénesis imperfecta) El
hueso es muy pobre, hay muy poca materia ósea. El tallo genético es variable.
Exceso de cortisol. Síndrome de Cushing o tratamiento con corticoides. El cortisol es
el grupo corticoide mayoritario. El exceso de cortisol produce el Síndrome de Cushing.
o Inhiben la síntesis de proteínas deprimen la acción de los osteoblastos
o Activan la proteólisis activa la acción de los osteoclastos
o Inhiben la absorción intestinal de calcio hipocalcemia estimula la
secreción de PTH (responsable de la lisis ósea)
o Se sacrifica la integridad de la masa ósea para mantener la calcemia.
Subalimentación y malabsorción intestinal
o Escorbuto: enfermedad ligada a la falta de vitamina C. La vitC es indispensable
para la síntesis de Hidroxiprolina necesaria a su vez para la síntesis de
colágeno.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
o Senilidad: disminución de la funcionalidad de los osteoblastos y/o falta de
calcio por disminución de la absorción intestinal ligada a un creciente
insensibilidad a la vitamina D para estimular la síntesis de transportadores
intestinales de calcio (TRPV6, calbindina D, PMCA1b)
Inmovilidad: falta de estímulos mecánicos
Causas que exaltan la osteolisis:
Hipertiroidismo las hormonas tiroideas activan las dos procesos pero más el de
osteolisis, por lo que encontramos osteoporosis de “turnover” alto. ” turnover”
regeneración muy activa del hueso
Alteración del balance de hormonas sexuales. (osteoporosis involutiva) Común en
mujeres postmenopáusicas y personas de edad avanzada (>65 años) de ambos sexos.
Es la osteoporosis más común. Después de los 40 años se pierde 0.5% de la masa ósea
por año y esto aumenta a 1% en mujeres menopáusicas.
Tratamiento con heparina: se ha observado en un % pequeño (5%) de los pacientes
tratados durante más de 6 meses con dosis altas en heparina.
Consecuencias:
1. Dolor difuso y sordo por irritación del periostio
2. Crisis de dolor agudo y bien debido a microfracturas
3. Disminución de la resistencia mecánica fracturas que pueden ser frecuentes o
injustificadas
4. Deformaciones
OSTEOESCLEROSIS: exceso de cantidad de tejido óseo por
unidad de volumen de hueso. Se produce una insuficiencia
funcional de los osteoclastos
Causa: el balance osteolisis-osteogénesis está alterado en sentido
inverso a como lo estaba en la osteoporosis. La causa suele ser
una insuficiencia funcional de los osteoclastos.
La osteopetrosis es la forma de osteoesclerosis difusa más
característica. Se trata de una enfermedad hereditaria en la que
existe un déficit de osteoclastos funcionales. Se corrige mediante un implante de médula ósea
sana.
Consecuencias:
1. Disminución de la resistencia mecánica fracturas
2. Compresión de estructuras nerviosas (ceguera)
3. Anemia más todos los problemas fisiológicos por la pancitopenia.
TRASTORNOS CUALITATIVOS: se caracterizan por un cambio en la composición de la
sustancia ósea, formada por 60% de sustancia mineral, 30% de sustancia inorgánica y 10% de
células.
TIPOS:
1. Raquitismo
2. Osteomalacia
3. Osteitis fibrosa
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. Osteodistrofia renal
RAQUITISMO Y OSTEOMALACIA:
desacoplamiento entre síntesis de sustancia
osteoide y su mineralización. El raquitismo es
el cuadro infantil mientras que la
osteomalacia es la forma adulta de la
enfermedad. El hueso raquítico u
osteomalácico carece del contenido mineral
adecuado por lo que es más blando y
maleable, suelen aparecer curvaturas y es
muy transparente en ratos X.
Mecanismo patogénico:
A) Inhibidores de la mineralización: como exceso de pirofosfato por déficit hereditario
de fosfatasas alcalinas óseas – hipofosfatasia – o acidosis. El pirofosfato es regulado
por la fosfatasa alcalina que es producida por los osteoblastos.
B) Bajas concentraciones plasmáticas de Ca y/o P
Causas:
1) Déficit 1,25-dihidroxi colecalciferol o 1,25-(OH)2D3 el metabolito activo de la vitamina D
que activa la absorción intestinal de Ca y P. Causas que nos llevan al raquitismo:
a. Falta de vitamina D
b. Fallo hepático en la hidroxilación en 25
c. Fallo renal de hidroxilación en 1
d. Exceso de inactivación hepática en 24
2) Resistencia tisular al 1,25-(OH)2D3
3) Hipofosfatemia sin hipocalcemia asociada a la diabetes de fosfato (raquitismo vitamina
D-independiente)
Analítica:
a) Elevación de fosfatasa alcalina sérica
b) Cuando la causa es la falta de vitamina D, la fosfatemia es muy baja y la calcemia está
solo moderadamente reducida.
Referente al siguiente esquema: cuando el calcio en sangre baja se activa la PTH ( que
compensa la bajada de Calcio) que activa al hueso para producir osteolisis y bajar la
concentración de calcio y por otro lado estimula el riñón para aumenta la disminución renal de
Pi.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Consecuencias:
OSTEOMALACIA
1. Dolores sordos (por irritación del periostio debido a
la maleabilidad de los huesos). Más intensos en los
huesos que soportan cargas
2. Deformaciones
Consecuencias:
RAQUITISMO
1. Crecimiento retrasado
2. Deformaciones óseas:
incurvaciones de los
huesos largos,
reblandecimiento del
cráneo con el
consiguiente peligro de
lesiones cerebrales.
OSTEITIS FIBROSA: osteopatía desmineralizante del hiperparatiroidismo. La osteolisis
está exaltada por exceso de PTH, con la consiguiente eliminación renal de Pi. Como
consecuencias se produce dolores y fracturas.
OSTEODISTROFIA RENAL: el término osteodistrofia renal (ODR) se aplica en sentido
genérico a todas las variedades de enfermedades esqueléticas que aparecen como
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
consecuencia de la insuficiencia renal crónica (IRC) y del tratamiento sustitutivo de la función
renal, bien sea la diálisis o el trasplante.
TIPOS:
1. OSTEITIS FRIBROSA + OSTEOPENIA
2. OSTEITIS FRIBROSA + OSTEOSCLEROSIS
OSTEOPATIAS LOCALES
ENFERMEDAD DE PAGET: Exaltación de la osteolisis y secundariamente de la osteogénesis. La
estructura del nuevo hueso es anormal y contiene una rica vascularización para mantener la
alta tasa de renovación, pero mecánicamente es muy imperfecto.
Observamos que el hueso del cráneo es anormal ha perdido densidad. Y en el caso del fémur
tiene una transparencia a los RayosX, se distribuye mucho hueso pero también se produce de
forma que la estructura es anormal.
Causa: infección vírica de los osteoclastos por paramixovirus
Analítica:
Actividad osteoclástica: aumento de la Hidroxiprolina en orina
Actividad osteoblástica: elevada liberación a plasma de fosfatasa alcalina.
Consecuencias:
1. Dolor
2. Deformaciones
3. Fracturas (descenso de la resistencia mecánica)
4. El exceso de vascularización puede favorecer una insuficiencia cardiaca debido al
aumento de la demanda por gasto cardiaco.
ARTROPATÍAS
ARTRITIS: el término artritis indica inflamación en alguna articulación
- Monoartritis: si afecta únicamente a una articulación
- Oligoartritis: cuando son 2 o 3 las articulaciones afectadas
- Poliartritis: si afecta 4 o más simultáneamente.
Etiología: existen >100 enfermedades diferentes que pueden causarla
Por agentes mecánicos: cristales que se depositan en las articulaciones
Por agentes químicos: en situaciones de diátesis hemorrágicas, como la que aparece en
hemofílicos.
Por agentes vivos: alcanzan la articulación por vía hemática
Por mecanismo inmunológico:
Artritis de la enfermedad de suero
Fiebre reumática
Artritis reumatoide
Artritis del lupus eritematoso
Artropatías seronegativas
Manifestaciones clínicas:
LOCALES:
1. Articulaciones hinchadas y tumefactas, calientes y enrojecidas. Los contornos de la
articulación están desdibujados
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
2. Aparece dolor espontáneo y cuando se presiona o intenta activarlas activa o
pasivamente
3. Existe pérdida de funcionalidad a la que se superpone una contracción muscular refleja
que fija a cada articulación en una posición característica antálgica en la que la capsula
está relajada (generalmente flexión ligera)
4. La secuela cicatrical puede ser una perdida la movilidad (anquilosis) por fusión de los
extremos óseos.
GENERALES:
1. Fiebre
2. Anorexia
3. Adelgazamiento
Manifestaciones radiológicas:
1. Sombra fusiforme de partes blandas, que al estar infiltradas presentan mayor densidad
radiológica que las normales y aparecen como una sombra.
2. Estrechamiento de la hendidura articular. Se debe al acúmulo de líquido en la cavidad
que al tensar las uniones tendinosas aproxima a los cartílagos
3. Erosión del hueso subcondrial, puesto que el tejido inflamatorio de la sinovial destruye
el cartílago y también lesional al hueso
4. Osteoporosis de la epífisis yuxtaarticular. Las prostaglandinas y linfoquinas liberadas
por las células inflamatorias activan a las osteoclastos.
Manifestaciones analíticas:
Líquido sinovial: turbio debido al exceso de proteínas y células (menos glucosa) y poco viscoso
debido a que el ácido hialurónico está menos polimerizados
En sangre: las generales del proceso inflamatorio (anemia, leucocitosis, etc.).
Además puede encontrase cambio específicos en cada tipo de artritis:
Artritis gotosa: hiperuricemia
Fiebre reumática: elevado título de estreptolisinas
Artritis reumatoide: factor reumatoide positivo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Artritis del lupus eritematoso: anticuerpos antinucleares
Artropatías seronegativas: antígeno HLA B27
ARTROSIS: Básicamente consiste en la degeneración del cartílago articular. A veces la
artritis puede acabar en artrosis.
Etiología: (saberse solo negrita)
1. Sobrecarga mecánica: desvitalización y lisis del cartílago por microtraumatismos
repetidos. La actividad de la articulación estimula la capacidad remodeladora,, pero
esta puede estar desbordada.
2. Factores metabólicos: depósitos de uratos en la hiperuricemia o de ácido
homogentisínico en la alcaptonuria. Estos productos agreden a los condrocitos y
modifican las propiedades físicas de la matriz, por lo que el cartílago pierde su
capacidad de soportar presiones.
3. Factores endocrinológicos: la artrosis es más frecuente en mujeres postmenopáusicas
o en enfermos acromegálicos
4. Factores hereditarios: como en la enfermedad de los nódulos de Heberden en las
articulaciones interfalángicas distales de las manos
5. Factores inflamatorios.
Cambios estructurales en la artrosis:
Manifestaciones funcionales:
1. Rigidez (al iniciar los
movimientos pero desaparece
al calentar)
2. Dolor
3. Limitación de la movilidad
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. Crepitaciones (“chasquidos” que se dan en la articulación)
Manifestaciones radiológicas:
1. Estrechamiento de la hendidura articular
2. Condensación de las superficies óseas
subcondrales
3. Proliferación ósea en los bordes (OSTEOFITOS)
4. Imágenes quísticas claras formadas por
acúmulo del líquido.
DIFERENCIAS ENTRE ARTRITIS Y ARTROSIS:
TEMA 14: FISIOLOGÍA DEL TIROIDES
El tiroides está abrazando a la tráquea. Posee 2 lóbulos unidos por el istmo. La glándula deriva
de la parte baja de la lengua, sale una bolsa embrionaria que se crea la tráquea. En adultos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
queda el conducto tirogeneo que es un vestigio de la bolsa que se adhiere a la tráquea. Siendo
la glándula estrictamente embrionaria es la más grande.
CIRCULACIÓN TIROIDEA:
La parte de arriba del tiroides la irriga la arteria-tiroidea superior que sale de la carótida. La
parte baja, una arteria que sale de la subclavia, arteria tiroidea interior.
La irrigación venosa igual.
Glándula Tiroides 20 g (entre 15 y 25g)
Características:
1. Alto flujo de perfusión: 100 ml/min
(aprox 4 ml/min/g). Uno de los
flujos por gramo de tejido más
altos, salvo el del cuerpo carotideo
y el riñón. Recibe gran cantidad de
sangre, Muy bien perfundido
2. Capilares Fenestrados. Poseen poros o fenestras. Intercambio rápido de glucosa entre
extracelular y sangre.
INERVACIÓN TIROIDEA:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
a. Simpática: proviene del simpático cervical. Proviene de los plexos simpáticos que
rodean a las arterias tiroideas. Receptores para catecolaminas:
Adrenalina (más abundante en sangre)
Noradrenalina (terminales sinpáticas)
b. Parasimpática: proviene de los nervios laríngeo superior y laríngeo recurrente,
ambos procedentes del nervio vago.
1. La inervación regula el sistema vasomotor, y a través de éste, la irrigación de la
glándula. Mayor aporte de oxigeno y nutrientes pero también de yoduro y TSH para
estimular la tiroides
2. Efecto directo del SNV-S por su acción directo sobre receptores adrenérgicos, estimula
la secreción de hormonas esteroideas.
Las células están muy cargadas de Tg en los coloides (coloide: sustancia espesa y acuosa
10/15% en tirogeobulina Tg) por lo que es muy viscoso. Todo está recubierto por estructura
fibrosa. Además hay células para-foliculares o células C secretoras de calcitonina. Los que
poseen un tamaño
pequeño son los folículos
muy anchos cuando
acaben la función y se
llenen de coloide, son más
grande y son células con
poca actividad, son células
de reserva.
DINÁMICA DEL YODO EN EL ORGANISMO
La ingesta óptima del yodo es de 15 μg/día y la mínima de 50 μg/día. De las moléculas de Tg
solo se yodan determinados restos de tirosina. El tiroides pasa una parte continua de yodo y
80 μg excreta en forma de T3, T4.
En las paredes internas de las células foliculares está la TPO (tiroperoxidasa; yoduro
peroxidasa; peroxidasa tiroidea): 3 funciones:
1. Conversión: I- + H202 oxidación (TPO) I0 Gracias a la generación local de H202. Este
I0 es muy reactivo que reacciona con tirosina en 3 y 5 y se yoda.
2. Cataliza la reacción de acoplamiento, quita un grupo feridico yodado y se le pone a
otro, agrupación de DYT y MYT
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ESTRUCTURA QUÍMICA DE LAS HORMONAS TIROIDEAS: la tirosina con un anillo fenólico y tras
yodarse se forman la T3 y la T4.
T4: cuando se pierde la 5’ se obtiene la triyodotirosina. Este paso de T4 a T3 es clave, gracias a
la enzima 5’desyodasa tipo I, se da en el hígado y aumenta mucho la actividad. A veces T4 se
considera una prohormona.
En algunos territorios del SNC, adenohipofisis y placenta se puede activa la T3 con la enzima
5’desyodasa tipo II.
DINÁMICA DEL YODO EN LAS CÉLULAS TIROIDEAS:
La célula folicular del tiroides posee
una all co-transportadora (simparter)
para captar yodo se llama NIS (Na/I
symporter). Este transportador lo
mueve un gradiente de sodio que
luego usa un transportador activo 2º.
Este NIS está en otros sitios donde se
capta yodo. El transportador de un
anión grande que se usan para inhibir
la captación de sodio. Dentro de la
célula, por el transportador Pendrina
pasa al coloide.
También captan yoduro: el ovario, la
glándula mamaria, la mucosa gástrica,
la placenta, el cuerpo ciliar, la hipófisis
posterior y la corteza adrenal.
1. Oxidación
2. Yodación Tg
3. Acoplamiento de residuos DYT y MYT
4. Pinocitosis
5. Fusión
Hay parte de yodo que no sirve, por lo que se desmonta la proteína completa y el yodo sale
por la Pendrina y vuelve el proceso.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
SÍNTESIS DE LAS HORMONAS TIROIDEAS: todo este proceso se hace bajo la estimulación de
TSH estimula todos los procesos ya que activa genes y también favorce al crecimiento de la
glándula (que las células multiplican). La concentración plasmática de hormonas tiroideas es
del orden de 8 μg/100 ml, la mayoría unida a proteínas.
CONCENTRACÓN PLASMÁTICA DE HORMONAS TIROIDEAS
• 8 ug/100ml unidas a proteínas
• 3 ng/100ml libreas
Larga vida media en sangre T3 (1 día) y T4 (7 días)
METABOLISMO:
Son mecanismos de inactivación. Si se pierde un yodo de anillo interno se convierte en
T3 reversa que es inactiva (manera específica de inactivación) esto lo hace la desyodasa tipo 3
(D3) que está en hígado y riñón.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
CARACTERÍSTICAS DIFERENCIABLES DE LAS HORMONAS TIROIDEAS.
REGULACIÓN DE LA FUNCIÓN TIROIDEA
• Mecanismo Intrínseco (Efecto de Wolff-Chaikoff): el exceso de Yodo inhibe el efecto
de la TSH en el tirocito.
• Mecanismo Extrínseco
La TSH estimula:
1. La captación de Yoduro
2. La síntesis de Tg
3. La yodación de Tg
4. La reacción de acoplamiento de restos yodados de tirosina
5. La endocitosis de Tg yodada y sus proteólisis
6. El crecimiento de la glándula en situaciones de exposición prolongada a concentración
elevadas de TSH.
- En ausencia de TSH se produce atrofia tiroidea
- En situaciones de explotación prolongada a concentraciones elevadas de TSH se
produce bocio.
TSH (hormona diurética)
Mecanismo: glicoproteína de 28kDa (cadena α y cadena β). La cadena βes idéntica a la cadena
α de la FSH, la LH y la GCH. La cadena β es específica para cada una de las hormonas FSH, LH,
GCH.
Actúa sobre un receptor de membrana formado por una glicoproteína y un gangliosido.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Esta unión activa una proteína G activadora que activa a la adenilato ciclasa, lo que conduce a
la generación de AMPc.
Control de la secreción de TSH:
- Positivo: TRH
hipotalámica
- Negativo: T4 >> T3.
Directamente sobre la
hipófisis
Quizá muy débilmente
sobre el hipotálamo
La glucocorticoides
inhiben la liberación de
TRH y la de TSH.
EFECTOS FISIOLOGICOS
1. Efectos morfogénicos.
Necesarios para el
crecimiento y desarrollo
del esqueleto y sistema muscular
2. Necesarias en procesos de crecimiento, diferenciación y desarrollo, sobre todo del SN
y del esqueleto. Inhiben la proliferación de neuroblastos (desde 6 meses de vida fetal)
y estimulan la diferenciación neuronal y el desarrollo de conexiones neuronales y
mielinización (hasta 6 meses de vida neonatal)
3. Regulan el consumo de oxígeno: lo aumentan en todos los tejidos, salvo en el encéfalo
adulto, testículos, útero, ganglios linfáticos y bazo, mientras que en la adenohipofisis lo
inhibe.
4. Regulan la termogénesis. Primero aumentan el metabolismo y después de la síntesis
de proteínas desacopladas mitocondriales UCP-1, UCP-2 y UCP-3
5. Juegan un papel importante en el balance mineral. Activan osteogénesis y osteolisis.
6. Tienen un efecto potenciador recíproco con las catecolaminas
7. Activan la función del SNC por aumentar la sensibilidad de la formación reticular
facilitadora (FR) a las catecolaminas
8. Regulan el metabolismo de proteínas, carbohidratos y lípidos. Afectan a casi todos las
células menos las neuronas del adulto a pesar de haber receptores para hormonas
tiroideas.
Adaptación de la secreción de hormonas tiroideas a las necesidades metabólicas cambiantes
durante el ciclo día/noche ritmo circadiano de la secreción de TSH
EFECTOS SOBRE EL METABOLISMO
SOBRE METABOLISMO DE CARBOHIDRATOS
1. Aumentan su absorción en el tubo digestivo
2. Potencian la acción de la insulina y de la adrenalina
3. A dosis bajas estimulan la glucogenogénesis
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. A dosis altas estimulan la glucogenolisis y gluconeogénesis hepáticas
SOBRE METABOLISMO LIPIDICO
1. Aumentan la síntesis de colesterol
2. Aumentan su secreción biliar
3. En adipocitos eleva los niveles de AMPc y estimula la lipolisis.
SOBRE METABOLISMO PROTEICO
1. Favorece la acción de la GH
2. A dosis bajas estimulan la síntesis de proteínas
3. A dosis altas estimulan la proteólisis con pérdida de la masa muscular y
balance negativo de nitrógeno.
EFECTOS SOBRE LAS VITAMINAS (quedarnos solo con que interviene también en moléculas
más pequeñas como son las vitaminas)
1. Favorece la conversión de riboflavina en mono y dinucleotidos de flavina.
2. Favorece la conversión de carotenos en vitamina A y de ésta en retineno
OTROS EFECTOS
1. Algunos efectos son indirectos, regulando no solo la síntesis y secreción de otras
hormonas sino también el número de receptores para ellas.
2. En otras especias como las de anfibios, las hormonas tiroideas son responsables de los
cambios sincronizados que implica la metamorfosis.
TIPOS DE RECEPTORES NUCLEARES (RNs):
Tipo II. (el receptor de ácido retinoico, el receptor X retinoide y el receptor de
hormona tiroidea)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
RECEPTORES DE HORMONAS TIROIDEAS
Las hormonas tiroideas se unen a sus receptores que son 2 tipos NR1A1 (gen que codifica un
receptor nuclear) y NRA2 que pueden dar lugar a cuatro receptores de los cuales β tiene 3
isoformas y α tiene 2 isoformas. En cada tejido se va a sintetizar uno u otro teniendo un efecto
diferente en cada tejido.
α(TR-α) NR1A1 (nuclear receptor subfamily 1, group A, member 1)
β(TR-β) NR1A2 (nuclear receptor subfamily 1, group A, member 2)
TRE= elemento de respuesta tiroideas, están en la parte promotora de los genes diana. La
hormona tiroidea produce una pérdida de yodo de 5’ para dar T3, el receptor nucleico se une a
RXR. Así que este dímero TR-RXR formado se une a diferentes zonas al DNA y está unión
desencadena cosas. Favorece que la polimerasa se una también y de esa forma polimeriza.
INTERACCIÓN CON OTROS SISTEMAS ENDOCRINOS
AFECTAN A OTRAS HORMONAS
1. Favorece a la secreción de GH por aumento de receptores a GHRH
2. Activan el catabolismo de otras hormonas: insulina, esteroides
3. Potencian la acción de las catecolaminas. Aumenta la expresión de receptores beta
adrenérgicos
4. La T3 estimula la sulfatación de los mucopolisacaridos esqueléticos por mediación de
la somatomedina y de la GH
AFECTADAS POR OTRAS HORMONAS
1. La GH inhibe la liberación de TSH hipotalámica
2. Los esteroides afectan a la secreción de T3 y T4
De forma aguda:
Estrógenos y glucocorticoides inhiben la liberación de TRH.
De forma prolongada:
Estrógenos activan la síntesis de GBT aumenta la síntesis y la liberación de T3 y T4.
Los estrógenos activan la síntesis de las proteínas transportadoras de las hormonas
tiroideas (GBT), aumenta la síntesis y la liberación de T3 y T4
Andrógenos inhiben la síntesis de GBT disminuye la síntesis y la liberación de T3 y T4.
En este caso al revés que los estrógenos.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 15: FISIOPATOLOGÍA DEL TIROIDES
CURVAS DE DINÁMIA TRAS LA ADMINISTRACIÓN DE I131
BOCIO: aumento del tamaño de la glándula tiroidea en respuesta a la falta de hormonas
tiroideas circulantes. El más frecuente es el bocio difuso que se forma en respuesta a la falta
de hormonas tiroideas circulantes y aumenta de la estimulación de crecimiento del tiroides.
En el bocio simple se puede conseguir equilibrar el déficit hormonal si la falta de yodo no es
muy grave. La mayor captación de yodo puede compensar los bajos niveles sanguíneos.
Causas:
Menor ingestión de yodo (bocio endémicos). Falta de yodo en el agua y en los
alimentos.
Trastornos congénitos. Déficit de síntesis de T3 y T4
Ingestión de medicamentos: interfieren en el metabolismo del yodo (sales de litio)
Bociógenos naturales (plantas de las familias Brassica y Crucifera)
Componentes que interfieren en el metabolismo del yodo (coles, nabos y leche
de vacas alimentadas con estos vegetales
Sintomatología:
Aumento del tamaño del tiroides
1º FASE: difuso, homogéneo
2º FASE: nodular y funcionalmente heterógeno
En el bocio simple se consigue equilibrar el déficit hormonal. Si la falta de yodo no es
muy grave la mayor captación de yodo puede compensar los bajos niveles sanguíneos.
Recuperaciones mecánicas:
Compresión de la tráquea y del esófago (dificultad de tragar o respirar)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Puede afectar a la cava superior (distensión de las venas del cuello y de las
extremidades superiores, con edema de la conjuntiva y párpados y síncope al
toser)
Tratamiento:
Endémico: sal yodada (100-200 ug/día)
En los otros casos: interrumpir la ingestión de Bociógenos y administración de T3,T4.
HIPERTIROIDISMO: aumento de función del tiroides con niveles elevados de T3 y T4
Consecuencias fisiopatológicas:
1. Elevación del 35-60% en el metabolismo basal.
2. Hiper-actividad simpática (T3, T4 potencian la respuesta de los receptores β-
adrenérgicos).
3. Aumento de actividad de los tejidos diana
Tirotoxicosis: significa niveles tóxicos de hormonas tiroideas endógenas o exógenas.
Diagnóstico:
1. Elevación del 35-60% en el metabolismo basal
2. Mayor fijación de yodo (prueba de I131 positiva) en la glándula
3. Aumento de los niveles séricos T3 y T4
Cuadros clínicos:
- Hipertiroidismo primario, bocio nodular tóxico o enfermedad de Plummer:
• Nódulos o adenomas en la glándula que escapan al control hipofisarios
• No se acompaña de exoftalmos.
- Hipertiroidismo secundario (en la adenohipofisis) o hipertiroidismo difuso:
Hipertiroidismo con Exoftalmos (protusión del globo ocular).
Producción anormalmente elevada de TSH
• Adenoma hipofisario. Liberación TSH de forma incontrolada.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
• Resistencia hipotálamo/hipofisaria a la inhibición de T3, T4. El
hipotálamo estimula a la hipófisis y esta a las hormonas
tiroideas por lo que sigue produciéndose hormonas tiroideas.
• Más frecuente enfermedad de Graves-Basedow: proceso
autoinmune debido a la producción de anticuerpos LATS (“long
lasting tyroid stimulator”). El individuo produce LATS
(anticuerpos) que estimula hormonas tiroideas como lo hacen
las TSH
HIPERTIROIDISMO SECUNDARIO
Enfermedad de Graves-Basedow
1. Enfermedad autoinmune
2. Suele aparecer entre los 20 y los 40 años
3. Es 5 veces más frecuente en mujeres que en hombres.
Causas:
• Pérdida de peso y aumento de apetito
• Intolerancia al calor con sudoración excesiva
• Piel caliente y húmeda. Los anejos de la piel se ven afectados
o Pelo fino y poco fuerte que tiene a encanecer
o Alteraciones frecuentes en las uñas que tienden a separarse
• Trastornos osteomusculares:
o Debilidad muscular
o Osteoporosis de “turnover” alto
• Trastornos neurovegetativos:
o Hiperactividad, nerviosismo, pérdida de fuerza, temblor, mirada brillante
o Cambios de ánimo bruscos e injustificados
• Trastornos digestivas:
o Tendencia a sufrir dolor abdominal, náuseas y diarreas
• Trastornos cardiocirculatorios
o Aumento del gasto cardiaco (taquicardia y aumento de volumen/latido)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
o Palpitaciones
o Tendencia a la hipertensión y a la fibrilación auricular
• Trastornos respiratorios:
o Disnea. Fatigan prematura.
Exoftalmos: protusión del globo ocular que se asocia a la producción de un auntoanticuerpo
denominado EPF (“exophtalmos producing factor”) que producen:
1. Infiltración linfocítica y edema en los músculos oculares extrínsecos y del tejido
situado en el espacio retroocular
2. Puede complicarse con ulceraciones de la córnea, parálisis de los músculos oculares
extrínsecos y afectación del nervio óptico.
Tratamiento del hipertiroidismo:
1. Extirpación quirúrgica (tiroidectomía subtotal)
2. Drogas antitiroideas (propiltiouracilo y metimazol)
3. Yodo o Yodo radiactivo
4. Bloqueantes adrenérgicos
5. Medidas generales
HIPOTIROIDISMO: hipofunción de la glándula tiroidea con bajos niveles circulantes de T3 y
T4
Consecuencias fisiopatológicas:
- Falta de estimulación en los tejidos diana
- Mixedema: acúmulo en los tejidos de una sustancia mucoide rica en ácido hialurónico
Hipotiroidismo del adulto (Mixedema)
Causas:
- Afectación primaria del tiroides o hipotiroidismo primario
Los niveles de TSH están elevados
Respuesta de administración de T3, T4 descenso de secreción de TSH
- Hipotiroidismo secundario (hipofunción del lóbulo anterior de la hipófisis).
Los niveles de TSH son bajos
La respuesta a la administración de TRH es nula
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Hipotiroidismo
terciario
(hipofunción del hipotálamo)
Los niveles de TSH son bajos
Respuesta de administración de
TRH elevada secreción de
TSH
Hipotiroidismo de adulto o Mixedema
Causas:
• Afectación primaria del tiroides o hipotiroidismo primario
o Los niveles de TSH están elevados
o Respuesta a la administración de TRH elevada secreción de TSH
• Hipotiroidismo secundario (hipofunción del lóbulo anterior de la hipófisis)
o Los niveles de TSH son bajos
o La respuesta a la administración de TRH es nula
• Hipotiroidismo terciario (hipofunción del hipotálamo)
o Los niveles de TSH son bajos
o Respuesta a la administración de TRH elevada secreción de TSH
• Resistencia tisular a la hormonas tiroideas
o Hay niveles elevados de T3, T4 pero los tejidos son insensibles a ellas.
Sintomatología:
• Reducción del metabolismo basal, intolerancia al frío y anorexia
• Debilidad muscular
• Aspecto edematosos de la cara, la lengua y el aparato fonador
• Voz ronca
• Ageusia
• Cofosis de conducción
• Respuesta de los reflejos tendinosos retardada
• Niveles séricos elevados de colesterol, carotenos y proteínas totales
• Piel pálido amarillenta, áspera y edematosa
• Anemia macrolítica
• Cardiomegalia
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
• Bradicardia
• Hipotensión
• Estreñimiento
• Descenso del metabolismo cerebral: embotamiento, apatía y somnolencia
• Menorragia
Tratamiento:
• Durante toda la vida
• Administración de toroides desecado o de T4 y T3 en una proporción 4:1
Hipotiroidismo infantil:
Causas:
1. Falta de aporte de yodo, cretinismo o hipotiroidismo endémico
2. Falta de fijación del yoduro por el tiroides.
3. Falta de conversión del yoduro a forma molecular
4. Incapacidad de acoplar las mono- y diyodotirosinas para formar T3 y T4
5. Respuesta inexistente al estímulo de TSH
6. Falta de respuesta de los tejidos diana a la acción de las hormonas tiroideas
Cretinismo: durante la vida fetal o primeros años de vida extrauterina
Sintomatología:
• Enanismo
• Abdomen prominente
• Retraso mental
• Lengua agrandada con la cara ancha
Diagnóstico:
• Desde el nacimiento
• Presentan una hipotermia y piel seca
• Comportamiento apático
• Se observa retraso en el crecimiento
• Niveles plasmáticos de las hormonas tiroideas bajos
Hipertiroidismo juvenil: en niños mayores de 2 años que eran normales anteriormente.
Etiología:
• Tiroiditis autoinmune
• Deficiencia de Yodo
• Deficiencia funcionales parciales congénitas
• Fármacos bociogénicos
Sintomatología:
• Pueden parecer clínicamente normales
• Disminución de capacidad intelectual: letargia, apatía y déficit de aprendizaje
• Posteriormente se observa retraso del crecimiento
• Falta de maduración sexual.
TIROIDITIS: inflamación del tiroides
Cuadros clínicos:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Tiroiditis aguda: debida a una infección vírica
Tiroiditis de Hashimoto: escape de tiroglobulina
Producción de anticuerpos anti-tiroglobulina
Bocio acompañado de hipertiroidismo seguido de hipotiroidismo
ENFERMEDADES QUE MODIFICAN LA FUNCIÓN TIROIDEA
Inanación: disminuye la conversión de T4 a T3
Nefrosis: pérdida de TBG en orina.
Hiperestrinismo: aumento de la síntesis de TBG aumento de la tiroxina sérica total
Insuficiencia renal avanzada: anomalías en el metabolismo del yodo y de la TSH
FÁRMACOS QUE AFECTAN A LA FUNCIÓN TIROIDEA
Inhiben la captación de yoduro:
Acciones monovalentes:
Clorato
Perclorato
Peryodato
Biyodato
Nitrato
Tiocianato
Pertecnetato
Inhiben la yodación de la tirosina y bloquean la condensación oxidativa:
Tiocarbamidas
Tiouracilo y derivados
Propil tiouracilo
1-metil-2-mercapto imidazol
Inhiben el paso de yoduro a yodo:
PABA (ácido p-amino benzoico)
Antibióticos sulfamídicos
TEMA 16: FISIOLOGÍA Y FISIOPATOLOGÍA DE LAS GLÁNDULAS
SUPRARRENALES
Hormonas esteroides:
1. Mineralcorticoides
2. Glucocorticoides
3. Esteroides sexuales
PRODUCCIÓN DE HORMONAS POR LA MÉDULA ADRENAL
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
70-80% adrenalina (epinefrina) la
mmmás importante
20-30% Noradrenalina
(norepinefrina) en menor cantidad
La medula adrenal está inervada por
el SNV-S desde el ganglio celíaco
mediante una rama del nervio
esplácnico. La estimulación de las
células cromafines se realiza por
conexiones colinérgicas.
CATECOLAMINAS
La médula suprarrenal recibe
acción del simpático
secreción de catecolaminas y del parasimpático que en este caso no tiene inervación.
En la medula adrenal transforma la tiroxina en catecolaminas DOPA (dopamina) que actúa
como neurotransmisor Noradrenalina (más neurotransmisor aún) adrenalina que es
como la Noradrenalina pero con un metilo más, que cambian mucho, una se utiliza en el SNC y
la otra en la médula adrenal.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Dif entre el Sistema Endocrino y el Sistema Nervioso: en el sistema endocrino hay mayor
lentitud de respuesta y mayor duración mientras que en el SN es al revés.
Los principales tejidos diana de las catecolaminas son: hígado, riñón, ME, músculo liso y
estriado, tejido adiposo, corazón, vasos sanguíneos. Vamos a ver sus funciones en los
diferentes tejidos diana:
FUNCIONES DE LAS CATECOLAMINAS
- Hígado:
1. Activa glucogenolisis
2. Inhibe glucogenogénesis
3. Activa gluconeogénesis
4. Aumentan la liberación de glucosa desde el riñón
- Riñón:
1. Activación gluconeogénesis
2. Aumenta la liberación de glucosa desde el riñón.
- Músculo esquelético: si tiene acúmulo de glucógeno, activación de glucogenolisis. No
lo cede
- Músculo liso y músculo estriado: la adrenalina disminuye el catabolismo proteico.
Inhibición del catabolismo de proteínas en el M.liso, M.cardiaco y M.esquelético.
- Tejido adiposo: en el tejido adiposo blanco, la adrenalina libera glicerol y ácidos grasos
libres a partir de triglicéridos almacenados por los adipocitos. Y también activación de
lisis de triglicéridos.
- Corazón: aumentan la FC, la fuerza de contracción y la velocidad de conducción; lo que
nos lleva a un aumento del volumen sistólico y aumento de la presión arterial sistólica
y diastólica.
- Vasos sanguíneos: vasoconstricción regional en arteriolas y venas. Vasodilatación
regional en arteriolas y vénulas: ME, miocardio, hígado, SNC son territorios que
necesitan una buena perfusión. Aumenta el flujo sanguíneo en el miocardio, músculo
esquelético e hígado.
Redistribución del flujo sanguíneo en respuesta de estrés.
HIPERSECRECIÓN DE CATECOLAMINAS: FEOCROMOCITOMA
- Tumor en tejido cromafín generalmente benigno
- A veces fuera de los adrenes localizado en el bazo, aorta, ovarios, testículos y vejiga
urinaria.
- El feocromocitoma produce un aumento en
la secreción de catecolaminas de forma
controlada
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Imagen de TAC en la que se señala una masa tumoral suprarrenal. ( )
Feocromocitoma:
Formas de presentación:
1. Con hipertensión intermitente o
paroxística.(paroxística = que aparece bruscamente
y desaparece también bruscamente)
Se desencadena por:
- Situaciones de estrés emocional
- Cambios de postura
Se acompaña de:
- Nerviosismo, ansiedad, sudores, dolores de cabeza, palpitaciones.
2. Con hipertensión mantenida
Se distingue la hipertensión debida a otras causas en que el
feocromocitoma se acompaña de hiperglucemia con glucosuria.
Aumenta el metabolismo basal siendo normales los valores de T3 y T4
Los niveles de catecolaminas en plasma y sus metabolitos en orina
están aumentados.
CORTEZA ADRENAL: la médula sintetiza catecolaminas es decir Noradrenalina y adrenalina
como ya hemos visto. En la corteza se distinguen tres zonas:
1. Zona glomerular: sintetiza mineralcorticoides, el principal
es la aldosterona
2. Zona fasciular que es la central: sintetiza glucocorticoides
(cortisol)
3. Zona más cercana a la medula es la zona reticular: secreta
andrógenos en mayor cantidad y estrógenos pero en
menor cantidad. Es decir en este zona se produce la
secreción de hormonas sexuales, la principal andrógenos
sexuales (hormonas sexuales masculinas):
o DHEA
o Androstenodiona (menos importante)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ACCIONES:
1. Anabolizantes (aumentan la síntesis de proteínas) “dooping”
2. Funciones andrógenicas (favorece los caracteres sexuales masculinos secundarios)
CONTROL DE SU SECRECIÓN: se estimula por la ACTH que es liberada por la hipófisis y
controlada por el hipotálamo y no actúan sobre el eje hipotálamo-hipófisis-adrenales.
HIPERSECRECIÓN DE ANDRÓGENOS: SINDROME ANDROGENITAL
Causas:
1. Hiperplasia suprarrenal congénita (por
aumento de la ACTH)
2. Tumores suprarrenales
Consecuencias: distintas según el momento y
el sexo del individuo:
- Niñas durante la vida intrauterina:
trastornos en el desarrollo de los
órganos genitales y virilización
- Niños antes de la pubertad:
pseudopubertad precoz, crecimiento
rápido pero insuficiente
- Hombres adultos: refuerzan los caracteres sexuales secundarios masculinos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Mujeres adultas: virilización. Hirsutismo es el patrón de pelo/bello típico en hombres
que aparece en mujeres como consecuencia de este síndrome.
GLUCOCORTICOIDES
ESTRUCTURA QUÍMICA DEL CORTISOL
21 carbonos
Núcleo esteroide derivado del colesterol
3 grupos de OH en C11, C17, C21
2 grupos ceto en C3 y C20
1 doble enlace en C4-C5
Cambios en dicha molécula producen precusores :
Cortisona (con interés farmacológico) y 11-
Desoxicortisol
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
CONTROL DE LA SECRECIÓN DE CORTISOL
El hipotálamo responde al estrés y al ritmo circadiano de forma que libera de forma rítmica
CRH y controla todo el eje.
REGULACIÓN DE LA SECRECIÓN DE GLUCOCORTICOIDES
La ACTH regula y mantiene la secreción de cortisol, activando la adenilato ciclasa en las
zonas fascicular y reticular, a través de la unión a un receptor de membrana especifico
para la ACTH.
El AMPc estimula la esteroidogénesis activando una enzima que cataliza la
transformación del colesterol en pregnenolona (paso limitante)
El ritmo circadiano hipotalámico que marca la secreción de CRH se transmite a las
suprarrenales. La secreción de cortisol es máxima alrededor de las 8 a.m y mínima en
las últimas horas de la tarde.
La secreción diaria de cortisol en un adulto es de aprox. 20 mg.
Vida media 60-90 min. Acción intracelular prolongada superior a su vida media por
aumento de la transcripción de genes específicos.
Transporte plasmático: transcortina (CBG) fija el 90% del cortisol circulante.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El defecto genético de CBG no presenta manifestaciones clínicas.
MECANISMO DE ACCIÓN DE LOS GLUCOCORTICOIDES
1. Ingresan a la célula por difusión pasiva.
2. Los GC actúan a través de su unión a receptores para
GC (GR) citoplasmáticos que permanecen inactivo
3. La interacción GC-GR produce un cambio
conformacional en el receptor y el complejo se
trasloca al núcleo celular
4. En el núcleo el complejo interactúa secuencias de
ADN donde actúa el complejo GC-GR que se
denominan glucocorticoid responsive elements o GRE.
5. Los GRE se encuentran en genes específicos
modulando su expresión
6. Los efectos de los GC son ejercidos por un incremento
o una disminución de la síntesis de estas proteínas
ACCIONES DE LOS GLUCOCORTICOIDES:
1. Inhiben la síntesis de proteínas
2. Promueve el catabolismo proteico
3. Favorecen la gluconeogénesis y aumenta la glucemia
4. Potencian la movilización de grasa
5. Estimulan la eritropoyesis
6. Tienen acción inmunosupresora
7. Inhiben la osteogénesis
HIPOFUNCIÓN GLUCOCORTICOIDE
Hipofunción o insuficiencia corticosuprarrenal primaria.
Enfermedad de Addison
- Enfermedad rara:
- Prevalencia aprox 110 casos/millón de habitantes
- Incidencia de 5 a 6 casos/millón/año
- Con mayor incidencia en mujeres (3:1)
Etiología: autoinmunidad (antes frecuentemente asociada a tuberculosis)
Patogenia: destrucción de hasta un 90-95% del tejido corticoadrenal (deficiencia conjunta,
mineralcorticoides, glucocorticoides y andrógenos en la mujer lo que conlleva perdida de vello
axilar y púbico)
Forma de presentarse: insidiosa y crisis. Se presenta de forma insidiosa (sin síntomas) y
después ya se produce una crisis.
Tratamiento: acetato de cortisona, flurocortisona, sal
Anatomía patológica:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- Las tres zonas de las glándulas adrenales son progresivamente destruidas y sustituidas
por tejido fibroso.
- La médula no es atacada pero se muestra atrófica
- Se produce en primer lugar la destrucción de la zona glomerulosa seguida meses o
años más tarde de la disfunción de la zona fasciculata.
- Las hemorragias e infecciones agudas de las glándulas adrenales suelen ir asociadas a
una pérdida repentina de funcionalidad adrenal.
Manifestaciones: (ex)
1. Languidez y debilidad, mialgias, artralgias
2. Actividad hipocinética del corazón, hipotensión
3. Irritabilidad gástrica, vómitos, diarrea, dolor abdominal
4. Anorexia, atrofia muscular, azoemia
5. Cambio peculiar de la coloración de la piel (hiperpigmentación + vitíligo)
6. Hiponatremia, avidez por la sal, hiperpotasemia
7. Amenorrea
8. Disminución de la libido, menopausia prematura.
Hipofunción o insuficiencia corticosuprarrenal secundaria (ISS)
Es una condición que se desarrolla cuando la glándula pituitaria no produce suficiente
ATH para controlar la producción de hormonas suprarrenales.
Causas: cualquier procedimiento, condición o enfermedad que afecta a la glándula pituitaria
podría causar ISS.
1. Problemas en el parto
2. Fármaco (esteroides a largo plazo)
3. Radioterapia
4. Traumatismos
5. Tumores
Los signos y síntomas podrían desarrollarse lentamente sobre meses o años:
1. Sensación de mareo, debilidad o cansancio
2. Náuseas, vómito, apetito disminuido y pérdida de peso
3. Depresión o dificultad para pensar claramente
4. Dolor en los músculos, articulaciones o espalda.
5. Pérdida de cabello o parches de piel blancas.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
6. Oscurecimiento de ciertos áreas tal como los pezones, el área genital, la parte interior
de su boca o áreas expuestas al sol.
7. Deseos de alimentos particulares como regaliz o alimentos salados.
HIPERFUNCIÓN GLUCOCORTICOIDE
Prevalencia muy baja: 35-40 casos por millón de habitantes
CLASIFICACIÓN SEGÚN SU CAUSA:
Dependiente de la liberación de ACTH:
1. Tumores hipotalámicos o adenohipofisarios, hiperactividad del eje
hipotálamo-hipófisis (60-70% de los casos). Enfermedad de Cushing
2. Aumento de la secreción de ACTH por células que no están en la
adenohipofisis (tumores de pulmón, páncreas, timo). Es el síndrome de
ACTH ectópico o síndrome de Cushing paraneoplásico
3. Administración excesiva de ACTH natural o sintético.
Independiente de la liberación de ACTH:
1. Tumores adrenocorticales (secreción de ACTH disminuida)
2. Administración excesiva de cortisol exógeno (Síndrome de Cushing
Yatrogénico)
MANIFESTACIONES CLÍNICAS
1. Cara de luna llena
2. Giba por búfalo por acúmulo de grasa en los hombros
3. Obesidad central con extremidades delgadas (aspecto de escarabajo)
4. Intolerancia a la glucosa subclínica o incluso diabetes mellitus clínica
5. Hipertensión. Retención de Na+ por efecto mineralcorticoides del cortisol
6. Osteoporosis. Frecuentes fracturas vertebrales
7. Menor crecimiento en longitud en niños
8. Debilidad muscular
9. Acné, adelgazamiento de la piel, estrías purpúreas, equimosis espontaneas
10. Plétora (cara roja encendido por exceso de policitemia)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
11. Impotencia, amonorrea, virilización
12. Disminución de la resistencia a infecciones
13. Trastornos psiquiátricos: depresión, insomnio, degeneración severa, psicosis aguda.
MORTALIDAD 50% A 5 AÑOS (sin tratamiento)
a. Infecciones
b. Cardiopatía arterioesclerótica
c. Suicidio
TEMA 17. CONTROL ENDOCRINO DEL BALANCE HÍDROELECTROLÍTICO
Diferencia entre aldosterona y corticosterona en el hidroxilo que hace que 2 esteroides tengan
2 funciones diferentes. La cortisona metil oxidasa (CMO) o también llamada aldosterona
sintetasa enzima importante “enzima llave”. Si no hay ACTH no hay síntesis de aldosterona. La
zona glomerular es la única que expresa la CMO (enzima llave)
El estímulo más importante es la angiotensina II e hiperpotasemia.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
SECRECIÓN
Basal: aumenta por la mañana, postura erecta.
Estimulado: angiotensina II e hiperpotasemia
ESTÍMULOS
1. Hipovolemia:
- Disminuye la presión de perfusión renal (arteriolas aferentes)
- Estimulación de células yuxtaglomerulares
- Secreción de renina
- Activación de Angiotensinógeno (hígado) a Angiotensina (10 aa’)
- Formación de Angiotensina II (8 aa’) por la enzima conversa (vasos
pulmonares)
Estimula síntesis y liberación de aldosterona
Efecto trófico sobre la zona glomerular
Vasocontricción
Formación de Angiotensina II (7 aa’)
Importante: si hay hipovolemia hay una bajada de la perfusión renal en las arteriolas afeentes,
estimulando así las células yuxtaglomerulares dando renina Angiotensinógeno que está da
Angiotensina II: que es la clave para desbloquear la ACTH es decir estimula la síntesis y
liberación de ACTH.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ANGIOTENSINOGENO
453 aa (precursor)
ANGIOTENSINA I
10 aa. Inactivado y luego se activa en angiotensina II por ECA
ANGIOTENSINA II
8 aa. Que interaciona con su receptores y se activa. Se inactiva cuando se le
quita un aa terminal pasando de 8 aa a 7 aa. Y pasa así a angiotensina III
2. Cambios electrolíticos en el LEC: descenso del contenido en Na+ o elevación de K+
3. ACTH (efecto permisivo)
4. ASF (factor estimulador de la aldosterona de origen hipofisario)
5. Hormona lipolítica (LPH)
6. Hormona estimulante de los melanocitos (MSH)
INHIBIDORES:
1. PNA
2. Dopamina
PROPIOMELANOCORTINA Y ACTH.
1) ACTH es la principal hormona que estimuladora de la biosíntesis y secreción de
glucocorticoides
2) Hormona peptídica 39 aa. PM 4500.
3) Proviene de la POMC (241 aa.)
4) POMC se desdobla en hormonas peptídicas más pequeñas.
5) Este proceso da lugar a la secreción de β-lipotropina y pro-ATCH.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Transporte
Degradación
Vida media 15-20 min
Hígado
Riñón
Tracto gastrointestinal
Fas I: citocromo P450
Fase II: conjugación (ácido glucorónico > sulfato)
Fase III: exportación (MRP2)
Eliminación en bilis (25%) y orina (75%)
FUNCIONES DE LOS MINERALCORTICOIDES
1. Regulación de la volemia y presión arterial
a. Aumenta la volemia
b. Aumenta la presión arterial
c. Estimula la liberación de ADH por la nuerohipófisis
2. Regulación del equilibrio de Na+, K+, Cl-, H+ (sobre TCD y túbulos colesteres)
a. Estimula la reabsorción renal de Na+, Cl-, HCO-3
b. Estimula la eliminación renal de K+, H+
3. Secreción electrolítica en glándula exocrinas
a. Salivares: disminuye Na+ y Cl-
b. Sudoríparas: disminuye Na+ y Cl-
c. Gastrointestinales: eleva K+
MECANISMO DE ACCIÓN
Actúan para prevenir
1. Hiperpotasemia
2. Hiponatremia
3. Hipovolemia/hipotensión
Túbulo contorneado distal y conducto colector
1. Δ Actividad Na/K-ATPasa
2. Reabsorción de Na+
3. Acumulo de K+
4. Apertura de canales de voltaje dependientes
para K+
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
5. Secreción de K+
Conducto colector
1. Eliminación de H+
2. Reabsorción de HCO3
Hipotálamo
1. Secreción de ADH
Mecanismo de Seguridad
1. Secreción de PNA
2. Superación de tasa de reabsorción de Na+ + H2O
EFECTOS DE LA ANGIOTENSINA II
1. Es la sustancia vasopresina más potente conocida.
2. Actúa sobre el músculo liso sobre todo de las arteriolas
3. Produce reducción de la filtración glomerular por vasoconstricción simultánea de la
arteriola aferente y la eferente
4. Potencia su efecto vasopresor la Noradrenalina liberada por estimulación del SNV
simpático
5. Y la adrenalina secretada por la médula adrenal
6. Acción dipsogénica (sobre el hipotálamo) muy potente. La AGII no cruza la barrera
hematoencefálica.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
HIPOFUNCIÓN SUPRARRENAL
Causas:
1. Insuficiencia corticoadrenal primaria crónica (enfermedad de Addison)
2. Insuficiencia corticoadrenal secundaria o terciaria
a. Alteración localizada en hipófisis o hipotálamo
b. No se secreta suficiente ACTH
c. Solo se atrofia la zona fascicular y reticular
d. Se mantiene la secreción de aldosterona y disminuye la de cortisol y
andrógenos
e. Debilidad, cansancio, hipoglucemia, pérdida de vello sexual, atrofia muscular
3. Hiperplasia suprarrenal Congénita: deficiencia de 21α-hidrolasa, 11β-hidrolasa o
17αhidrolasa. Falta de enzimas comunes para la síntesis de costicosteroides exceso
de ACTH.
4. Hipoaldosteronismo
a. Primario: deficiencia de enzimas de su síntesis
b. Secundario: fallo en el sistema Renina-Angiotensina-Aldosterona (nefropatías,
intoxicación por plomo)
Consecuencias de la Hipofunción Mineralcorticoide
1. Pérdida crónica de ClNa
a. Hipovolemia
b. Hipotensión arterial
c. Elevación anormal de la reina
d. Incapacidad del organismo para hacer frente a las pérdidas hidrosalinas
2. Hiperpotasemia
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
a. Debilidad muscular
b. Arritmias cardiacas
c. Alteraciones del SNC
Manifestaciones de la HIPERFUNCION Mineralcorticoide
1. Exceso de retención de sodio: aumento del volumen del líquido extracelular
• Hipertensión > disminución de la secreción de renina menor AGII (no
confundir con la hipertensión esencial hiperreninémica)
2. Perdida urinaria de potasio: hipopotasemia debilidad y fatiga
3. La acción glucocorticoide determina una disminución de la tolerancia a la glucosa:
diabetes mellitus
4. Aumento de la eliminación renal de H+ y recuperación de bicarbonato: alcalosis
metabólica
La eliminación de H+ esta estimulada directamente por la aldosterona e
indirectamente por la producción tubular de amonio que está estimulada en
presencia de hipopotasemia (el potasio inhibe la amoniogénesis)
Causas de la HIPERFUNCIÓN mineralcorticoide
1. Hiperaldosteronismo primario: (está en la glándula suprarrenal)
a. Síndrome de Conn (adenoma adrenocortical unilateral): responde a la
adrenalectomía
b. Hiperplasia adrenocorticales bilateral (idiopático)
2. Hiperaldosteronismo secundario (la causa está fuera de la glándula)
a. Estenosis de la arteria renal hipersecreción de renina
b. Tumor de células yuxtaglomerulares productor de renina
c. Disminución del volumen intravascular: edemas hipoalbúminémicos,
insuficiencia cardíaca congestiva. Sí disminuye el volumen de los vasos se
detecta edema y insuficiencia cardiaca (no sale suficiente presión del riñón)
PROSTAGLANDINAS (familia de compuestos con muchas funciones antiagregante,
mantenimiento del conducto arterioso fetal…)
PGE2 (efecto natriurético es decir favorece la eliminación de sodio e inhibe el efecto
de la ADH)
PGF2a
PGI2 (prostaciclina)
TXB2 (tromboxano)
Acciones:
1. Sobre el sistema cardiovascular:
a. Vasodilatadores: PGE2, PGI2
b. Vasoconstrictoras: PGE2a
c. Antiagregante: PGI2
d. Efecto cronotrópico positivo sobre el corazón: PGI2
e. Mantenimiento del conducto arterioso: PGE2 y PGI2
2. Sobre el riñón
a. Reducción de la reabsorción de Na+: PGE2
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
b. Inhibe el efecto de la ADH: PGE2
La bradicina y lisi-bradicina (son inactivadas por el pulmón) Cininas y calicreina.
Efecto natriurético dificulta la reabsorción y favorece que baje la presión arterial.
Actúa sobre los vasos, sobre el riñón, sobre los vasos de la médula renal aumenta el
lavado, reducción de la presión arterial. Sistema inverso al que realiza el clico
angiotensina-renina.
SISTEMA CALICREINA-CININA
Las calicreínas son proteasas séricas que actúan sobre el cininógeno para
formar cininas (bradicinina y lisil-bradicinina) que son potentes vasodilatadores
Las cininas son inactivadas por las cininasas I y II
Pueden actuar aumentando el flujo renal medular disminuyendo el gradiente
osmótico y por tanto favoreciendo la pérdida de agua en los túbulos colectores
También presentan un efecto natriurético que podría estar mediado por una
estimulación de la síntesis de prostaglandinas.
PÉPTIDO NATRIURÉTICO ATRIAL (PNA)
Síntesis: se sintetiza los cardiocitos de la aurícula derecha. Pre-pro-PNA (152aa)
pro-PNA (126aa) PNA 28 aa
Secreción: se secreta en respuesta al aumento de volumen o presión de la
aurícula derecha.
Acciones
1. Inhibe la secreción de aldosterona y en menor medida la de
renina
2. Produce relajación del músculo liso vascular en la arteriola
aferente y una pequeña Vasocontricción en la aferente lo
que determina un aumento de la filtración glomerular
3. En conjunto induce una diuresis con natriuresis
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
4. Inhibe el centro del control cardiocirculatorio bulbar y reduce
la presión arterial.
TEMA 18: EL PÁNCREAS ENDOCRINO
El páncreas tiene una doble irrigación arterial. La salida venosa (importante) es común y va a la
vena porta que va directamente al hígado.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Anatómicamente el páncreas e hígado están muy conectados. Está formado por estructuras
globulares conectadas por canalículos. Los islotes tienen una irrigación muy abundante que va
de dentro hacia fuera. La mayor parte la forman las células β productoras de insulina, células α
(las siguientes en abundancia) sintetizan glucagón y se sitúan en la periferia, células ϒ
sintetizan Somatostatina y gastrina y menos del 5% que son las células pp que producen
polipéptido pancreático. Y menos del 5% ghrenila.
INSULINA HUMANA
Formada por 3 enlaces de disulfuro uno intracatenario y 2 cuaternario. (Cadena A + cadena B).
La insulina se libera por las células β del páncreas endocrino en respuesta a niveles elevados de
nutrientes en la sangre.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
En las vesículas de secreción disminuye el pH y corta a la proinsulina insulina + péptido C.
Por cada molécula de insulina se libera un péptido C. Se libera cuando recibe la señal está
señal es el aumento de nutrientes en sangre. No solo
se libera insulina también proinsulina, péptido C,
enzimas proteolíticas.
El péptido C tiene la ventaja de que se degrada muy
lentamente. Su liberación se lleva por las proteasas
dependientes de pH ácido.
El estimulo fundamental para liberar insulina es la
glucosa, la glucosa entra por el GLUT-2 se fosforila
por una glucokinasa, una vez fosforilado entra en la
glucolisis y genera ATP. Este ATP es muy importante
para enviar la señal. Cuanto más ATP más glucosa. El
ATP se va a canales K+ sensibles a ATP de forma que
cuando hay mucho ATP los canales K+ se cierran y se acumula el K+ dentro, el acumulo de K+
dentro produce la despolarización de la membrana que los canales de Ca++ voltaje dependiente
se abren por esta despolarización. De forma que entra Ca++ y es la señal para que las vesículas
se movilicen y se produce la liberación de insulina.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El páncreas humano adulto medio contiene aprox. 200 unidades de insulina (8mg). La
secreción diaria media de insulina se estima entre 20 y 40 unidades.
- Estimulación basal a glucemia de 80-100 mg/100ml
- Niveles en ayunas: 10 y 20μ Vml
- Máxima estimulación a glucemia de 300-500 mg/100ml
- Tras una comida o más carga de glucosa 50 a 150μ Vml
- Vida media 10 min (a la del péptido es mucho más carga)
- Degradación en hígado y riñón.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
CONTROL DE LA SECRECIÓN DE INSULINA
ACTIVAN:
1. Hiperglucemia
2. Algunos aminoácidos (leucina y arginina)
3. Ácidos grasos (palmítico)
4. El glucagón
5. Hormonas intestinales: gastrina, secretina, CCK-PZ y péptido “glucagon-like”
6. El SNV parasimpático
INHIBEN:
1. La Somatostatina suprime la secreción de ambos, insulina y glucagón
2. El SNV simpático
3. Catecolaminas: a través de los receptores adrenérgicos alfa (inhibidores) y beta
(activadores). Predomina el efecto inhibidor de la secreción de insulina.
4. Las prostaglandinas inhiben la respuesta de la glucosa pero no a los aa. Por ello los
inhibidores de la síntesis de prostaglandinas (salicilato, tolbutamida, cloropropamida)
mejoran la respuesta a la glucosa.
5. La insulina inhibe la secreción
EFECTO INCREATINA
El efecto increatina es el fenómeno por el cual la ingesta de glucosa por vía oral produce un
incremento de glucosa por vía oral. Produce un incremento en la secreción de insulina superior
a la administración de cantidades similares de glucosa por vía intravenosa.
RECEPTOR DE INSULINA.
Tiene capacidad de sí solo de llevar a cabo
la señal.
Cuando llega la insulina el receptor se
activa y lo primero que hace es
fosforilarse. Las células se hacen un poco
sensibles a la insulina porque bajan los
niveles de TNFα. De todos los IR el más
activo es el IRS-1 (fosfatidil- inositol-
3kinasa), se desencadena una cadena de
señales que son responsables a corto y
largo plazo de la síntesis de insulina.
Las GLUT funcionan en función de gradiente de glucosa.
- GLUT-2: células pancreáticas, hígado, intestino
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
- GLUT-3: SN, placenta
- GLUT-1
Estas son no sensibles a la insulina (es decir
no necesitan insulina) Sin embargo los que
captan glucosa a través del GLUT-4 (músculo,
tejido adiposo y musculo cardiaco) estos
tejidos necesitan insulina.
EFECTO REGULADOR DE LA EXPRESIÓN GÉNICA.
Intervienen en la vía de señalización de MEX kinasa
Mecanismo de regulación de la señal de la insulina.
1. Degradación y número de receptores de la membrana celular por endocitosis y
reciclaje.
2. Fosforilación en residuos de Ser/Thr de IR y de IRS. Disminuyen la actividad del
receptor o de proteínas de la vía de señalización.
3. Proteínas con actividad fosfatasa de tirosina (PTPs), que desforilan proteínas clave de
la señalización de la insulina como el IRS a su propio receptor.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ACCIONES DE LA INSULINA
A grandes rasgos se puede decir que la insulina:
a. Favorece el anabolismo (construir reserva)
b. inhibe el catabolismo.
Gran parte de los efectos de la insulina son dependientes de los niveles de otras hormonas y
muchos son tejido-específicos. Por ejemplo, estimula el transporte de glucosa a través de la
membrana plasmática del musculo y el tejido adiposo pero no del tejido nervioso, los
eritrocitos ni el hígado.
ACCIONES RÁPIDAS (segundos):
1. Aumentan la oferta intracelular de sustratos.
2. Estimulación del transporte de glucosa, aminoácidos y nucleósidos.
ACCIONES A MEDIO PLAZO (minutos si se trata de activación o más lento si se trata de síntesis
de novo)
1. Modificaciones en la actividad de algunas enzimas que determinan cambios en las
células diana.
2. Activación de la glucolisis hepática
3. Estimulación extrahepática de rutas anabólicas
a. Síntesis de glucógeno
b. Lipogénesis
c. Síntesis proteica
4. Inhibición de rutas catabólicas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
a. Glucogenolisis
b. Lipolisis
c. Proteolisis
ACCIONES A LARGO PLAZO (horas o días)
1. Estimula el crecimiento. Al inhibir la proteólisis favorece el crecimiento, sobre todo el
músculo
2. Estimula la diferenciación celular.
Gran parte de estos efectos son dependientes de los niveles de hormona y muchos son tejidos-
específicos. (Estimula el transporte de glucosa a través de la membrana plasmática del
músculo y el tejido adiposo pero no del tejido nervioso, los eritrocitos ni el hígado)
GLUCAGON
• Células alfa de los islotes de Langerhans
• Polipéptido sencillo de 29 aa (3.5 kD) sin puentes disulfuro. Requiere la secuencia
entera para su efecto hiperglucemiante, mientras que le bastan los primeros 23 aa
para su acción lipolítica.
• Se sintetiza en forma de proglucagón de 37 aa
• Vida media 10 min
• Degradado en el hígado y otros tejidos por la Dipeptidil aminopeptidasa I.
El glucagón hormona antagonista de la insulina. Se sintetiza por las células α del páncreas y
sube todo cuando no hay glucosa. La hiperglucemia es la señal más potente que inhibe la
síntesis de glucagón.
El pre-pro-glucagón procesada diferente en distintos territorios, es una señal única y se queda
como pro-glucagón en las células pancreáticas se corta en diferentes péptidos y uno de
ellos es el glucagón. En cambio en otras células de otros tipos de péptidos pero ninguna es el
glucagón, diferente valor hormonal.
La regulación paracrina la llegan las células próxima al tejidos que son la β. Cuando hay insulina
frena la síntesis de glucagón. Otras son ϒ (Somatostatina) que inhibe la síntesis también de
glucagón.
MECANISMO:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
1. Receptor ligado a una proteína G
2. Activación de adenilato ciclasa
3. Aumento de los niveles de AMPc
4. Activación de PKA
5. Inicio de cascada de señales intracelulares en diferentes territorios
La consecuencia es que hace lo contrario a la insulina:
1. Inhibe el anabolismo
2. Activa el catabolismo.
SECRECIÓN DE GLUCAGON
La estimulan:
a. Hipoglucemia es el estimulador más potente
b. Aumento de aa gluconeogénicos como arginina y leucina.
c. Factores hormonales : GH, PZ-CCK
d. Control nervioso: SNV Simpático (receptores β-adrenérgicos)
La inhiben:
a. La hiperglucemia
b. Ácidos grasos y cuerpos cetónicos
c. Factores hormonales:
Somatostatina
Secretina
Serotonina
d. Control nervioso: SNV Parasimpático.
ACCIONES DEL GLUCAGÓN
A grandes rasgo se puede decir que el glucagón:
1. Inhibe el anabolismo
2. Estimula el catabolismo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ACCIONES DEL GLUCAGÓN SOBRE OTROS ÓRGANOS
RELACIÓN INSULINA/GLUCAGÓN (I/G)
OTRAS HORMONAS PANCREATICAS
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
• Somatostatina
• Polipéptido Pancreático (PP)
• Pancreastatina
• Betagranina
• Amilina
• Ghrelina
SOMATOSTATINA
Existen dos formas 28 aa y 14 aa.
Secreción:
- Por las células D de los islotes de Langerhans
- Su liberación es estimulada por el glucagón
También se sintetiza por diferentes regiones del SNV: eminencia media (capa externa),
hipotálamo (núcleo arqueado), Glándula pineal, órgano subcomisural.
Acciones:
1) Control paracrino por inhibición de la secreción de:
Insulina TSH VIP Gastrina
Glucagón PTH GIP Motilina
GH Calcitonina CCK Pepsina
2) Inhibe el vaciamiento gástrico
3) Inhibe la motilidad duodenal
4) Inhibe la motilidad de la vesícula biliar
5) Inhibe la absorción intestinal de glucosa.
POLIPÉPTIDO PANCREÁTICO (PP)
36 aa 4,3 kDa
Secreción:
• Se libera por las células PP o F tras comidas ricas en proteínas
• No se afecta por grasas o carbohidratos
• La inervación vagal es un potente estimulador de la liberación de PP medida por
receptores colinérgicos bloqueables por atropina.
• La Somatostatina inhibe la secreción de PP, mediante un fenómeno con efecto rebote
una vez que se ha liberado la inhibición.
Acciones:
1. Inhibe la secreción ácida del estómago
2. Inhibe la secreción de enzimas pancreáticas
3. Relaja la vesícula biliar.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
TEMA 19: DIABETES MELLITUS Y SÍNDROME METABÓLICO
DIABETES MELLITUS
Se reconoce desde la antigua medicina griega por la triada:
1. Polifagia
2. Poliuria
3. Polidipsia
Mas modernamente por la detección de
1. Hiperglucemia
2. Glucosuria
Epidemiología:
Afecta al 3% de la población. El máximo de morbilidad se encuentra entre los 60 y 70
años. Proporción de jóvenes en la cifra total de diabéticos: 1-2% en Europa Central; 5%
en Estados Unidos.
Causas:
Predisposición genética:
El 40% de los diabéticos tienen antecedentes familiares
En los gemelos univitelinos, la diabetes se presenta en ambos individuos casi un 100%
de los casos
Los hijos de padres diabéticos tienen una probabilidad del 28 al 30% de convertirse
también en diabéticos.
Los patrones de transmisión hereditaria de la diabetes se desconocen.
Factores desencadenantes:
Exceso de peso corporal
Modificaciones hormonales (embarazo)
Determinados medicamentos
Ciertas enfermedades infecciosas
Ciertas enfermedades metabólicas (cirrosis hepática)
Patogenia:
1) Deficiencia de insulina por hipofunción de las células beta
a. La desconexión de las células beta del sistema endocrino
• Pancreatectomía total
• Infecciones selectivas por virus citotropos
• Destrucción autoinmune de las células beta
• Ataque químico de las células beta
b. La síntesis deficiente de insulina activa
• Se forma muy poca proinsulina
• Se sintetiza una insulina errónea
• Está alterada la conversión de proinsulina en insulina
• La insulina se inactiva intracelularmente antes de su secreción
c. La alteración de la secreción
• Acoplamiento estimulo-secreción defectuoso.
2) Deficiencia de insulina por alteraciones ajenas a las células beta.
Alteraciones del transporte de insulina a la célula destinataria
Mayor degradación de insulina en hígado, riñón, músculo y tejido adiposo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Inhibición por hormonas antagonistas (corticoides, somatotropina o glucagón)
Defecto del receptor de insulina en la célula destinataria.
3) Hiperglucagonemia
FORMAS DE DIABETES MELLITUS:
Diabetes juvenil o de tipo I:
o Falta casi total de insulina
o Células β disminuidas tanto en número como en tamaño y funcionalidad
o Típico en pacientes menores de 40 años
o Es necesaria la administración de insulina
Diabetes del adulto o Tipo II:
o La falta de insulina es relativa
o En ayunas: niveles normales o incluso algo elevadas de insulina
o Tras la comida: no se secreta insulina en tiempo y cantidad adecuados
o Puede influirse favorablemente sobre estos procesos con sulfonilureas
o En pacientes obesos, pueden existir alteraciones en el receptor de insulina.
Diabetes gestacional:
o Aparece en la 2º mitad del embarazo en 3-10% de las gestaciones
o Hiperglucemia con niveles normales o elevados de insulina
o Desaparece tras el parto
o Efecto antiinsulimico de lactógeno placentario y el cortisol.
FASES DE LA DIABETES MELLITUS:
Diabetes mellitus potencial: es la predisposición genética a la enfermedad
Diabetes mellitus latente: cuando puede presentarse una alteración metabólica diabética
transitoria (durante el embarazo, infecciones u otras circunstancias). Las pruebas de carga de
glucosa son transitoriamente patológicas.
Diabetes mellitus subclínica: de forma estable las pruebas de carga de glucosa dan valores
anormales, pero en ayunas, los valores de glucemia, no son patológicamente elevados.
Diabetes mellitus manifiesta (clínica): aparece hiperglucemia, glucosuria e hipo-insulinemia
claramente anormales y mantenidas.
PRUEBA DE TOLERANCIA DE GLUCOSA
1. Toma inicial de una muestra de sangre (en ayunas de 10-12 h)
2. Se ingiere una solución glucosada (algún zumo) con 75g de glucosa
3. Se espera en reposo de 2 h antes de realizar una nueva extracción de sangre
A veces se extrae una muestra de sangre adicional a la hora o con mayor frecuencia. Según los
valores de glucemia obtenidos a las 2 h resulta:
Glucemia Diagnóstico
< 140 mg/dL Normal
Entre 140 y 200 mg/dL Prediabetes, intolerancia a la glucosa o
resistencia a la insulina
>200 mg/dL Signos de diabetes mellitus. Alcanza altos
valores y tarda más tiempo en recuperarse.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ALTERACIONES DEL METABOLISMO DE LOS GLÚCIDOS
Si no hay insulina en el tejido muscular y los tejidos adiposos no captan glucosa por falta de
GLUT-4. Se produce proteólisis y utiliza aminoácidos y también hipolisis de forma que se pase
en disposición del hígado más lípidos. Todo ello contribuye a que suba la glucemia.
En el riñón hay mucha glucosa y tiene glucosuria porque los sistemas de recuperación del riñón
están saturados por lo que es muy proclive a las infecciones en el sistema urinario. Y además
tiene diuresis osmótica dando lugar a hipovolemia.
Está hipovolemia produce hipoxia: lactato que tiene un sustrato que tiene el hígado para
producir más glucosa. La hipovolemia se va a detectar a nivel del aparato yuxtaglomerular
produciendo renina llegando a la corteza adrenal produciendo aldosterona, haciendo disminuir
K+ que repercute en las células excitables y también lo detecta el hipotálamo produciendo
sensación de sed (polidipsia). La hipovolemia también produce hipertensión, sensación de
cansancio, la perdida de agua nos lleva a la deshidratación como por ejemplo en el ojo
frecuente oftalmopatias
Dijimos que como no hay insulina se producía una proteólisis aumentada dando lugar a atrofia
(pérdida de peso). Los aminoácidos se utilizan para la gluconeogénesis produciendo urea y la
parte carbonada pasa a glucosa, así que el balance de nitrógenos es negativo.
En estado de acidosis el musculo libera K+ (pierde el riñón mucho K+ favorecido por el músculo
y por el efecto de la aldosterona) En el caso de lípidos hay una – lipogénesis y + lipolisis que
desmanta las reserva lipídica de los adipocitos y liberan a la sangre colesterol y ácidos grasos
(acetil-CoA y acetoacetil-CoA)
Aumenta la cetogénesis , muchos cuerpos cetónicos dan muchos efectos secundarios:
cetonuria, dolor abdominal, nauseas, vómitos. Además, da alcalosis metabólica que el pulmón
intenta compensar, entonces hipoventilación: produciendo “cansancio” en el corazón.
Con los ácidos grasos que el hígado está convertir en cuerpos cetónicos, lo que hace es
restrificarlo formado otra vez TG y almacenarlo y se acumula en forma de gotas de grasa
produciendo a largo tiempo una inflamación produciendo esteatosis (una causa de cirrosis)
Parte de los TG formado se ponen en circulación como LDL produciendo hiperlipemia
disminución de triglicéridos por lo que hay una lipidemia acumulativa produciendo
pancreatitis, aterogénesis, lipemia, xantomas, ateromas…
+ diapo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
COMPLICACIONES CLÍNICAS AGUDAS
A. Hipoglucemia: postprandial en diabetes tipo II o insulinemia en tipo I
B. Como diabético:
Coma cetoacidótico: olor a manzanas del aliento, respiración de Kussmaul (lenta y
profunda) sequedad de piel y mucosas e insuficiencia circulatoria ( depleción
hidrosalina e hipovolemia), embotamiento progresivo pro trastornos
hidroelectrolíticos.
Coma hiperosmolar
Complicaciones a largo plazo:
1. Arteriosclerosis acelerada:
a. Es más precoz
b. Se desarrolla más rápidamente
c. El estrechamiento es más marcado
d. Afecta a más vasos sanguíneos
2. Microangipatias: engrosamiento de la membrana basal de arteriolas y capilares.
a. Retina: retinopatía
b. Riñón: proteinuria. Descenso de la velocidad de filtración glomerular.
Insuficiencia renal.
3. Neuropatía:
a. Alteración de los nervios periféricos: parestesia, dolor, hipoestesia ( perdida de
la percepción de temperatura)
b. Alteración del SNV: diarrea nocturna, hipotensión postural, impotencia por
disfunción de la erección, alteraciones en la micción (vejiga neurógena)
4. Cataratas seniles prematuras: opacidad del cristalino
5. Pierna y pie “pie diabético”: claudicación intermitente, dolor en reposo y necrosis
gangrena.
SÍNDROME METABÓLICO: síndrome metabólico, síndrome X, plurimetabólico, de
insulinorresistencia o síndrome de Reaven: situación en la que concurren en un mismo
individuo varias enfermedades o factores de riesgo que aumentan su probabilidad de padecer
tanto diabetes mellitus como enfermedad cardiovascular por hipertensión arterial y
dislipemia, generalmente acompañada de obesidad e hígado graso.
En USA 25% de la población mayor de 20 años padece del síndrome metabólico. Los criterios
de la OMS (1999) para el diagnóstico del síndrome metabólico requieren la presencia de:
1. Diabetes mellitus,
2. tolerancia anormal a la glucosa,
3. glucemia de ayuno anormal o
4. resistencia a la insulina
más dos de los siguientes:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
1. Hipertensión arterial (>140/90mmHg)
2. Dislipidemia: triglicéridos (TG): > 1.695 mmol/L y/o colesterol HDL (HDL-C) <0.9
mmol/L (en hombres), <1.0 mmol/L (en mujeres)
3. Obesidad central: relación cintura/cadera >0.90m (en hombres), >0.85m (en mujeres),
y/o índice de masa corporal (IMC) > 30 kg/m2
4. Microalbuminuria: excreción urinaria de albúmina >20 mg/min o relación
albúmina/creatinina en orina >30 mg/g
TEMA 20: FISIOLOGÍA Y FISIOPATOLOGÍA DEL APARATO REPRODUCTOR
MASCULINO
Determinación y diferenciación sexual
El sexo de un individuo viene determinado por los cromosomas. En la mujer hay ausencia del
cromosoma Y que hace que predomine la X. Se necesitan los 2 para dar lugar a un individuo
fértil.
Proceso que ocurre desde que estamos en el estadio indiferente hasta que tenemos un
individuo perfectamente definido de cualquiera de los 2 géneros. Esta diferenciación se
produce a partir de la sexta semana.
En el varón la presencia de una región determinante del sexo es el cromosoma Y. En la sexta
semana empieza a producir factores que hacen que esa gónada indiferente se forme en el
testículo.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Además estos testículos empiezan a producir testosterona (hormonas) que hace que se
desarrollen los conductos de Walt y se forme el aparato reproductor masculino y se formen y
desarrollen los genitales masculinos. Se produce el factor inhibidor de Muller que va a impedir
que se generen los conducto de Muller y así no se forme el gameto femenino (AMH: hormona
anti- mulleriana)
En el caso de la mujer
ocurre lo mismo. La
gónada indiferente va a
evolucionar hasta
originar el ovario. Como
no hay testosterona, los
conductos de Walf
degeneran , se forma el
útero y todo el aparato
reproductor.
Durante la infancia no se
producen muchos cambios. En la escercia (pubertad) sí se producen cambios secundarios. La
pubertad se produce de media a los 11 años en niñas y 12 en niños. La mujer a partir de la
menarquia y varón por la primera eyaculación alcanzan la madurez sexual.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La espermatogénesis del varón se mantiene durante toda la vida a diferencia de las mujeres
hasta a menopausia, sobre los 50 años cesa el ciclo reproductor.
Anatomía del aparato reproductor masculino:
En los testículos (gónadas) se van a formar los espermatozoides y la testosterona. Aprox. 80%
de la masa del testículo está formado por los túbulos somníferos en cuyo interior se van a
producir los espermatozoides.
Además hay una serie de conductos reproductores accesorios:
Epidídimo: pegado al testículo donde se almacenan los espermatozoides y adquieren
movilidad.
Conducto deferente: sale de la cola del epidídimo, se continúa con el conducto eyaculador y
por último la uretra (salida de semen y de orina).
Además hay unas glándulas secretadoras (3) que van a producir el semen: vesículas seminales,
glándula prostática y glándulas bulbouretrales.
Inmediatamente después del nacimiento los testículos descienden desde el abdomen hasta la
bolsa escrotal, si no descienden se produce criptorquidia y puede producir esterilidad.
Espermatogénesis:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Se produce dentro de los túbulos somníferos. Los túbulos somníferos están llenos de
precursores de espermatozoides en distintos estados de diferenciación. Además están las
células de Sertoli que van a producir sustancias nutritivas para los precursores de los
espermatozoides.
En varones, a partir de la pubertad, la FSH (folículo estimulante hormonal) va a estimular la
producción de espermatozoides.
Las células espermatogonias se dividen y van a dar un espermatocito primario, este se divide
por meiosis y da lugar a una
espermatocito secundario.
Éste se divide para dar
espermátidas que se
diferencian y dan lugar al
espermatozoide.
En este proceso las células se
acercan a la luz del túbulo,
este proceso tarda 75 días.
Estos recién formados son
inmaduros e inmóviles. Pasan
al epidídimo donde adquieren
movilidad.
El espermatozoide:
Los espermatozoides son viables durante varios meses, sino son fagocitados por las células del
epidídimo.
Los espermatozoides maduros tienen 3 partes: cabeza, fragmento intermedio y cola o flagelo.
En la cabeza, prácticamente está el núcleo y una cubierta, acrosoma, que va a liberar enzimas
líticas que van a ayudar a disolver la cubierta que protege el óvulo.
La zona intermedia está formada por una banda de mitocondrias, ésta rodea a los
microfilamentos que van a mover a los microtúbulos de la cola y produce energía.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
El semen:
Volumen medio: 3ml
Composición:
- Espermatozoides (100 millones/ml) oligospermia < 20 millones/ml = infertilidad.
- Secreciones de las glándulas accesorias (90% volumen):
o Vesículas seminales
o Próstata
o Glándulas bulbo-renales
Funciones:
- Transporte y protección de los espermatozoides (rico en prostaglandinas, alcalino)
- Nutrición de los espermatozoides (rico en fructosa)
-
Fluido eyaculado que está formado por
espermatozoides y por secreciones de las
glándulas seminales.
Vasectomía: el volumen de semen no se
modifica (90% secreciones) pero no hay
espermazoides
Erección y eyaculación:
Erección: se produce por un encharcamiento del pene con sangre. El proceso se inicia con
estímulos seminales o la estimulación táctil del glande del pene. La alteración de la erección
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
puede deberse a algún problema físico o psicológico (impotencia). Está involucrado un arco
reflejo medular (región sacra), las órdenes se mandan por vías eferentes parasimpáticas que
produce una VD de las arteriolas del pene, de tal manera que entra sangre y las estructuras
que forman el pene (cuerpo cavernoso, y cuerpo esponjoso) se llenan de sangre. Además hay
una contracción del músculo isquiocavernoso que impide la salida de la sangre, esto va a llevar
a su endurecimiento que es lo que contribuye la erección.
Eyaculación: es una acción refleja que consiste en la escisión de espermatozoides y de
secreciones de las glándula, primero a la uretra, seguido de una eyección súbita del semen
fuera de la uretra. Los emisores de las secreciones de las glándulas siguen un orden. En un
primer lugar ya durante la erección descargan las glándulas bulbo uretrales que van a lubricar
la uretra. En la eyaculación lo primero que descarga es la próstata, es una secreción alcalina.
Tras esto se liberan los espermatozoides del epidídimo y por último descargan las vesículas
seminales que arrastra y empuja hacia fuera los espermatozoides.
Esta eyaculación también es un reflejo medular que se integra en la región lumbar, los
estímulos son táctiles, las órdenes en este caso se emitían por eferentes simpáticos que van a
contraer el músculo liso de las paredes de las glándulas y del epidídimo. Finalmente la
contracción del músculo isquiocavernoso y bulboesponjoso son lo que producen la salida
pulsátil del semen fuera de la uretra. Mientras ocurre esto, se cierra el esfínter de la uretra
(esfínter uretral superior) para que no se ascienda a la vejiga de la orina
FASES En el hombre: En la mujer:
1. Excitación Erección del pene Lubricación vaginal
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
2. Meseta Erección del pene Erección del clítoris
3. Organismo Eyaculación Contracciones vaginales
4. Resolución
La testosterona:
Acciones:
1. Estimula el desarrollo del aparato
reproductor masculino: pene y
testículos
2. Estimula el desarrollo de los caracteres
sexuales secundarios: cambio tono de
voz y vello corporal
3. Es anabolizantes proteica (en músculo
y hueso)
4. Promueve la libido.
Principal hormona masculina, se produce en
las células de Leydig es una hormona esteroide
que se sintetiza a partir del colesterol, viaja en
sangre unido a la globulina específica.
Por acción de una reductasa se forma
dihidrotestosterona que es mucho más
potente en los tejidos.
Tiene varias acciones.
La mayoría de las acciones se ponen de manifiesto en la pubertad.
Control hormonal de la reproducción masculina:
Bajo regulación del HPT e hipófisis.
En cuanto al HPT se produce una hormona que se llama hormona liberadora de gonadatrofinas
(GnRH) y estimula la liberación de otras hormonas que son FSH y LH (tienen 2 subunidades α y
β ) son comunes las α y distintas las β. La FSH estimula la espermatogénesis en los túbulos
seminíferos y la LH actúa sobre las células Leydig estimulando la producción de testosterona.
Esta testosterona a su vez es necesaria para llevar a cabo la espermatogénesis. Bajo el control
feed-back negativo. El exceso de testosterona va a inhibir la secreción de LH pero apenas la de
FSH. La inhibina (hormona peptídica se produce en las células de Sertoli que dan nutrientes) en
exceso inhibe a nivel de HPT y adenohipófisis la FSH.
Tanto en el hombre como en la mujer depende de la regulación del eje hipotálamo/hipofísis
hormona liberado de horganotropinas se libera na cantidad de esta hormona a la sangre de
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
manera pulsatil estimulando otras hormonas FSH y LH (glicoproteínas con 2 subunidades alfa y
Beta que son comunes las alfa se diferencian en las beta, tienen acción sobre testículos)
- FSH; estimula la producción de espermatozoides en los túbulos semininferos
- LH: actúa sobre las células de leche produciendo la formación de testosterona. De
manera indirecta también actúa para la espermatogénesis.
Este eje hipotálamo-hipófisis está regulado por retroalimentación negativa. Un exceso
testosterona inhibe la producción de LH pero sobre la FSH no tiene gran efecto. La inhibina
se produce en las células de Saroli que producen nutrientes para los espermatozoides y
cuando están en exceso inhiben la FSH.
HIPOGONADISMO MASCULINO:
Situación patológica, producción insuficiente de testosterona por parte de los testículos de tal
manera que los niveles de testosterona en sangre son bajos.
1. Primario: de origen testicular, por: castración, agresión por microorganismo o
radiación, traumatismos, fármacos, Síndrome de Klinefelter
Síndrome de Klinefelter: situación congénita, estos individuos tienen una trisomia de los
cromosomas (XXY) son estériles al tener un cromosoma X de más.
2. Secundario/terciario: lesiones de hipófisis/hipotálamo. Hiperprolactinemia
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Hiperprolactinemia: niveles elevados de prolactina en sangre que inhibe a nivel del eje
hipotálamo-hipófisis de Gonadotropinas. Cuando el trastorno se instala antes de los cambios
durante la pubertad hipogonadismo prepuberal. Presenta también poca masa muscular.
Formas de hipogonadismo masculino
Hipogonadismo prepuberal o enunquismo: no se desarrollan los caracteres sexuales
primarios ni secundarios. No aparece la libido. Impotencia y esterilidad. Talla superior
a la normal, con extremidades largas
Hipogonadismo pospuberal: disminuye la libido. Impotencia e infertilidad.
HIPERGONADISMO MASCULINO
Situación patológica debido a un exceso de testosterona bien en términos absolutos o en
término relativo a la edad de individuo.
Causas de hipergonadismo:
Primario: tumores testiculares productores de testosterona.
Secundario: hiperestimulación por gonadotrofinas hipofisarias o ectópicas.
Ectópica: cuando se produce una hormona en sitios que no son el suyo. Las consecuencias van
a ser diferentes si ocurren antes o después de la pubertad.
Consecuencias del hipergonadismo:
- Pubertad precoz (con espermatogénesis, en el secundario): si ocurre antes de los 9
años el desarrollo. Si se producen espermatogénesis, el individuo es fértil y se habla de
pseudopubertad no se produce espermatogenesis, como hay mucha testosterona no
se produce FSH (inhibida) no se producen espermatozoides. Después de la pubertad
no hay manifestaciones.
- Pseudopubertad precoz (sin espermatogénesis, en el primario)
- Después de la pubertad no hay manifestaciones
TEMA 21: FISIOLOGÍA Y FISIOPATOLOGÍA DEL APARATO REPRODUCTOR
FEMENINO.
ANATOMÍA DEL APARATO REPRODUCTOR FEMENINO
Durante la hemorragia menstrual se elimina el endometrio. (Controlada por un ritmo
intrínseco). Los órganos primordiales son los ovarios con 2º función producción de los gametos
femeninos (óvulos) y la producción de las hormonas (estrógenos y progesterona) También las
trompas de Falopio, muy próximo al ovario, cuando se produce la ovulación por movimiento
de las fimbrias se aproximan hacia el ovuducto. La parte de abajo del útero cérvix
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
comunicación con el exterior. Los genitales externos son el himen con labio superior y inferior
y el clítoris.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La pared del útero está formada por miometro. El endometrio se implanta aquí el embrión,
está capa es la que se desprende en cada menstruación para preparar en el caso de
fecundación.
EL CICLO OVÁRICO.
Las células germinales que van a dar lugar a los ovarios (oogenias precursores del óvulo) ya
sufren a un primer estado de la meiosis para dar lugar a oocitos primarios de tal manera que
en el momento del nacimiento hay un millón de oocitos primarios en los ovarios. Estas células
van degenerando de tal manera que al llegar a la pubertad solo quedaría 400.000 oocitos
primarios. Esa disminución sigue ocurriendo con el tiempo. Esos oocitos primarios se
encuentran dentro de los folículos primarios formados por el oocito primario y una capa de
células llamada capada de células
de granulosa. A partir de la
pubertad y bajo la FSH en cada ciclo
ovárico cada mes varios folículos
primarios empiezan a crecer y a
desarrollarse aunque lo normal es
que solo una de ellas llegue el
estadio final de la ovulación el resto
degenera. Solo 400 oocitos
primarios son los que van a ovularse
del resto se degenera.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Las células empiezan a multiplicarse y producen una sustancia rica en mucopolisacaridos
produciendo una zona pelusida sigue el crecimiento y se rodea a de una doble capa de células
del ovarios: TECA externa y TECA interna más fibrosa
Sigue el crecimiento y las células produce un líquido que se van acumulando en una capa
central antro, hasta que al final es esta fase tenemos un único folículo maduro que recibe el
nombre del folículo de Graft. Durante este crecimiento en la fecha se producen los precursores
de hormonas -> estrógenos (solo durante esta primera fase se produce estrógenos) y en un
momento dado el folículo maduro y bajo la influencia de la LH en sangre, revienta y sale al
exterior el occito y se forma al redecir del ocito la corona radiata ovulación.
Mientras esto ocurre también ocurre que se termina la meiosis y el oocito primario da lugar a
un oocito secundario (haploide) y se pierde una pequeña célula que se llama primer cuerpo
polar. Ya en el ovoducto (trompa) se produce una segunda división para formar el ovulo
maduro para dar lugar a la ovulación.
Esta estructura se llama el cuerpo luteo formado por los restos del folículo maduro que es una
estructura endocrina muy importante sigue produciendo estrógenos y además progesterona.
Este cuerpo luteo tiene una vida viable de 12 días, sí no se reciben señales de embrión este
cuerpo luteo regenera y baja bruscamente de producir hormonas y esta caída brusca es la que
desencadena el sangrado menstrual.
Por lo que el ciclo ovárico se divide en 2 fases:
1. Fase folicular hasta la obtención del folículo maduro produciendo estrógenos. Se
produce un pico de estrógenos al final de la fase folicular. Este pico produce la
liberación de LH por lo que se produce la ovulación
2. Además de producción de estrógenos que produce progesterona. 28 ± 7 de
menstruación intervalo.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Cuerpo luteo nueva estructura endocrina, produce sobre todo estrógenos y también
progesterona.
CICLO MENSTRUAL
Se refiere más a los acontecimientos que ocurre en el útero. Se inicia el primer día de la
hemorragia menstrual, la menstruación tiene una duración entre 3 -5 días en los vuales se
produce desprendimiento de la pared endometrial quedando solo una zona basal. Durante
estos días en los ovarios empiezan a crecer los folículos que se produce estrógenos cuya
misión es estimular y la proliferación del endometrio por ellos esta primera fase se llama fase
proliferativa. De hecho en esta fase empieza entre 2 a 3 veces. La anclura del endometrio y se
produce la ovulación y empieza a producir progesterona y los estrógenos siguen proliferando
el endometrio y la progesterona. Las glándulas empiezan a cargase de producto secretores
como glucógeno y otras de tal manera que se convierte el endometrio en un tejido llamado
decidua (grande y esponjoso y con mucha irrigación)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Está preparándose para el “nido” de la implantación, por esto esta fase se llama la fase
secretora. El cuerpo luteo sufre una regresión y caen los niveles de progesterona y estrógenos.
Lo que produce que el endometrio se encaja y deja de pasar sangre y toda esa zona se necrosa
y empezamos a perder todo ese tejido muerto y se elimina por la viajan en el periodo
menstrual.
HORMONAS OVÁRICAS.
Hay dos tipos:
- Estrógenos, el más importante estradiol (eliminado en la orina por el riñón)
- Progesterona, en la 2º mitad del ciclo coinciden con la fase lutea (examen)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Acciones de los estrógenos (producidas durante todo el ciclo)
1. Sensibilización los ovarios a gonadotrofinas es decir en los folículos aumenta también
los receptores de gonadotrofinas y así produce más síntesis de estrógenos (bloque de
alimentación)
2. Estimula el crecimiento del endometrio es decir aumenta la proliferación del
endometrio y estimula la contractibilidad de la pared uterina
3. Producción más fluido presente en la primera fase de ciclo ayuda en el aunque de las
espermatozoides.
4. Estimulan la proliferación epitelio vaginal
5. Aumenta el desarrollo de mamas, también durante la gestación
6. En los niños, aumenta el crecimiento en los niños y también promueve el cierre de la
epífisis
7. Favorecen en la conservación del hueso
8. Feed-back negativo y también estimula en un momento muy puntual el ciclo sobre la
adeno/hipófisis y/o hipotálamo.
Acciones de la progesterona (sólo en la 2º mitad del ciclo)
1. Transforma el endometrio en decidua (cargado de nutrientes) y muy importante
inhibe la contractibilidad del miometrio (del músculo) (ex). Inhibe las contracciones
uterinas.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
2. Estimula la producción de un mucus espeso en el cuello uterino la consistencia cambia,
gracias a la progesterona es más espeso. Impidiria el avanza de los espermatozoides
3. Regresión del epitelio vaginal
4. Más desarrollo de mamas
5. Aumento de la temperatura corporal (0,5 ºC aprox) en algunas mujeres es últil para
ver si ha producido ovulación o no.
La progesterona prepara al organismo para el embarazo.
CONTROL HORMONAL DEL CICLO REPRODUCTOR FEMENINO
Está bajo el control del eje hipotálamo / hipófisis, GnRH, se libera en forma de pulsos lo normal
es cada hora (liberación pulsátil) estimula la producción de la hormona folículo estimulante
(estimula la proliferación de los folículos) y luteinizante actúa sobre folículos y cuerpo luteo
estimulan la producción de hormonas.
A su vez estos estrógenos actúan sobre los folículos sensibilizando y produciendo las hormonas
en respuesta a gonadotrofinas. Además en los folículos se produce Inhibina (hormona
peptídica) ejerce una acción feed-back
negativa inhibiendo sobre toda la
producción de FSH, no tanto de LH. Los
estrógenos también ejercen la acción
de feed-back (exceso) inhibe la
producción de LH pero hay un aumento
de acido que los niveles elevados de
estrógenos producen un pico en la
secreción de LH, ese pico desencadena
la ovulación.
Al final del ciclo, se desinhibe la
adenohipofisis y sube FSH y LH está
aumenta de FSH es lo que hace que un
nuevo grupo de folículos empieza a
crecer en el nuevo ciclo.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ANTICONCEPCIÓN HORMONAL
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La píldora está formada
por una mezcla de
estrógenos y progesterona
sintéticos (los naturales no
resisten vía oral) en
cantidades adecuadas. Se
mantiene más niveles
estables de estrógenos, se
mantiene el pico de LH por
lo que no se anula y la
progesterona sintética
hace un moco espeso que
bloquea el paso de
espermatozoides (efecto
barrera)
INSUFICIENCIA OVÁRICA:
Causas de insuficiencia ovárica (hipoestrogenismo): situación patológica caracterizada por la
ausencia de ciclos ováricos, falta de función de los ovarios)
Primario: de origen ovárico por: ovaridectomía, agresión por radiación,
autoanticuerpos, fármacos disgenesis gonadal (Síndrome de Turner: XO)
Secundario/terciario: lesiones de hipófisis/hipotálamo, hiperprolactinemia, trastornos
funcionales hipotalámicos: anorexia, nerviosa, estrés.
Formas de hipogonadismo femenino:
Hipogonadismo prepuberal: amenorrea femenina: no aparece la menarquía. No se desarrollan
los caracteres sexuales primarios ni secundarios. Esterilidad por falta de ovulación. Talla
superior a la normal, con extremidades largas. Osteoporosis.
Hipogonadismo pospuberal: cesa la menstruación: amenorreas secundaria. Esterilidad por
falta de ovulación. Atrofia de genitales y mamas. Osteoporosis. La menopausia es un
hipogonadismo pospuberal.
Disgenesia gonodal: mujeres que nacen con el epitelio degenerado
Amenorrea: ausencia de menstruación. Será primaria si nunca ha habido menstruación. Será
secundaria si ya se ha menstruado antes (se considera cuando desaparece la menstruación
durante 6 meses).
La menopausia es un hipogonadismo pos puberal fisiológico.
HIPERgonadismo femenino (hiperestrogenismo): situación patológica por una secreción
anormal de estrógenos bien a nivel absoluto o relativo. Aceleran los cambios en la pubertad
precoz (por debajo de 5 años se considera anormal. Con el primario no se anula por lo que no
puede quedarse embarazada)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Causas de hiperestrogenismo:
Primario: tumores ováricos productos de estrógenos
Secundario: hiperestimulación por gonadotrofinas hipofisarias o ectópicas
Consecuencias del hiperestrogenismo
Pubertad precoz: en el secundario
Pseudopubertad: en el primario
Después de la pubertad:
Reglas irregulares
Ciclos anovulatorios. Esterilidad.
TEMA 22: FISIOLOGÍA DE LA
GESTACIÓN, EL PARTO Y LA
LACTANCIA
FECUNDACIÓN E IMPLANTACIÓN
Cuando se producía la ovulación, el ovario era recogido por las fimbrias y pasaba a las
trompas de Falopio. Este óvulo es viable durante aproximadamente unas 24horas. Sin
embargo, los espermatozoides son viables durante aproximadamente 3-5 días. Por lo tanto,
para que la fecundación sea viable los espermatozoides tienen que ser depositados unos pocos
días antes de la ovulación. El tiempo que los espermatozoides pasan en el tracto genital
femenino se denomina capacitación (para que alcancen su maduración). La fecundación
ocurre en la porción lateral más alejada del oviducto. Aproximadamente solo llegan tan lejos
unos 100 y de esos solo 1 puede fecundar. Para que se produzca la fecundación ese
espermatozoide va a atravesar las capas que rodean al óvulo y libera hialuronidasa y otras
enzimas en un proceso que se
denomina reacción acrosómica. Llegan
a la zona pelúcida donde hay
receptores de especia que impedirán la
fecundación por receptores de otra
especie. Y también liberan acrosina
cuando penetran en el óvulo. Ciertos
materiales van a liberarse y van a
impedir la entrada de nuevos
espermatozoides.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Una vez dentro, se unen dando lugar al cigoto que es diploide (23+23 = 46) que da lugar a la
célula del nuevo individuo. Y sería la primera célula del nuevo individuo que se va a desarrollar,
va viajando por la trompa de Falopio por el útero, para el tiempo en el que consigue entrara ya
en el útero han pasado 3 días y el cigoto ya es una masa de células llamada mórula. Cuando se
da el caso de gemelos idénticos ocurre porque la mórula se divide en dos por lo tanto serían
genéticamente idénticos ya que habría dos mórulas idénticas. En el caso de mellizos sería
cuando la mujer ovula 2 ovarios y irían dos espermatozoides diferentes.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Dicha mórula empieza a diferenciarse dando lugar a la blástula o blastocito, que es una
vesícula rellena de liquido. Las células de la parte externa de la blástula son llamadas células
trofoblasticas dan lugar a la placenta o trofoblasto.
Mientras que en la parte interna hay un acúmulo de células que dan lugar al embrión,
este acúmulo es llamado botón embrionario.
A la vez que esto tiene lugar, la
blástula ha entrado ya en el útero
y se produce ya la implantación,
es decir entra en la pared uterina.
Dicha implantación tiene lugar el
día 7 desupés de la fecundación,
todo ello gracias a la
progesterona que es producida
como ya vimos por el cuerpo
lúteo y el endometrio
previamente preparado. Se
produce gracias a la células trofoblásticas y van digiriendo las células del endometrio y van
haciéndose un hueco, sí recordamos, el endometrio estaba cargado de nutrientes, pues estos
nutrientes van a ser los primeros que van a utilizar el embrión para poder desarrollarse. De
hecho es la única fuente de nutrientes hasta que la placenta sea ya funcional.
Aproximadamente ya en el día 9, las células de la placenta empiezan a producir una hormona
llamada gonadotrofina coronica humana (HCG). Esta hormona pasa a la sangre y va al ovario y
va a mantener la vida media del cuerpo lúteo. Este paso es importante porque el cuerpo lúteo
tiene muy poca vida media, y podría producirse un aborto. Por lo tanto, con esta hormona lo
que conseguimos es que el cuerpo lúteo seguirá creciendo y va a ser la principal fuente de
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
hormonas. Luego ya este papel lo hace la placenta. Esto es crucial como ya hemos dicho, para
que no se pierda la pared del endometrio y no se produzca un aborto.
FUNCIONES DE LA
PLACENTA
La placenta permite la
supervivencia del feto. La
placenta es una especie de
disco de 18 cm de diámetro y
un peso de 1kg
aproximadamente. La placenta
se forma a partir de la capa
externa de la blástula que
forma el corion que es la capa
más externa de la placenta, la que rodea al embrión. Las otras membranas proceden del botón
embrionario, una es llamada acunios (más cerca, la que produce el líquido amniótico),
alantoides que se continúa con el cordón umbilical que permite la transmisión de la sangre y el
saco vitelino que degenera con el parto. Importante tener en cuenta que solo el corion
proviene de la placenta y las demás del botón embrionario.
En el corion se producen unas vellosidades coronicas, son ramificaciones que
contienen los vasos sanguíneos del feto y que están inmersas en la pared uterina rellenas de la
sangre materna. Mientras que la sangre del feto va dentro de las ramificaciones. De tal manera
que las células de la placenta que tapizan las vellosidades coronicas , separando la sangre fetal
y de la madre.
Funciones de la placenta:
1. Pulmón fetal. Ya que las células de la placenta permiten el intercambio de oxígeno y
CO2 entre los tejidos maternos y del feto. El oxígeno llega por difusión de la placenta
2. Intestino fetal. Del mismo modo, los nutrientes de la madre en la forma más sencilla
pasan a la sangre fetal.
3. Riñón fetal. Hay que eliminar los desechos de tejidos de embrión pasando a la sangre
materna.
4. Hace también de barrera inmunológica entre la madre y el feto. La sangre de la madre
y la del feto no puede estar en contacto porque generaría anticuerpos. También sirve
de protección de patógenos de la madre.
5. Función endocrina: en la placenta se producen hormonas para el éxito del embarazo.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
HORMONAS PLACENTARIAS
A nivel de la placenta se producen 4
hormonas:
1. Dos de ellas son peptídicas:
a. HCG
b. HCS
(somatomamotropina
corionica humana ó
también llamada
lactógeno placentario)
2. Y las otras dos, hormonas
esteroides:
a. Progesterona
b. Estrógenos (estradiol)
HCG: hormona peptídica, es una glicoproteína concretamente. Tanto estructural como
funcional se parece mucho a la LH. Los niveles de HCG son muy altos durante el primer
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
trimestre de la gestación y su papel es el mantenimiento del cuerpo lúteo para que no
degenere.
Como se forma a partir del día 9 y se elimina en orina, su detención en orina de dicha
hormona sirve como una prueba de embarazo. También es la que se usa en las
técnicas de reproducción asistida, se induce con la HCG.
HCS: esta hormona (producida por la placenta también) sus niveles aumentan
continuamente hasta el final de la gestación. Es más pequeña y es una proteína que se
parece a la hormona de crecimiento GH. No se sabe a ciencia cierta pero por un lado
esta hormona estimula el crecimiento en la vida fetal. Y en la madre lo que hace es
inducir resistencia a la insulina favoreciendo así que los nutrientes (glucosa) queden
para la utilización del feto, permitiendo por lo tanto su desarrollo. Además estimula el
desarrollo de las glándulas mamarias y las prepara para la lactancia.
Progesterona: en la mujer embarazada la progesterona presenta dos picos: uno de
ellos corresponde a la progesterona producía por el cuerpo lúteo y el segundo al de la
progesterona producida por la placenta.
La progesterona es crucial para mantener el endometrio y inhibir las contracciones
espontáneas del endometrio. (contracciones uterinas). También estimula el desarrollo
de glándulas mamarias y prepara para la lactancia.
Estradiol: van aumentando a medida que transcurre el embarazo. Permiten el
crecimiento uterino para acomodar al feto que cada vez es más grande. También
prepara para la lactancia.
Los niveles de estas hormonas caen bruscamente después del parto. La placenta no es capaz
de sintetizar estrógenos y tampoco de sintetizar sus precursores como la
dihidroepicondrasteroma, por lo que es necesaria la unidad feto-placentaria.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ADAPTACIÓN MATERNA AL EMBARAZO
Ganancia media de peso: 11 kg
(Aporte adicional de 300 kcal/día y 30g/día proteínas)
1º mitad de la gestación: ESTADO ANABÓLICO: durante el primer periodo se prepara ello para
subsistir las demandas que luego en el 2º estado requiere el feto.
o Sensibilidad a la insulina normal o elevada
o Niveles de glucosa, ácidos grasos libres y aminoácidos en plasma normales o bajos
(carbohidratos y proteínas de la dieta se utilizan rápidamente)
o Alta síntesis de proteínas, lípidos y glucógeno
La madre se prepara para resistir las demandas metabólicas finales del feto
2º mitad de la gestación: ESTADO CATABÓLICO: en este periodo todo lo que come va a pasar
al feto. La madre se vuelve resistente a la insulina, los tejidos humanos no la aprovechan pero
sin embargo el feto los va reteniendo.
o Resistencia a la insulina (inducida por el lactógeno placentario)
o Altos niveles postpandriales de glucosa y aminoácidos en plasma (los tejidos maternos
los utilizan mucho), que caen mucho durante el ayuno
o Glucosa y aminoácidos atraviesan la placenta hacia el feto
o Lipolisis incrementada (proporciona energía a madre y feto)
La madre está en “inanición acelerada”
PARTO
La duración del embarazo son 280 días = 40 semanas desde el inicio de la última menstruación,
es decir 38 semanas desde la fecundación (266 días).
El feto durante ese tiempo va creciendo y gracias a un cierto nivel de hormona progesterona
se inhibe las contracciones uterinas. Pero en un determinado periodo ya se producen
contracciones del endometrio (estiramiento que estimula la motilidad uterina
contracciones, dichas contracciones empiezan alrededor del octavo mes.
En la especie humana no se conocen las señales que desencadenan el parto: se sabe
que en la oveja vienen del cortisol fetal, desencadena el parto. Los niveles de cortisol
en el feto sube mucho las últimas semanas de la gestación en la especie humana. Es
importante también este aumento de cortisol porque ayuda a la maduración de los
pulmones fetales y tras el parto el feto pueda respirar con normalidad.
Los estrógenos están muy altos al final de la gestación, sensibilizan al miometro del
útero para que responda a la oxitocina (hormona peptídica, estimula la contracción
del miometrio).
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La oxitocina se libera al estar encajado el feto estira la pared uterina y ese
estiramiento es el que manda receptores de estiramiento y se libera la oxitocina y ya
se producen las contracciones uterinas y se
empuja el feto hacia fuera y eso manda más
señales y se produce más oxitocina y así se
forma un ciclo. Farmacológicamente, la
oxitocina induce el parto (pero NO lo
desencadena)
Otras hormonas son las prostaglandinas
producidas por la pared del útero, que
también ayudan a las contracciones. Estas
prostaglandinas están muy elevadas durante
el parto.
Relaxina: hormona peptídica que relaja el
canal del parto, por donde tiene que salir el
feto, es decir el cuello uterino, canal vaginal)
El PARTO se divide en 3 fases:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
1. FASE DE DILATACIÓN: la fase de dilatación cervical dura entre 6-12h, comprende esta
fase desde que se inician las contracciones coordinadas y hasta que se dilata el cérvix.
La mujer experimenta dolor y se cree que ese dolor viene por la hipoxia producida en
el miometrio.
2. FASE DE EXPULSIÓN DEL FETO: es más breve. Consiste en el paso del feto a través del
canal del pato. Esta fase es muy dolorosa. Después de la expulsión del feto no ha
terminado el parto, vendría la tercera fase.
3. FASE DE EXPULSIÓN DE LA PLACENTA: la expulsión de la placenta dura entre 10-40
min. Se desprende la placenta y se expulsa del cuerpo con una fuerte contracción y ya
queda finalizado el parto. Se produce una hemorragia entre 250 ml de sangre que se
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
controla por la propia contracción uterina y también ayuda a controlar dicha
hemorragia la prostaglandina.
Durante el siguiente mes, el peso del útero se va reduciendo. Un 50% se reduce en la
siguientes semana después al parto.
LACTANCIA
La mujer va a producir leche para el alimento del feto. Es importante no solo a nivel nutritivo
sino también porque lleva anticuerpos que ayuda a la protección inmunológica.
La leche se estimula por las glándulas mamarias, las células epiteliales son las que estimulan la
leche. Las células mioepiteliales rodean a los alveolos y al contraerse expulsan la leche hacia
los conductos y convergen
en el pezón. La salida de la
leche es un fenómeno
controlado por las
hormonas. Hay muchas
hormonas que controlan
esto. Durante la gestación,
todas las que suben sus
niveles estimulan las
glándulas mamarias.
(Estrógenos, progesterona,
prolactina… y otras).
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Cuando se produce la lactación las que intervienen son principalmente:
- La prolactina: estimula la producción de leche.
- La oxitocina: lo que hace es facilitar o permite la salida de la leche.
Contrae los músculos de las glándulas y “exprime” y así sale la leche.
El estímulo para que se instaure la lactancia, lo que se llama coloquialmente “para que baje la
leche” se tiene que producir la caída brusca
de niveles elevados de hormonas al perder la
placenta y tiene que subir la prolactina. La
prolactina sube al succionar el bebe en el
pezón. Esto es necesario porque con la
succión se estimulan los mecanorreceptores
en el hipotálamo y van a inhibir la dopamina y
al no llegar dopamina inhibidora se produce la
prolactina y así aumenta los niveles de
prolactina y se genera la leche. También con
este estímulo se libera la oxitocina así se
produce la contracción del musculo liso y sale
la leche. Esta misma succión también produce
la inhibición de la producción de
gonadotrofinas (LH y FSH) por eso durante la
lactancia no se ovula, ya que sí recordamos la
ovulación se producía por el pico de la LH.
TEMA 23: FISIOPATOLOGÍA DE LA
FECUNDACIÓN, LA GESTACIÓN Y EL PARTO
CAUSAS DE INFERTILIDAD
Femenina:
Ausencia de ovulación,
por:
- Hipersecreción de
gonadotrofinas
hipofisarias
- Anormalidades
anatómicas en el
ovario
- Síndrome de ovario
poliquístico (SOP)
Endometriosis
Salpingitis
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Secreción anormal de moco por el cuello del útero
Masculina:
Impotencia
Baja calidad del semen (número y motilidad de los espermatozoides):
- Anomalías genéticas
- Criptorquidia
- Varicocele
- Orquitis bilateral
- Traumatismo, procesos autoinmunes
- Fármacos, contaminantes ambientales
estrógenos, etc.
Recuento normal de espermatozoides: 100 millones/ml
semen
Oligospermia < 20 millones/ml = infertilidad
Azoospermia: ausencia de espermatozoides.
Se evalúa también su morfología y motilidad
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ALTERACIONES DE LA ADAPTACIÓN MATERNA AL EMBARAZO
TRASTORNOS EN LA GESTANTE
Los cambios en la gestante se producen de manera coordinada para lleva a cabo un correcto
crecimiento del feto. En ocasiones se ponen de manifiesto las enfermedades “latente”, son
mujeres que no tienen reserva nutricional durante la gestación
- Vómitos: ocurren en el 80% de lo cosas, sobre todo durante el primer mes de
embarazo. Estos vómitos son debidos a las alteraciones hormonales (náuseas, vómitos
en ayunas por la mañana…) Al segundo o tercer mes de gestación “suelen
desaparecer” pero hay casos en los que se intensifican produciéndose Hyperemsis
gravidarum con elevado riesgo de deshidratación.
Enfermedad matutina de la embarazada
Hyperemesis gravidarum
- Pirosis (por reflujo gastroesofágico): la pirosis o dicho de otra forma “ardor en el
estómago” se produce por reflujo gastroesofágico producido porque el aumento de
hormonas inhiben la contracción del musculo liso y inhibe el cardias del estómago por
lo que es fácil el reflujo y además hay una presión por el feto.
- Infecciones urinarias: también intervienen aquí la progesterona, que facilita el
movimiento de la orina hacia el riñón.
- Anemia: durante la gestación los niveles de demanda de hierro y ácido fólico son muy
altos por lo que es necesario dar suplementos para hacer frente e esas demandas.
- Descalcificaciones: el feto retira el calcio, por lo que si no se aporte en suficientes
cantidades se va a retirar de los huesos.
Problemas graves:
- Preeclamsia:
Hipertensión, edema y albuminuria (albúmina en orina). Deben aparecer estas
tres manifestaciones para que se dé el caso. No se sabe muy bien el porqué se
produce pero se cree que viene por problemas renales. Es una situación muy
grave, la cual si se complica provoca eclamsia.
- Eclamsia o toxemia gravídica
Hipertensión marcada, edema cerebral, convulsiones, coma (prácticamente
mortal)
- Trombosis venosa: en la mujer embarazada el potencial homeostático es alto, no es
infrecuente que se produzcan trombos, esos trombos se convierten en embolias que
van a alojarse en las arterias pulmonares. Caso raro.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
ABORTO: se entiende por aborto a la interrupción del embarazo antes de 28 semanas de
gestación. Después de las 28 semanas se considera nacidos muertos. Esto ocurre de manera
espontánea en el 20% de los embarazos y la mayoría durante la semana 8-13. Normalmente a
partir del 3º mes ya es raro. Un 50% de los cigotos no son viables, es decir hay casos que se
eliminan durante 4º, 5º, 6º semanas y la mujer no se entera de que está embarazada.
CAUSAS DE ABORTOS ESPONTÁNEOS: hay casos en los que los embarazos espontáneos
son repetidos, se considera que 3 abortos repetidos la posibilidad de tener hijos es baja. Las
causas van a depender bastante del momento:
Antes de que el embarazo sea aparente
Anormalidades fetales
Fase lútea insuficiente
Embarazo ectópico: cuando el embarazo se desarrolla en otro lugar que no sea
el útero. Ejemplo en las trompas de Falopio que puede llegar a reventarse y
producir una gran hemorragia peritonitis
Predominantemente en el primer trimestre
Anomalías cromosómicas (frecuentemente trisomías)
Función lútea insuficiente
Factores inmunológicos
Predominantemente en el segundo trimestre
Defectos anatómicos del útero
Incompetencia del cérvix
Predominantemente en el tercer trimestre
Desequilibrio de hormonas sexuales
Infecciones por vía ascendente (Corioamnionitis) o hemática. La
corioanmionits es la inflamación de las membranas que rodean al feto.
Enfermedades maternas
Hipertensión y cardiopatía
Lupus eritematoso sistemático
Diabetes mellitus
Hipotiroidismo e hipertiroidismo.
FISIOPATOLOGÍA DE LA PLACENTA
PRINCIPALES ALTERACIONES PLACENTARIAS.
Lo normal es que la placenta esté en la parte
alta del útero.
Trastornos en la placentación:
Lóbulos accesorios: no suelen dar
problemas en el embarazo pero sí en
el parto: hemorragias postparto.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Placenta bilobulada: 2 lóbulos, a medida que crece la pared uterina se puede dar
desgarro.
Placenta previa: placenta implantada en la parte baja del útero, impidiendo el parto
vaginal en te caso hay que hacer cesaría.
Hemorragia placentaria
Desprendimiento (abruptio placentae): desprendimiento de la placenta antes de tiempo.
Edema placentario
Infarto placentario
Corioamnionitis aguda: infección/inflamación ¿?
Alteraciones del cordón umbilical: lo normal es que el cordón salga del centro de la placenta,
pero se pueden dar casos que salga del lateral produciéndose desgarraduras. También hay
casos en los que el cordón umbilical es más largo produciéndose a veces enrollamiento del
cordón hipoxia en el feto.
Polihidramnios: cantidad elevada de líquido amniótico. Lo normal 1L. Se produce por obesidad
materna.
PARTO PREMATURO, RETRASADO Y PROLONGADO
Lo normal es 40 semanas = 280 días ± 7
PARTO PREMATURO: El que se presenta antes de las 37 semanas de gestación o cuando el
recién nacido pesa
menos de 2,5 kg
Las causas pueden ser
inducidas o causas
espontáneas.
La incompetencia del
cérvix se refiere a que
el cuello uterino no soporta el peso del feto. A veces hay que inducir el parto antes de tiempo
por diferentes causas como son: situaciones de Preeclamsia que ya hemos visto, también por
un crecimiento intrauterino retardado cuando se observa que el feto ha dejado de crecer.
PARTO RETRASADO: el parto no se presenta hasta las 42 semanas, cuando el feto ya suele
pesar 4 kg (12% de los recién nacidos son “postmaduros”)
Consecuencias para la madre:
Más molestias durante el parto y posibles desgarros
Consecuencias para el feto:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Insuficiencia placentaria (placenta senil) La placenta está programada para 38
semanas, pasadas esas semanas la placenta no será capaz de dar nutrientes y oxígeno
que necesita al feto. Menos supervivencia y mayor riesgo de cardiopatías congénitas y
de retraso intelectual.
PARTO PROLONGADO: el que se alarga más de 24 horas
Consecuencias para la madre:
Agotamiento (por las contracciones mantenidas),
Deshidratación (por pérdida de sudor y orina)
Mayor riesgo de infección, lesión uterina y hemorragia post-parto
Consecuencia para el feto:
Mayor sufrimiento (anoxia), riesgo de infección
Nota: el meconio es el contenido gástrico del feto, que cuando hay anoxia (sufrimiento fetal)
produce que defeque el feto y al romper aguas la madre, el contenido de las aguas presenta un
color verdoso.
TEMA 24: FISIOLOGÍA Y FISIOPATOLOGÍA DEL DESARROLLO DEL
ENVEJECIMIENTO
FISIOLOGÍA PRENATAL: ETAPAS
La vida prenatal en la especie humana es de 266 días/38 semanas. Se divide en 3 periodos:
1. Periodo germinativo: abarca las dos primeras semanas tras la fecundación. En el
botón embrionario empiezan a formarse las capas germinativas primordiales:
ectodermo, mesodermo y endodermo, que van a dar lugar a los órganos.
2. Periodo embrionario: periodo que abarca desde la 3º semana hasta la 8º semana de
embarazo. En este periodo se forman todos los sistemas y órganos organogénesis a
partir de las capas germinativas primordiales. El individuo en crecimiento se llama
embrión y en esta etapa el embrión es más susceptible.
En esta etapa por alteraciones pueden darse niños con carencia de extremidades,
denominado Amelia. También en torno a la 6º semana se producen los dedos de
manos y pies pudiendo dar lugar también a una
alteración. Además hay que destacar que la
exposición a ciertos fármacos produce a veces
afecciones al embrión. Como por ejemplo en el
caso de la talidomina en los años 50, afectando a la
teratogénesis (alteración en el desarrollo de niños)
3. Periodo fetal: es el último periodo que ya abarca
desde el tercer mes hasta el parto. En este periodo
el embrión se llama feto (recibe este nombre ya
cuando están todos los órganos formados). Se
desarrollan, crecen y maduran los diferentes
sistemas orgánicos.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
FISIOLOGÍA PRENATAL: CRECIMIENTO
El crecimiento de forma longitudinal en esta etapa
es rápido y marcado, ocurre a la 4º semana/8º
semana de gestación, ocurre de manera lineal. En la
parte media de la gestación el crecimiento es más
marcado. En cambio, el crecimiento en peso es más
marcado al final de la gestación que es donde se
producía el estado de catabolismo o inanición por
parte de la madre para suplementar las demandas
nutritivas del feto.
FISIOPATOLOGÍA DEL EMBRIÓN Y DEL FETO
CAUSAS DE ALTERACIONES FETALES O EMBRIONARIAS.
Hereditarias: alteraciones genéticas de origen materno o paterno
Alteraciones de las células germinales: que afectan a la dotación genética del embrión
Alteración durante el embarazo:
Tóxicos ambientales
Drogas y fármacos (talidomina)
Hormonas (niveles maternos altos de T3 afectan a tiroides fetal)
Infecciones (sobre todo víricas, como rubeola)
Inmunológicas. Anemia hemolítica por eritoblastosis
Desnutrición materna
Tabaquismo (por niveles elevados de CO en sangre materna)
Diabetes mellitus
Enfermedades cardíacas o pulmonares maternas.
FISIOLOGÍA PRENATAL: RESPIRACIÓN
Son las funciones placentarias las que
permiten el desarrollo del feto. El feto
depende de la lamenta para obtener oxígeno
y eliminar CO2. El CO2 es muy permeable y
puede difundir fácilmente por la membrana,
se forma por el metabolismo fetal y llega a
las arterias fetales y difunde a favor de
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
gradiente pasando a la sangre materna y se elimina por la respiración De la madre.
En cuanto al oxígeno, el oxigeno de la sangre materna llega al útero ya con una presión parcial
baja de 50mmHg y va a difundir hacia la sangre fetal por la vena umbilical con una presión
parcial de 30mmHg. Hay por lo tanto un gradiente de 20mmHg que es lo que permite la
difusión. Es una presión parcial baja pero se puede llevar a cabo dicha difusión por 3 factores
(favorecen que a pesar de la baja presión el feto tenga oxígeno):
1. Presencia mayoritaria de hemoglobina fetal: la Hb fetal tiene desplazada la curva de
disociación de oxigeno hacia la izquierda, eso significa que para la misma presión
parcial de oxígeno la hemoglobina
fetal es capaz de unir un 80% más
de oxigeno, es decir se satura más.
2. Elevada concentración de 2,3
difosfoglicerato en sangre materna
que facilita que se suelte el
oxigeno.
3. Mayor concentración de
hemoglobina en sangre fetal
4. Existencia de un doble efecto Borh.
El efecto Borh es la relación entre
el pH y la saturación del oxigeno
por parte de la Hb. Se establece un
doble efecto Borh:
a. Por un lato la sangre fetal debido a un aumento de pH se alcaliniza y aumenta
la afinidad del oxigeno por la Hb
b. En el caso de la madre, el CO2 del feto pasa a la madre y se produce una
disminución del pH por lo que se acidifica, disminuyendo la afinidad de la Hb
por el oxigeno y lo suelta y lo capta la Hb fetal que ha ganado el balance por
alcalinizarse.
Los pulmones no están funcionando,
están colapsados durante la gestación.
Es muy importante de que a partir del 7º
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
mes del pulmón fetal empiece a producir el agente tensioactivo que va a permitir la
respiración fetal después del parto. El cortisol es el que estimula la producción del agente
tensioactivo. Se suele dar glucocorticoides a la madre antes del parto.
FISIOLOGÍA PRENATAL: CIRCULACIÓN
Es el sistema que se forma primero, el corazón humano late en la 4º semana de fecundación
late unos 65 latidos/min pero esta frecuencia va aumentando y en el parto es de 140-160
latidos/min.
El sistema circulatorio es muy diferente al post natal porque el feto no está respirando por los
pulmones sino que respira por la placenta. De la aurícula derecha pasara la sangre al ventrículo
derecho e iría al pulmón pero en el feto la mayor parte de la sangre atraviesa el corazón a
través de un conducto llamado Foramen Oval que permite que la mitad de esa sangre pase a
la aurícula izquierda directamente y de ahí al ventrículo izquierdo. La circulación fetal esta
pensada para atravesar la sangre en la placenta.
FISIOLOGÍA PRENATAL: HEMATOPOYESIS
En el adulto el mayor órgano de células sanguíneas es la médula ósea. En el feto actúan otros
órganos como:
El saco vitelino (que degenera tras el parto) donde empiezan a producir las primeras
células sanguíneas del feto.
El hígado fetal que tiene la importante función de producir células sanguíneas, dicha
función desaparece tras el parto.
También otras como el bazo, tejidos linfoides.
ADAPTACIÓN A LA VIDA EXTRAUTERINA: RESPIRACIÓN
La compresión intermitente del tórax durante el parto expulsa el líquido que rellenaba
los conductos aéreos.
Las primeras inspiraciones aspiran al líquido restante y el aire hacia los alvéolos; se
forma la interfase aire-líquido
El surfactante pulmonar reduce la tensión superficial y disminuye la presión necesaria
para dilatara los alveolos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
La presión necesaria para expandir los pulmones no ventilados es mucho mayor que
cualquier otro momento de la vida.
A este esfuerzo ayuda el primer llanto del niño.
ADPATACIÓN A LA VIDA EXTRAUTERINA: CIRCULACIÓN
Es inmediato el cambio de circulación
fetal con la circulación extrauterina. El
cordón umbilical se corta y se “liga”.
Con el llanto del niño los pulmones se
llenan de aire facilitando que la
sangre pase fácilmente al pulmón. De
forma que pasa más cantidad de
sangre a la aurícula derecha y al VD y
de ahí a las arterias pulmonares y va a
regresar más sangre oxigenada de los
pulmones a la AI. Esta sangre empuja
a la válvula de Foramen Oval y así se
cierra funcionalmente y después
según pasan las semanas de vida del niño, el tejido se escinde y se cierra. Muchas veces si no
se cierra bien se produce un soplo.
ADAPTACIÓN A LA VIDA EXTRAUTERINA: METABOLISMO
Los sustratos metabólicos cambian mucho. En la vida prenatal, el feto se alimenta de
nutrientes digeridos por la madre, principalmente de glucosa y también de aminoácidos que
los quema para obtener energía o los utiliza como precursores para obtener otros. Al final de
la gestación se carga de glucosa en forma de glucógeno para reserva a la hora del nacimiento.
Una vez pasado el parto, se produce la lactancia que proporciona al niño de otra serie de
nutrientes diferentes. La lactancia tarda en comenzar, en ese periodo, denominado
prelactancia, el glucógeno almacenado por el hígado fetal se rompe para dar glucosa. Pero
además el feto se ha cargado de lactato y se utiliza como sustrato ya que el cerebro neonatal
es capaz de utilizar dicho lactato.
ADPATACIÓN VIDA EXTRAUTERINA: TERMORREGULACIÓN
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
También es importante mantener la temperatura corporal (termorregulación). El feto vive
dentro de la madre a una temperatura de 37ºC y en el momento del parto pasa a un ambiente
frío. En las primeras horas de vida se produce una caída importante de la temperatura que se
va recuperando a las 5-6h del nacimiento gracias a los sistemas de regulación. Es más difícil de
conseguir en los neonatos prematuros, es más difícil control la temperatura.
ADAPTACIÓN VIDA EXTRAUTERINA: F.GASTROINTESTINAL
Durante la vida fetal su nutrición ya hemos dicho que depende de la madre. Desde la semana
12 se empiezan a formar enzimas digestivas, y empieza así a formarse el meconio y luego más
tarde la orina. En la vida postnatal tienen una elevada actividad de lactosa por eso es capaz de
digerir la leche. Esta actividad va disminuyendo a lo largo de la vida. La secreción pancreática
no madura hasta el primero o segundo año de vida.
ADAPTACIÓN VIDA EXTRAUTERINA: FUNCIÓN HEPÁTICA.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
DESARROLLO SOMÁTICO POSTNATAL
Existen diferentes patrones de crecimiento a los que se ajustan los diferentes tejidos de los
órganos y cuerpo. La mayoría sigue el patrón general, con un crecimiento de vida hasta los 3-4
años elevado, a este tipo es el que se ajusta el tejido óseo, muscular… Luego hay otro
crecimiento más constante (6-8 años) y luego otra vez en la pubertad aumenta.
Otro patrón, es el patrón genital el cual no hay crecimiento en la infancia, la fase de
crecimiento brusca se produce en la pubertad.
En cuanto al patrón linfoide, el tejido linfoide sigue una pauta diferente aumenta mucho
aproximadamente 6 años y después se produce una involución (disminuye). Y por último la
tasa de crecimiento neural se da en los primeros años de vida.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Fisiología y Fisiopatología III
Curso 2015/2016
Celia Muñoz Hernández
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
TEMA 24: ORGANIZACIÓN ESTRUCTURAL Y FUNCIONAL DEL SISTEMA RESPIRATORIO.
1. Generalidades
Funciones del sistema respiratorio (proceso en el que se intercambia gases entre el organismo
y el medio. Aportar oxigeno y eliminar CO2)
- Intercambio de gases entre atmósfera y sangre
- Regulación del pH del organismo
- Protección frente a patógenos inhalados y sustancias irritantes
- Vocalización
- Pérdida de agua y de calor
Etapas del proceso respiratorio
1. Ventilación pulmonar: entrada y salida, entre atmósfera y alvéolos
2. Intercambio alveolar: difusión de gases entre alvéolos y sangre
3. Transporte de gases (O2 y CO2) por la sangre
4. Intercambio de gases entre sangre y células
Regulación
2. Estructura del aparato respiratorio
- Pulmones: superficie para el intercambio de O2 y CO2, grande (100m2), fina y húmeda
asociada a vasos sanguíneos.
- Vías respiratorias: sistema de conductos
- Caja torácica: bomba muscular para crear gradiente de presión
- El aire entra por las fosas nasales se humedece y se calienta, también ejercen la
función de filtración de partículas y producción de mucos.
- En una situación de exceso de ejercicio el aire entra por la boca y también se
humedece y se calienta pero no es tan eficaz y no tiene la función de filtración.
- Epiglotis: entre faringe y laringe. Se cierra durante la deglución evitando que los
alimentos pasen al aparato digestivo.
- Tráquea: tubo cuyas paredes están formadas por anillos cartilaginosos. Son
importantes para mantener abierto el paso del aire.
- Dentro del tórax se divide en 2 ramas llamadas bronquios y entra en los pulmones. Los
bronquios tienen una serie de ramificaciones hasta 23 divisiones, de las cuales, hasta
la 11 son bronquios y después de la 12 son los bronquiolos, que se diferencian en que
los bronquios tienen anillos cartilaginosos y los bronquiolos tienen pared lisa.
- Alveolo: especie de sacos llenos de aire. Se produce el intercambio de gases. Están
rodeados de fibras elásticas, que le dan la propiedad de distenderse cuando se llenan
de aire.
- Importante los capilares sanguíneos que llegan de la rama de vena pulmonar, lleva
sangre pero poco oxigenada. A medida que la sangre va saliendo ya está oxigenada y
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
se repartirá por todo el cuerpo. De las arterias bronquiolares llega sangre con oxígeno
al pulmón.
- Pulmones: sacos distensibles que ocupan la cavidad torácica. Y también son elásticos.
Ocupan casi toda la caja torácica.
Cada uno de los pulmones está rodeado por una membrana llamada pleura. De la cual
hay dos tipos: pleura pulmonar (en contacto con el pulmón) y pleura parietal (en
contacto con la pared) y entre ambas el espacio pleural que contiene una capa fina de
líquido y crea una superficie líquida deslizante.
- Líquido pleural: crea una superficie líquida deslizante. Mantiene el pulmón pegado a la
pared torácica. El pulmón se desliza con facilidad por el tórax.
- La caja torácica es más grande que los pulmones. Los pulmones no se colapsan,
siempre tienen aire dentro. Si se separan los dos membranas de la pleura se colapsan
(neumotórax)
Las costillas están unidas por los músculos intercostales. El diafragma separa el tórax
del abdomen. Cuando se contrae el diafragma aumenta la capacidad torácica.
3. Mecánica de la ventilación pulmonar
Proceso rítmico, que consiste en la inspiración seguida de la espiración. Las fuerzas que rigen
este proceso es el gradiente de presión
1º Inspiración. Es un proceso activo pues requiere de la contracción activa de los músculos. Y
se consigue contrayendo el diafragma y los músculos intercostales internos.
Para conseguir los cambios de presión modificamos el volumen de la caja torácica
2º Espiración. Es un proceso pasivo. Cuando se relajan los músculos el volumen disminuye y el
aire sale del pulmón.
- Sí queremos forzar la inspiración ya se utilizan los otros músculos a parte del
diafragma, eleva el esternón aumentado la caja torácica. En una espiración forzada
requiere de la participación de intercostales internos y musculo abdominales.
- Dentro de la pleura hay una presión negativa pues que la presión intra y extra están
equivalente pero en la pleura no por eso se crea una presión negativa.
4. Volúmenes y capacidades pulmonares, espirometría
Espirómetro: registra el volumen de aire que entra y sale de los pulmones durante la
respiración.
Volúmenes pulmonares:
- Volumen de ventilación pulmonar (VVP), volumen respiratorio o volumen corriente =
volumen de aire inspirado o espirado en cada respiración normal (0,5L)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Volumen de reserva inspiratoria (VRI) = volumen de aire extra que puede ser
inspirado en una inspiración forzada (3L)
- Volumen de reserva espiratoria (VRE) = volumen de aire extra que puede ser espirado
en una espiración forzada (1L)
- Volumen residual (VR) = volumen de aire que queda en los pulmones tras una
espiración forzada (1,5L) (no se puede medir por el espirómetro)
Capacidades pulmonares: combinación de dos o más volúmenes pulmonares. Son cálculos
matemáticos
1. Capacidad inspiratoria = VVP + V Reserva Inspiratoria (3,5L)
2. Capacidad funcional residual = V Reserva Espiratoria + V Residual (2,5L)
3. Capacidad vital = V Reserva Inspiratoria + V Reserva Espiratoria + VVP (4,5L)
4. Capacidad pulmonar total (CPT) = Capacidad Vital + V Residual (6L)
Factores que modifican los volúmenes y capacidades pulmonares
- Distensibilidad: capacidad de los pulmones de expandirse
- Elasticidad: capacidad de expandirse cuando se aplica una tensión y recuperar el
volumen inicial cuando desaparece esa tensión
- Resistencia de las vías aéreas al flujo de aire
TEMA 25. INTERCAMBIO Y TRANSPORTE DE GASES
Etapas del proceso respiratorio:
1. Ventilación pulmonar: entrada y salida de aire, entre la atmósfera y alvéolos.
2. Intercambio alveolar: difusión de gases entre alvéolos y sangre.
3. Transporte de gases (O2 y CO2) por la sangre.
4. Intercambio de gases entre sangre y células.
Regulación
1. La membrana respiratoria
Para difundir una molécula entre el capilar y el espacio tiene que pasar varias capas:
1. Capa surfactante
2. Después las células del epitelio alveolar, son células del tipo 1
3. Membranas fusionales que son membranas con un grosor pequeño (menos de 1mn)
facilita mucho la difusión y además es grande.
a. Membrana basal del epitelio
b. Espacio intersticial
c. Membrana basal del capilar
Están muy juntas y fusionadas
Surfactante pulmonar, también llamado líquido tensioactivo (primera capa) tiene varias
funciones:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Reducir la tensión superficial
- Impedir que los alvéolos pequeños se colapsen
- Facilitar la inspiración
2. Difusión de gases respiratorios en los alvéolos
Difusión de un gas
El intercambio se produce a favor
D = AP x C x A/T
D: capacidad de difusión del gas
AP: gradiente de P parciales
C: coeficiente de difusión del gas
A: área de difusión
T: espesor de la membrana
Intercambio de O2 entre el alvéolo y la sangre
Intercambio de CO2 entre el alvéolo y la sangre
El gradiente de presión es 60mmHg favorece que el O2 pase del aire alveolar a la sangre.
Cuando la sangre arterial ya sale oxigenada la presión de la sangre se iguala, ya es de
100mmHg.
Aquí también hay un AP pero es muy pequeño es de solo 6mmHg. Es suficiente porque C
(coeficiente del CO2) es 20 veces más mayor que en el O2. Por lo que es suficiente para que
aquí le sobre capilar.
3. Intercambio de gases entre sangre y tejidos
Primero viene la sangre arterial oxigenada y se reporta por los tejidos, llega a los tejidos y baja
la presión porque las células consumen cede O2 a las células. Y cuando sale la sangre
venosa se ha equilibrado. Llega al alveolo para volver a oxigenarse
4. Transporte de O2 en la sangre
- 97% unidos a la Hb el oxígeno
- 3% disuelto en el plasma el oxígeno
La hemoglobina es una proteína formada por cuatro subunidades que a su vez está formada
por un grupo hemo, formado por una protoporfirina que tiene un ión central Fe2+, que es
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
capaz de unirse reversiblemente a un átomo de 02, por lo que una molécula completa de Hb
puede transportar hasta cuatro átomos de O2
Fe2+ = O2
1mol Hb = 4 mol 02
1gHb = 1.34 mol 02
La Hb unida al oxígeno se denomina oxihemoglobina. 15g/Hb/100mL 20mL 02 /100Ml
Curva de disociación oxígeno-hemoglobina
En los tejidos un 75% de O2 se despresen para que pase a los tejidos. La Hb está prácticamente
saturada 97% de saturación, es decir toda la Hb está cargada de 02.
La cantidad de O2 que puede transportar la Hb va a ser función de la presión parcial de O2 en
sangre. La relación es sigmoidal cuando aumenta la presión de O2 no aumenta más la
saturación de Hb. Debido a un fenómeno cooperativo, cuando se une a un primer átomo de
oxigeno facilita la unión a un segundo.
Sí la curva se desplaza a la izquierda se produce un aumento de la afinidad de la Hb por el O2.
Un desplazamiento hacia la derecha implica que la Hb pierde afinidad por el O2. Se suelta más
fácilmente. En cuanto a la presión, hacía la izquierda, aumenta la afinidad para la misma P02 la
saturación es mayor, mas afinidad para aceptar.
Efecto del CO2 (efecto de Bohr): los niveles de CO2 aumentan la curva se desplaza hacia la
derecha. Además cuando aumenta la presión parcial del CO2 se produce ácido (se producen H+)
por lo que el ph disminuye. Ambos casos hacen que la curva se desplace hacia la derecha.
Los factores que modifican son: efecto del ph y efecto del CO2
Efecto de la temperatura: La caída de la temperatura hace que se transporte a la izquierda.
Una subida de la temperatura hace que se transporte la curva hacia la derecha.
Efecto de la concentración de 2,3 difosfoglicerato: cuando aumenta la 2,3 difosfoglicerato la
curva se desplaza hacia la derecha. En los tejidos hay mucha producción de 2,3
difosfoglicerato. Cuando disminuye la 2,3 difosfoglicerato se desplaza hacia la izquierda. Todos
los factores juntos desplazan la curva hacia la derecha, es decir que se suelte más fácilmente el
oxigeno de la Hb y así puede utilizarse
El monóxido de carbono tiene más afinidad que el oxigeno para unirse a la Hb. De tal manera
que se combina con la Hb formando carboxihemoglobina, por lo que no se pueden oxigenar
los tejidos (hipoxia)
3 mecanismos:
1. Disuelto en plasma (5-7%)
2. Como bicarbonato (70-80%) sucede en el interior del GR porque tiene una enzima:
anhidrasa carbónica (cataliza la reacción) por eso se hace rápidamente en el interior
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
del GR. El bicarbonato sale del plasma. Los H+ que se forman se neutralizan porque se
van a la Hb. La Hb es buen amortiguador de ph
3. Como compuesto carbamínicos (10-15%) el CO2 reaccionar con los grupos amino de las
proteínas y se forman carbaminohemoglobina es una unión débil.
En los alveolos todos las reacciones se revierten, para que el CO2 se pueda eliminar, se libera
CO2 por lo tanto.
Curva de disociación del CO2
Representa la cantidad de CO2 transportado en la sangre en función de la presión parcial de
CO2 . Efecto del O2 EFECTO HALDANE: efecto del oxígeno sobre el transporte de CO2. Cuanto
más aumente la presión del CO2 más CO2 se puede transportar (lineal) pero también influye el
oxígeno, de manera que al disminuir la presión del oxígeno el transporte de CO2 está
favorecido porque la Hb reducida se forma más carbaminicos y también puede unirse más a
los protones. Esto facilita el transporte de CO2.
TEMA 26: REGULACIÓN DE LA RESPIRACIÓN
1. Receptores, vías y efectores
La respiración es un proceso automático, es un efecto inconsciente. Está controlado por el SN
central, trata de mantener los niveles de pO2, CO2 y pH dentro de los límites, y mantener esos
niveles en todas las situaciones, para ello habrá una serie de estructuras que mandan la
información a las células. De tal manera que se estimule o se reprima la respiración para que
estén dentro de los límites.
Receptores
1. Quimiorreceptores, son los más importantes, detectan cambios en pO2 y pH y la
sangre. Pueden ser:
1. Periféricos: cuerpos carotideos y aórticos (arteriales) bajo pO2 se activan
arterial
2. Centrales: área quimiosensible del bulbo (al lado de los centros de control)
aumenta pCO2 se activan y cuando baja pH
2. Receptores de estiramiento pulmonares (mecanorreceptores). Músculo liso de
bronquios y bronquiolos que responden al estiramiento.
3. Barorreceptores (receptores de presión) en senos carotídeos y en el arco aórtico. Si
hay mucha hipertensión se activan
4. Otros receptores: de temperatura, de sustancias irritantes (tos, estornudos), etc..
estimulan la frecuencia respiratoria
Vía aferente: es el nervio vago en los receptores periféricos y en el estiramiento pulmonar.
Vías eferentes: son fundamentales en:
- Nervio frénico que inerva al diafragma
- Nervios intercostales que inerva a los músculos intercostales externo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Una vez que los receptores manden la señal al centro de control van al músculo
respiratorio. Cuando viajan potenciales de acción provocan la contracción del diafragma y
de los músculos intercostales externos se produce la inspiración.
2. Centros respiratorios
Están situados en el tronco encefálico, son grupos de neurona que están en el bulbo raquídeo
y protuberancia (centro respiratorio 2º)
- Área inspiratoria: parte detrás del bulbo
- Área espiratoria: en la parte -¿?
- Centro neumotáxico: parte alta de la protuberancia
- Centro apnéustico: parte baja de la protuberancia
3. Origen del ritmo respiratorio
El ritmo respiratorio se origina en el área inspiratorio del bulbo raquídeo en el grupo
inspiratorio dorsal que es el más importante para la regulación inspiratoria.
El área inspiratoria (GRD) es la más importante en la regulación del ritmo. La estimulación de
sus neuronas origina siempre inspiración. El origen del ritmo no se conoce bien, el origen de la
señal es espontánea (se activan neuronas que mandan potenciales de acción). También de
manera espontánea las neuronas cesan de manera que se forma la inspiración.
Los receptores de estiramiento pulmonares se activan cuando la respiración es muy forzada,
cuando se hinchan mucho los pulmones. Mandan señales al área inspiratoria de manera que
cese para impedir el daño en las paredes respiratorias. Se activa el Reflejo de Hering-Breuer:
reflejo protector, para impedir que el pulmón se hinche en exceso. En una respiración normal
este reflejo no se pone en marcha.
- El centro neuomotáxico tiene acción inhibitoria de tal forma que manda señales
inhibitorias de tal manera que cortamos por ahí la expiración dura más tiempo, pero el
ritmo se mantiene.
- El área espiratoria (GRV) interviene en la expiración forzada
- El área neumotáxica limita la duración de la inspiración (pero el ritmo se mantiene)
- El área apnéustica no se conoce bien el papel que realiza, estimula más la inspiración.
Están conectadas con los músculos intersticiales internas, que se contraen en una
espiración forzada.
4. Control químico de la respiración
Si la presión CO2 sube hay que estimular la ventilación. Mantiene estos niveles de CO2 dentro
de unos límites por los quimiorreceptores.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Los quimiorreceptores centrales se activan cuando se produce un aumento CO2 , baja el pH y
la concentración de protones aumenta. Los protones no atraviesan la barrera
hematoencefálica pero el CO2 sí. De manera que se forma HCO3 y H+ y estos protones son lo
que estimulan el quimiorreceptor central que estimula la ventilación y eliminamos el CO2 en
sangre.
Quimiorreceptores periféricos (cuerpos carotideos y cuerpos aórticos). Cuando la pO2 de los
cuerpos carotideos y cuerpos aórticos cae un 40% se estimulan los quimiorreceptores
periféricos y estimulan las neuronas del área inspiratoria.
5. Control voluntario de la respiración
Se puede controlar también desde el sistema límbico, puede controlar también el ritmo
respiratorio. Ejemplo: las emociones pueden modificar el patrón respiratorio. Cuando
mantenemos la respiración la sangre se carga de CO2 y llega un momento en el que
sobrepasan un punto límite, superan a la señal inhibitoria consciente, porque el
quimiorreceptor central a detectado el punto límite.
6. Otros reflejos respiratorios
Receptores de sustancias irritantes
- Tós: se produce irritación de vías aéreas y manda una señal al bulbo
1. Inspiración profunda
2. Cierre de epiglotis inmediatamente
3. Aire aprisionado sale con fuerza
- Estornudo: irritación de fosas nasales, ocurren los mismos pasos descritos
anteriormente.
- Bostezo: cuando se empobrece en 02 la sangre arterial.
En general son reflejos protectores donde se va a intentar eliminar material extraño e irritante.
La capa de moco retiene cosas que inhalamos. El movimiento de los cilios permite que esas
partículas salgan al exterior.
TEMA 29: ORGANIZACIÓN ESTRUCTURAL Y FUNCIONAL DEL SISTEMA DIGESTIVO.
1. Generalidades
La mayoría de los alimentos que ingerimos hay que procesarlos primero convirtiéndolos en
moléculas más sencillas para que sean metabolizados y sean absorbidos. Este proceso se
llamada digestión.
El músculo de tubo digestivo hace avanzar el bolo alimenticio y una vez procesado en
estomago (quimo) le hace avanza en tubo y lo mezcla con secreciones digestivas. El proceso
empieza en la boca, se mezcla con saliva (con amilasas que empiezan la digestión de almidón
en boca). El bolo pasa a jugo gástrico formado por HCl y pepsinas y luego pasa a duodeno
(intestino) el quino absorbe nutrientes del intestino delgado. El material que no se absorba
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
pasa a intestino grueso y riñón pero si se absorbe agua, sal y vitaminas. Los materiales que no
se absorben pasan a recto en forma de heces y se expulsan en defecación.
La función del aparato digestivo: digerir alimentos y absorber nutrientes. El sistema
gastrointestinal formado por tubo digestivo y glándulas anejas (próximas) donde se producen
secreciones que activan luego el tubo digestivo (glándulas salivales, hígado y páncreas)
2. Estructura del tracto digestivo
La estructura del tubo digestivo varia de una zona a otra pero la organización es constante. El
músculo de la pared del tubo digestivo es estriado (esquelético) en boca, faringe, esófago y
ano (en principio y fin). En el resto es musculatura lisa (la mayoría del tubo por tanto) que
tienen las capas de dentro a afuera.
Capas de dentro afuera:
1. Mucosa: células epiteliales especializadas que están sobre una lámina propia. En zona
con mucha abrasión (boca/ano) formada por 10-15 capas de células. La superficie de
absorción está facilitada por vellosidades. Muscularis mucosa: músculo de la mucosa
entre mucosa y capa submucosa. Su contracción regula el plegamiento de la mucosa.
2. Submucosa: formado por tejido conectivo laxo por donde circulan vías sanguíneas y
nervios. Formado por colágeno y elastina. Rica en glándulas.
3. Músculo circular (músculo circular + músculo longitudinal = músculo liso)
4. Músculo longitudinal cuando se contrae acortará el musculo. Es la muscularis externa.
Al contraerse interviene en los movimientos peristálticos.
5. Serosa o adventicia. Última capa es de tejido conectivo. Capa de tejido conectivo que
sigue con el mesenterio (mantiene unido el tubo digestivo con pared intestinal)
El sistema digestivo en la pared hay un sistema intrínseco que se llama S.N.entérico intestinal y
va de esófago a ano formado por neurona organizado en 2 plexos (plexo externo: mioentérico
de Auerbach y plexo submucoso o de Meissner) que están bajo el control del SNVS y SNV-PS.
- Placa de Peyer: acumulos de tejido linfoide acumulado en mucosa.
- Plexo mioentérico de Auerbach: capa muscular entre musculo liso circular y
longitudinal. Controla la motilidad del tubo digestivo.
- Plexo submucoso de Meissner: plexo neuronal que controla las secreciones y la
circulación sanguínea local.
Hay un sistema intrínseco con células inmune que protegen el organismo destruyendo
microorganismos patógenos y produce anticuerpos frente a antígenos alimentarios. Es un
sistema inmune. Están en los ganglios linfáticos mesentéricos ó placa de Peyer.
- Lamina propia: tejido conectivo laxo, contiene colágeno y elastina y es rica en
glándulas. Destacan los capilares sanguíneos y linfoides.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
3. Regulación de la función digestiva
Regulación nerviosa.
- A nivel intrínseco: llevada a cabo dentro de la propia pared por reflejos locales va
haber una serie de receptores, como barorreceptores y mecanorreceptores que
responden a la estriación, mandan señales a los plexos que van hacer sinapsis con las
neuronas, que van a regular, van a mandar órdenes a:
Musculatura
Células exocrinas
Células endocrinas (secreciones digestivas)
Vasos sanguíneos
Los neurotransmisores son adrenalina, noradrenalina, serotonina y otros
también que son péptidos como: CCK, somastostatina, sustancia P, ViP.
Sobre esta regulación se impone una regulación global que se va a llevar a cabo por el SN
vegetativo, van a esplácnicos y vagales hasta SNC y se mandan órdenes eferentes tanto al
simpático como al parasimpático.
- Parasimpático: estimular la motilidad y estimular las secreciones son excitatorias, son
ramas del nervio vago que producen acetilcolina (son colinérgicos) y hace sinapsis en
musculatura, células exocrinas, células endocrinas, vasos sanguíneos… o bien más
frecuentemente en las neuronas de los plexos entéricos, estimulan la motilidad.
- Simpática: Van a ser ordenes inhibitorias, inhiben motilidad y secreciones. Pero en
algunos casos hacen que se cierran y se abren esfínteres. Son neuronas adrenérgicas
van hacer hacer sinapsis con los nervios de los plexos entéricos, liberan noradrenalina
normalmente.
Si suprimimos en un animal la parte intrínseca, en unos días se recupera la motilidad y la
normalidad (puede actuar por si mismo). El control intrínseco puede ser suficiente.
Regulación hormonal
Se realiza en gran medida a nivel local va a ser una regulación paracrina, se produce hormonas
en glándulas situadas en la mucosa y submucosa del estomago y intestino y se liberan a la
sangre y llegan a la zona próxima de la pared muscular (musculo liso o musculo de la vesícula
biliar) controlando la motilidad y a las células de las secreciones digestivas, se trata de un nivel
local.
El control endocrino es más lento pero es más duradera que el nervioso que es más. La
motilidad está más bajo control nervioso mientras que las digestiones (secreciones) más
controlado en hormonal
4. Hormonas gastrointestinales
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Localización de las células Hormona
productoras
Estómago Gastrina
Somatostatina
Duodeno y/o yeyuno Secretina
Colecistokinina pancreozimina (CCK-PZ)
Motilina
Péptido inhibidor gástrico
Somatostatina
Páncreas Insulina
Glucagón
Polipétido pancreático
Somastostatina
Íleon y/o colon Enteroglucagón
Péptido YY
Neurotensina
Somatostatina
TEMA 30. MOTILIDAD GASTROINTESTINAL
1. Motilidad del tubo digestivo
La función de los movimientos digestivos es doble:
- Primero hacer avanzar el bolo para ello se utilizan los movimientos peristálticos o
movimientos de propulsión
- Segunda función, una función de mezcla. Mezclar el contenido digestivo del tubo y
facilitar que los nutrientes se pongan en contacto con la pared del tubo para favorecer
la absorción del tubo. Para ello hay contracciones covalentes pero no hay avance neto
del bolo.
2. Masticación
Los movimientos de masticación van a romper y reducir el tamaño de los alimentos y
mezclarlos con la saliva. Las enzimas digestivas actúan sobre la superficie de las partículas, esta
acción de cortar, rompe los alimentos más favorecidos luego la digestión, luego se mezclan con
la saliva y también ayuda.
También favorece que percibamos el sabor de los alimentos y también facilita mucho la
deglución, es decir el “tragar” el bolo alimenticio. La masticación consiste en combinar con los
incisivos y caninos (corte) y la acción de los premolares y molares. Es bajo control voluntario y
lleva a cabo por el coordinado movimiento de las mejillas, masticar (cerrado por acción refleja,
y por presencia de alimento en la boca hace que caiga al masticar, que inicia una contracción
de reflejo de fracción de sentido contario) y labios. Y de manera sucesiva es lo que produce la
masticación (activación e inactivación alternada de los músculos molares)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
El ritmo y la fuerza de masticación se controlan de manera refleja. Y son reflejos unilaterales,
de tal manera que hacemos más fuerza del lado de la boca con comida.
3. Deglución
La deglución es el paso del bolo desde la boca al esófago y de este al estómago es un proceso
complejo porque para pasar por esa zona el bolo tiene que pasar por la faringe, entonces tiene
que producirse sin interferir en la respiración. La deglución está controlada de manera refleja,
reflejo de deglución, de la cual tenemos 3 fases de las cuales solo la primera es voluntaria. El
resto es un reflejo que lo controla el centro de la regulación (entre bulbo y protuberancia)
La primera fase es la fase voluntaria y empieza cuando el alimento está listo se comprime
hacia atrás y para eso aplicamos la lengua sobre el paladar de manera que empuja el bolo
hacía la faringe, es involuntario y normalmente no se puede detener una vez que a llegado a la
parte atrás de la boca.
La segunda fase es involuntaria, pasó del bolo esta atrás de la boca activo receptores que
inician el reflejo de la boca de tal manera que:
- Se eleva el paladar blando para cerrar la nasofaringe de manera que el alimento no
vaya a las fosas nasales.
También se eleva la faringe para que se tengan las cuerdas nasales
- Además el bolo, empuja la epiglotis en el sentido que se cierra la tráquea, así evitamos
el paso del bolo al aparato respiratorio
- Se abre el esfinge esofágico superior, normalmente está cerrado, se abre en esta fase
para que pase al bulbo
También se forma una contracción una onda en la musculatura de la faringe, empuja el bolo
hacia el esófago. Todo esto ocurre en 1 o 2 seg, y durante esta fase inhibe la respiración.
4. Motilidad del esófago (motilidad isofágica)
Coincide con la tercera fase. El bolo alimenticio pasa por el esófago al estomago atravesando el
cardias. La musculatura del esófago en el primero tercio está formada por el músculo estriado
mientras que el segundo es musculo liso en medio coexisten ambos tipos de músculo, tanto
uno como otro están bajo control del nervio vago, que estimula la motilidad esofágica. Sí se
corta el vago, el esófago recupera su motilidad, porque tiene el SN entérico. En el estomago
existen dos tipos de movimientos peristálticos:
- Peristaltismo primario: es la onda peristáltica iniciada en la faringe durante la segunda
fase de deglución que se continúa con la musculatura del esófago. Aproximadamente
esa onda tarda entre 8-10 seg en recorrer el esófago.
- Sí después siguen quedando restos, la distensión de las paredes por ese residuo se
produce el peristaltismo secundario, que es similar a la onda primera pero de origen
esofágico. Y se producen nuevas ondas hasta que el esófago quede totalmente vacío.
Normalmente el cardias está cerrado para evitar el reflujo de ácido (jugo gástrico).
Después de la deglución (2-3 seg) el cardias se abre y permanece abierto.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
5. Motilidad gástrica
El estómago tiene una triple función motora, almacena grandes cantidades de alimento hasta
enviarlo al duodeno. La segunda función consiste en la ezcla de alimentos con jugo gástrico
hasta formar una papilla lechosa que es lo que llamamos QUIMO.
La tercera función es vaciarse progresivamente, permitiendo el paso del quimo al duadeno, de
una manera moderada para que se complete bien la digestión
El cardias y píloro esfínteres delimitan el estómago. El volumen que tiene es de 50mL, el
musculo liso de sus paredes tiene pocas contracciones. Cuando empezamos a comer las
contracciones del esófago pone en marcha un reflejo, que es un reflejo vagal, que pone en
marcha la relajación receptiva, que como son muy elásticas permite acumular el alimento sin
que alter la presión intragastrica, contracciones de la pared que mezcla los alimentos con el
jugo gástrico. Esas contracciones avanzan hacía el píloro formado anillo de contracción que
avanza acercando el quimo hacia el píloro hacia el duodeno pero solo llega una pequeña
cantidad, el resto rebota y mueve hacia atrás.
Esas ondas de contracción son miógenos, se producen en la propia pared del estómago. Las
contracciones de hombre cuando el estómago va acompañado de periodos de hambre.
Control de la motilidad y vaciamiento gástrico
1. Señales procedentes del estómago (estimulan la motilidad y el vaciamiento)
Nerviosas: distensión nervio vago
Hormonales: gastrina se libera en las células G y por los capilares llega
a la musculatura
2. Señales procedente del duodeno (inhiben la motilidad y vaciamiento)
Nerviosas: distensión reflejo gastroentérico (se ha estirado
demasiado el duodeno)
Hormonales: CCK-PZ, secretina, PIG
Importante tener en cuenta que predomina el control inhibidor duodenal: el objetivo es que el
quimo entre en el duodeno a la velocidad que puede ser procesado. El quimo entra poco a
poco en el duodeno para que pueda ser procesado adecuadamente. Puesto que el duodeno no
se puede aumentar la pared sin que aumente la presión.
6. Motilidad del intestino delgado
En este paso se juntan con bilis y jugo pancreático y ponerlo en contacto con nutrientes y
terminar la digestión y hacer avanzar el quimo a lo largo del intestino
- Movimientos peristálticos: son los movimientos peristálticos ya descritos
anteriormente.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Movimientos de segmentación: consisten en una contracción de segmentos amplios
del intestino que contraen y a continuación esos se relajan y los de al lado que no se
habían contraído se contraen mientras las otras se relajan.
Control de la motilidad del intestino delgado:
1. Control nervioso:
- Intrínseco: plexo mioentérico (reflejo mioentérico) el propio estiramiento de la pared
del intestino produce el reflejo mioentérico
- Extríseco: SNV-PS (+) y SNV-S (-)
Reflejo inhibidor entero-entérico: la distensión de un segmento
intestinal inhibe todo el intestino.
Reflejo ano-intestinal inhibitorio: la distensión del ano causa
inhibición intestinal.
Reflejo gastro-intestinal: el alimento que entra en el estómago excita
la motilidad intestinal.
2. Control hormonal: CCK-PZ(+) (se libera en presencia de grasas. En este caso
estimula la motilidad del intestino delgado)
7. Motilidad del colon
Para pasar del íleon al ciego los alimentos tienen que atraviesan el esfínter ileocecal, pero las
contracciones peristálticas van a relajar ese esfínter (reduce la presión) hay un reflejo
gastroileal, que consiste que cuando sale del estómago la válvula ileocecal se abre. En el colon
hay una absorción de agua de manera que el quimo se va compactando, convirtiéndose en las
heces. La motilidad es similar al intestino delgado pero el colon es más lento. De hecho el
colon la mayor parte del tiempo está inactivado hay tres tipos de movimientos en el colon
- Movimiento peristálticos
- Movimientos de segmentación
- Y contracción por acción masiva (solo en el colon) se contraen simultáneamente
amplias zonas del colon y esa empuja el contenido de esa zona a la porción siguiente y
así sucesivamente hasta llegar al recto. Ocurren 2 o 3 veces al día
8. Defecación
La mayor parte del tiempo el recto está vacío de heces y está cerrado gracias al esfínter anal
que tiene 2 partes el interno (músculo liso) y el externo (musculo estriado). El externo esa
controlado por el nervio pudiendo de modo que podemos contraerlo o relajarlo de manera
voluntaria. La distensión de las paredes del recto inicia contracciones reflejas, relajan el medio
interno (esfínter interno) y inicial la sensación de defecar. Se siente cuando la presión en el
esfínter anal es 18mmHg pero podemos inhibirlo por voluntad, no para siempre. Cuando la
presión en el esfínter supera >55mHg se produce ya el reflejo de evacuación rectal en la que se
relaja el esfínter anal externo y se vacía.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Previo a la defecación se produce una inspiración profunda, se aumenta la presión torácica, en
la cual se cierra la glotis.
TEMA 31: TRASTORNOS DE LA MOTILIDAD DEL TUBO DIGESTIVO
1. Trastornos de la deglución y el esófago
DISFAGIA
Def.: síntoma que se define como la dificultad para la deglución, sensación de detección del
bolo alimenticio desde la boca al estómago.
Odinofagia: es el dolor de la deglución. Y no tiene porque ir junto con la disfagia.
Causas de disfagia
Estenosis (estrechamiento y obstrucción) Afecta primero a la deglución de sólidos y si se
intensifica a los lípidos.
- Intraluminal: obstáculo dentro
- Parietal: de la propia pared
- Extraparietal: desde fuera.
Disfunción motora
- De origen nervioso (neuropático)
o espasmo esofágico difuso idiopático : contracción potente y sostenida que
interrumpe la ingesta, no se conoce su origen, idiopática.
o Acalasia: falta de relajación del cardias cuando llega el bolo alimenticio
- De origen muscular (miopática):
o Escleroderma: enfermedad sistemática. Afecta a muchos órganos. De los
primeros es el esófago. Ejemplo: el músculo del esófago se atrofia, no se
puede contraer.
Consecuencias de la disfagia: retención de alimento y líquidos por encima de obstáculo, y
produce una inflamación de los pulmones por espiración neumonía
Desnutrición y deshidratación
ENFERMEDAD POR REFLUJO GASTROESOFÁGICO
Def.: conjunto de síntomas y de lesiones anatomopatolígicas que se producen como
consecuencia de un reflejo anormal del contenido gástrico hacia el esófago.
Causas de la enfermedad por reflujo gastroesofágico:
- Incompetencia del esfínter esofágico inferior: del cardias que no se mantiene cerrado
como debería.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Incapacidad de peristaltismo secundario para eliminar material refluido (si falla
problema)
Consecuencias de la enfermedad por reflujo gastroesofágico
- Pirosia (ardor en el esófago)
- Regurgitación (el contenido pasa a la boca)
- Esofagitis (inflamación mucosa del estómago)
- Esófago de Barret: transformación del epitelio del esófago, se convierte en otro
epitelio más propenso a las úlceras y al cáncer. Primer factor de riesgo para padecer
cáncer de esófago.
Ejemplo: hernia de hiato: el polo superior del estómago se introduce en el tórax a través del
hiato esofágico. Explicación: es un agujero en el diafragma para pase el esófago. En algunas
personas parte del fondo del estómago y queda atrapado hernia de hiato (incapacidad del
cardias)
2. Trastornos de la motilidad gástrica
GASTROPARESIA / ESTENOSIS PILÓRICA / INCONTINENCIA GÁSTRICA
Gastroparesia: evacuación lenta del contenido del estómago sin que exista un obstáculo
mecánico para el vaciamiento. Estreñimiento anormal (bezoares formación de grandes
masas)
Estenosis pilórica: existe un obstáculo mecánico que dificulta el vaciamiento gástrico (ejemplo:
úlcera juxtapilórica (al lado del píloro) cicatrizada)
Incontinencia gástrica (“Síndrome de dumping”): vaciamiento gástrico acelerado, con
distención brusca de las primeras porciones del intestino sensación de plenitud, debilidad,
sudoración y palpitaciones. A veces se produce al hacer una piloroplastia (intervención
quirúrgica)
VÓMITO
Def.: Expulsión del contenido gástrico, de forma activa (reacción refleja compleja), por la boca.
Fases del vomito (3 fases)
- Pródromos: reacción vegetativa con palidez, taquicardia, taquipnea, salivación y
sudoración
- Respuesta motora digestiva: contracciones retrógradas del intestino delgado, que
impulsan su contenido hacia el estómago, relajación del esófago y sus esfínteres.
- Expulsión del contenido gástrico: por contracción violenta de los músculos
respiratorios y de la pared abdominal.
Antes se suele experimentar nauseas (sensaciones desagradables en el abdomen y el cuello) y
arcadas (vómitos frustrados)
Dos conceptos importantes:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Hematemesis: expulsión de sangre procedente del aparato digestivo por la boca.
- Melena: expulsión de sangre procedente del aparato digestivo por el ano.
Causas del vomito
Vómitos centrales:
- Psicógenos (ej. Volemia)
- Por estímulos sensoriales desagradables
- Por estimulación del laberinto estatocinético (ej.: mareo en el coche)
- Hipertensión craneal (vómitos en escopetazo)
- Por estimulación de quimiorreceptores centrales:
o Por tóxicos exógenos (quimioterapia)
o Por alteraciones del medio interno. Ej.: insuficiencia hepática, renal…
Vómitos periféricos
- Por estimulación de quimio o mecanorreceptores periféricos
Tipos de vomito. Diferentes clasificaciones:
Según el momento de su aparición:
- Matutinos: alcoholismo, uremia, embarazo
- Inmediatamente tras las comidas: psicógenos
- 30 min a 3 h después: daños gástricos o duodenales
- Tardíos (12h o más): estenosis pilórica, íleo
Según el color, aspecto, sabor y olor del material vomitado:
- Alimentarios: reconocibles los alimentos ingeridos
- Acuosos: claros, contienen secreción gástrica, sabor ácido
- Bilosos: color amarillo – verdosos y sabor amargo
- Porráceos: color verde, expulsión del contenido intestinal
- Fecaloides: aspecto y color de heces, en íleo avanzado
Consecuencias del vomito
- Acción defensiva: eliminación de sustancias que dañan o estorban
- Esofagitis y erosión dental
- Neumonía por aspiración
- Desnutrición, deshidratación, alteraciones del medio interno
3. Trastornos en la motilidad intestinal
ESTENOSIS INTESTINAL / ILEO
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Estenosis intestinal: reducción de la luz del intestino
Estenosis ileo: si lo interrumpe por completo
Causas del ileo
- Ileo mecánico (obstáculo mecánico) Puede ser por:
o Obstrucción simple: intraluminal, parietal, extraparietal (oprime el tubo hacia
afuera)
o Estrangulación: cesa la motilidad sin obstáculo que impida el transito, además
afecta a la irrigación. Ejemplo: una hernia intestinal, producida por un trozo de
intestino que sale por el orificio inguinal u otro tipo de orificio y se estrangula
si ese orificio se cierra puesto que no llega sangre.
- Ileo funcional (ileo paralítico)
o Origen reflejo (estimulación mecánica en cirugía)
Consecuencias del ileo
- Cesa expulsión de heces por el ano
- Manifestación de la estenosis intestinal
o Dolor cólico (dolor repentino)
o Ondulaciones de la pared abdominal
o Abombamiento de la pared abdominal
- Vómitos tardíos: doce horas o más después de las comidas
- Deshidratación, hipopotasemia, acidosis metabólica ( por perdida de potasio en la
sangre)
- Insuficiencia circulatoria aguda (shock) por la hipovolemia y por la producción de
toxinas (toxemia)
ESTREÑIMIENTO
Retroceso en la evacuación intestinal en general con heces escasas y duros (por en menor
volumen) Ocurre estreñimiento cuando:
- < 3 deposiciones/semana
- 3 o más días entre una u otra
- Peso de las heces sea > 35 g/día
Las dietas ricas en fibra son buenas para el estreñimiento se generan productos que
aumenta la excitabilidad y además retiene agua y facilitad su evolución
Causas del estreñimiento
- Enlentecimiento del tránsito del contenido de colon. Por:
o Obstáculos mecánicos (ejemplo cáncer de colon)
o Inercia colónica (hipomoticidad, descenso den la excitación de la musculatura
del colon)
Hipotiroidismo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Hipopotasemia e hipercalcemia
Medicamentos (opiáceos, antidepresivos, anticolinérgicos)
- Trastorno de la evacuación rectal
o Pérdida de los reflejos de defecación (causa más frecuente) Durante la infancia
o durante malos hábitos que debilita, el reflejo de la defecación o el abuso de
laxantes.
o Lesión de las vías del reflejo de defecación (lesiones medulares)
o Debilidad del diafragma y músculos abdominales
o Tenesmo rectal: sensación de ardor y ocupación y la impresión de que la
deposición no ha sido completa
Consecuencias del estreñimiento
- Hernias
- Lesiones anales
- Fecalomas (masas de heces en el recto) frecuente en ancianos
- Mayor riesgo de cáncer de colon, por mayor riesgo, más tiempo en contacto con la
mucosa, se puede producir mutación.
TEMA 32: SECRECCIONES SALIVAL Y GÁSTRICA
Introducción
Secreción Origen pH Componentes Regulación Regulación Efecto
orgánicos nerviosa hormonal
(además de
mucus)
Saliva Glándulas neutro Amilasa SNV-PS Estimula
salivales SNV-S sec.serosa
Estimula
sec.mucosa
Jugo Estómago ácido Pepsinas Vago Gastrina Estimula
gástrico Factor Estimula
intrínseco
SECRECCIÓN SALIVAL
1. Funciones de la saliva
- Facilita la deglución (lubrifica el bolo)
- Conserva la humedad de la boca
- Ayuda a la percepción del sabor
- Facilita la fonación
- Inhibe la proliferación bacteriana en la boca: lisozima, HCO-3 (el bicarbonato de la
saliva se neutraliza el ácido y se retrasa la aparición de caries)
- Inicia la digestión con 2 enzimas:
o Lipasa lingual: actúa sobre lípidos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
o Ptialina o alfa amilasa: degrada el almidón
Tienen un ph=7 por lo que con el ph ácido del estómago se degrada
3 glándulas salivales
- Glándula parótida
- Glándula submaxilar
- Glándula sublingual
Dentro de los glándulas salivales, las células se encuentran en los acinos, son una hilera de
células secretoras de saliva, los espacios acilares se unen y dan los conductos intercalar y estos
vierten a los conductos intralobular y estos ya tienen músculos para contraerse.
2. Composición y formación de la saliva
- 1500 ml/días ph=7 (ph óptimo)
- Hipoosmótica (menor molaridad que el plasma)
- Proteínas. Dos tipos de secreción
o Secreción serosa (ptialina) muy abundante y rica enzimas
o Secreción mucosa (mucinas) rica en mucos, más espesa
- Electrolitos: Na+, K+, Cl- y HCO-3 Además de las proteínas hay electrolitos, y en
relación al plasma la saliva tiene más potasio y bicarbonato y menos Sodio y Cloro
que plasma.
Las parótidas cuando se estimulan producen secreción serosa. Las submaxilares y sublingual
son glándulas mixtas tanto serosa como mucosa.
La saliva se forma en dos fases:
Primero tiene lugar en los acinos, se produce una solución primaria que tiene la misma
concentración electrolítica que el plasma y también tiene proteínas y cuando va pasando por
los conductos se va modificando y cuando viajen al plasma se va absorber Na y Cl y se van a
secretar potasio y bicarbonato y van a pasar a la saliva. Predominan los iones absorbidos que
los secretados y los conductos son poco permeable al agua, por ello es una saliva
hipoosmótica.
Si la secreción ocurre muy rápido, no da tiempo a la producción de esos cambios, por eso
cuando la secreción es rápido la composición de la saliva se parece más a la del plasma
3. Control de la secreción salival
Se produce de manera constante, aproximadamente a razón de 0.5ml/min es de tipo mucosa y
durante la noche la secreción salival disminuye. Durante esta situación de reposo se produce
estimulación en respuesta a diferentes estímulos como:
- Gustativos: 8ml/min de saliva (ej. El sabor ácido)
- Táctiles (ej. Los caramelos) el tener un objeto en la boca produce estimulación de
la saliva. Es de tipo nervioso, las vías aferentes llevaran la información al centro
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
control de la salivación y aquí también llega información de centros superiores y
por eso la vista, el olor, o pensar en comida produce que salivemos
- Mecánicos
Estos reflejos se pueden condicionar fácilmente.
En cuanto a las vías afectos son de dos tipos:
- Sistema nervioso parasimpático: que estimulan la secreción serosa por parte de las
parótidas (rica en ptialina) porque produce una vasodilatación de las glándulas
salivales.
- El sistema nervioso vegetativo simpático también estimula, una secreción mucosa
en este caso, produce saliva mucosa procedente sobre todo de los submaxilares.
SECRECCIÓN GÁSTRICA
1. La mucosa gástrica
La estructura de la pared del estómago es similar. La superficie está incrementada por la
presencia de invaginaciones: fosas o criptas gástricas que desembocan en las glándulas
gástricas.
Las células que están en la mucosa gástrica son:
- En la superficie de la mucosa están las células epiteliales superficiales, la cuales
secretan fundamentalmente mucus y una solución rica en bicarbonato y forman
un gel flexible (ph=7) que protege la mucosa fundamentalmente del HCl.
- Dentro de la glándulas están:
o Las células mucosas del cuello que producen mucus
o Más abajo, están las células parietales (oxínticas) que secretan el HCl del
jugo gástrico y también el factor intrínseco.
o Las células principales (pépticas) que producen el pepsinógeno
o Y en el fondo, en la zona del antro, en la parte final hay otras células
llamadas las células G, que producen la hormona gastrina, la cual se libera
a la sangre y con la sangre llega a las diferentes células con las que actúa
La mucosa recibe gran irrigación sanguínea y se inerva por el parasimpático del nervio vago y la
inervación simpática es a través de neuronas del plexo celiaco.
2. Composición y secreción del jugo gástrico
Se produce 2,5 L/día, se trata de un líquido isotónica y de pH muy ácido (pH=1).
Fundamentalmente está formado por:
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
1. El HCl, muy concentrado 150Mm le da el pH ácido del jugo gástrico. Es muy importante
aquí porque ayuda a digerir el tejido conectivo y las fibras musculares de la carne que
ingerimos. También porque es el responsable de la actuación del pepsinógeno.
PEPSINÓGENO PEPSINA (el HCl rompe el pepsinogeno y lo convierte en pepsina, la
cual tiene un pH ácido optimo y eso también le da el carácter ácido al jugo)
Otra función del HCl es también como bactericida, es decir elimina agentes dañinos
que ingerimos con los alimentos.
2. Mucus (glicoproteínas) formado por glicoproteínas y forman e gel flexible rico en
bicarbonato que protege a la mucosa de la acción química del ácido (barrea protectora
formada por glicoproteínas)
3. Pepsinógeno: es una proenzima. En las células pépticas este pepsinógeno se
encuentra almacenado en gránulos de Zianógeno y cuando se estimula la células para
que se secreten los gránulos de Zianógeno van hacia la membrana y se liberan el
contenido por endocitosis, de tal manera que el pepsinógeno llega a la luz de la
glándula gástrica. Las pepsinas rompen los enlaces del HCl de las moléculas de
proteínas (endopeptidasas). Las pepsinas digieren entre un 10-20% de las proteínas de
la dieta pero no son indispensable porque en ausencia de estas las proteasas del jugo
pancreático son capaces de completar la digestión.
Debido además a que su pH óptimo (ácido) cuando ya el quimo pasa al duodeno las
pepsinas se inactivan.
4. Factor intrínseco: es una glicoproteína porque fija a la vitB12 y la protege de los
diferentes jugos digestivos y permite que llegue intacta al íleo donde se absorbe. Esta
es la única función que es imprescindible para la vida. Si no absorben vitB12 se
produce la anemia perniciosa.
En las células oxínticas (parietales) el HCl se secreta en contra de gradiente gracias a la bomba
ATPasa que expulsa protones en contra de gradiente intercambiándolos con K+ y consume
ATP. Los protones salen de la hidratación del CO2 del metabolismo que se combina con agua
(esto lo cataliza la anhidrasa carbónica) que forman bicarbonato y protones, estos son los que
salen a la luz del estómago. El bicarbonato se intercambia con Cl- en la zona basal de las células
y sale a la luz a través del canal electrogénico.
Cuando se produce una secreción activa del ácido, pasa el bicarbonato a la sangre y se produce
un aumento, la sangre se vuelve alcalina: marea alcalino.
Marea alcalina: durante la secreción gástrica activa el pH de la sangre venosa del estómago es
alto por el paso a la sangre del bicarbonato.
A mayor velocidad la concentración de protones es más alta
A menor velocidad la concentración de protones es más baja y aumenta la
concentración de sodio.
El más importante es el Cl- y la concentración de potasio que a cualquier velocidad del jugo
gástrico es superior a la del plasma hipopotasemia: cuando hay muchos vómitos se puede
producir. Se producen estos cambios con la velocidad porque se piensa que cuando se
estimula la secreción de ácido mas bomba H+/K+ llegan a la membrana de la células y facilita el
que se expulsen los protones.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
3. Regulación de la secreción gástrica
Tanto el HCl y el pepsinógeno se regulan a la par, conjuntamente. Existen 3 moléculas
principales que estimulan la secreción gástrica:
- Histamina: producen algunas células de la mucosa, se une a los receptores H2 de
las células oxínticas, aumenta la producción mediante el aumento del AMPc
intracelular, la concentración intracelular es el principal estimulo fisiológico para la
estimulación del ácido.
- Acetilcolina: la liberan las neuronas del sistema nervioso parasimpático las ramas
del nervio vago y también las neuronas de los plexos intestinales. Y uniéndose a
receptores muscarínicos estimula la producción de ácido y también de
pepsinógeno. Actúa por incrementos de la concentración intracelular de Ca2+
- Gastrina: es una hormona producía en las células G de las mucosas del antro,
llegan a las células oxínticas y se unen a sus receptores y estimulan la formación de
ácido también por aumento de Ca2+ intracelular.
La acción de unas potencian la acción de otras, hay también manera de inhibir la secreción: el
exceso de ácido en la luz del estómago inhibe la secreción ácida, se auto limita. También hay
moléculas que inhiben la secreción ácida por ejemplo PGE2
La aspirina y los antiinflamatorios producen PGE2 por lo que favorecen a la inhibición de la
secreción gástrica.
Esta regulación ocurre en tres fases:
1. Fase cefálica: es el conjunto de procesos que estimulan la secreción gástrico incluso
antes de que los alimentos lleguen al estómago, se produce ya un 30% Consiste en la
activación de quimiorreceptores por el sabor de alimentos o olor y la estimulación de
los mecanorreceptores durante la masticación y deglución que van a mandar señales a
centros situados en el bulbo y a partir de ellos mandan órdenes estimuladores a través
del nervio vago. A estos centros del bulbo también pueden llegar estímulos en centros
superiores (como ya hemos visto)
Si el estómago todavía está vacío y no hay nada que neutralice el ácido, el ácido limita
e inhibe más secreción de acido (función: auto limita)
2. Fase gástrica: es el conjunto de procesos que estimulan la secreción gástrica cuando
los alimentos están en el estómago en esta parte se produce más del 60% del jugo. El
estimulo es el estiramiento de las paredes del estómago con los alimentos por vía
vagal que produce un estimulo para la secreción de ácido. Además, el estiramiento de
las paredes del antro hace que se libere gastrina, muy importante también la gastrina
se libera en respuesta a:
a. Estímulos nerviosos colinérgicos
b. Estímulos químicos ( de rectos de digestión de proteínas)
c. Estímulos mecánicos (distensión)
3. Fase intestinal: es un conjunto de procesos que se desencadenan por la presencia del
quimo en el duodeno en esta fase solo se produce el 5% En esta última fase el papel
del duodeno es doble, en primer lugar estimula la secreción gástrica cuando el quimo
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
que llega tiene un pH ácido de pH>3 (entonces se secreta aún mas). En la primera zona
del duodeno hay células G que en respuesta van a producir gastrina cuando llega el
quimo a esta zona se produce la formación de gastrina. Pero en una segunda fase
cuando el pH del quimo pH < 2 se inhibe la producción, porque el quimo ya es
demasiado ácido, y se interpreta como que ya no es suficiente mayor producción, y se
hace mediante hormonas:
a. Secretina
b. CCK
c. PIG (péptido inhibidor gástrico)
Estas hormonas inhiben la producción de ácido por el estomago.
TEMA 33: SECRECIONES PANCREÁTICA E INTESTINALES
SECRECCIÓN PANCREÁTICA
1. El páncreas exocrino
El páncreas tiene doble función:
- Endocrina: formación de hormonas. Muy importante por la formación de insulina y
glucagón para el metabolismo glucídico.
- Exocrina (donde nos vamos a centrar) produce el jugo pancreático porque contiene
mucho bicarbonato y ese bicarbonato va a neutralizar el ácido del estomago. Y tiene
un componente enzimática, una serie de enzimas que van hacer la mayoría de la
digestión.
El páncreas se organiza en acinos, células acinares, que secretan su contenido a un espacio
acinar, son los que producen el componente enzimática del jugo pancreático.
Muchos acinos se agrupan formando lóbulos, vierten a unos conductos, conducto intercalares,
que se unen entre sí y dan los conductos intralobulos y estos se juntan formando el conducto
extralobular y estos se juntan formando el conducto colector principal o conducto pancreático
junto con el colédoco, que desemboca ya en el duodeno unido al colédoco y dejan al duodeno
a través de la ampolla Better.
Las células son los responsables del componente acuoso electrolítico pancreático, las enzimas
las producen las células acinares. Por último el páncreas está irrigado por ramas de la arteria
celiaca y de la mesentérica superior y la sangre venosa que sale del páncreas va a verter a la
vena porta hepática. En cuanto a la inervación, el más importante, el del nervio vago que
estimula la secreción pancreática.
2. Composición del jugo pancreático.
El páncreas produce 1000-1500 ml/día, el páncreas pesa alrededor de 100gr. El jugo
pancreático es un líquido de pH alcalino que permite neutralizar el pH ácido del jugo gástrico
(pH= 1) Muy importante porque el pH optimo de actuación de las enzimas pancreáticas es
entre 7-8, por lo que es importante la neutralización del jugo gástrico también colabora la bilis.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Hay dos componentes fundamentales:
- Componente acuoso: agua y electrolitos: Na+, K+, Cl- y HCO3-
La concentración de Na+ y K+ es muy similar a la del plasma y se mantiene constante.
Sin embargo, la concentración de bicarbonato oscila bastante y es mayor cuando
aumenta el flujo de secreción de jugo pancreático. La concentración de Cl- disminuye
inversamente a la del bicarbonato. Entonces la suma de los 2 cationes tiene que ser
igual a la suma de los 2 aniones Cl- + HCO-3 = Na+ + K+
El componente acuoso lo produce las células de los conductos (intralobular,
extralobular…) y producen un liquido muy rico en bicarbonato. Cuando el páncreas es
estimulado para secretar más entonces también producen electrolitos las células de
conductos extralobulares (por ejemplo con secretina) produce liquido rico en
bicarbonato. A medida que va a pasar a los conductos el bicarbonato se va a
intercambiar con Cl- Si la secreción va lenta puede ocurrir, pero si la secreción es
rápida la concentración de bicarbonato es mayor y el cloruro varia con el bicarbonato
inversamente por eso.
El bicarbonato viene de las células de los conductos y el CO2 del metabolismo celular
CO2 + H2O <-> HCO3- + H+
Pero ahora el bicarbonato es el que sale a los conductos intercambiándose con el
cloruro mientras que los protones salen hacia el lado basal de la célula
intercambiándose con el Na+ a la sangre.
- Componente enzimático: producido por las células acilares que contienen gránulos de
Zianógeno donde están los precursores de las enzimas. Durante periodos de comida se
van cargando y cuando comemos esos gránulos de Zianógeno se funde y se estimula la
secreción y las pro enzimas se liberan por endocitosis.
o Proteasas: tripsina, quimotripsina y carboxipeptidasa. Se secretan como
proenzimas que son respectivamente tripsinógeno, quimotripsinógeno y
procarboxipeptidasas, y así llegan al duodeno y allí hay una enzima producida
por la mucosa duodenal ENTEROPEPTIDASA que rompe el tripsinógeno para
dar la tripsina activa y la tripsina rompe los otros. Es decir la actuación tiene
que darse en el duodeno porque si se activa dentro del páncreas se podría
digerir el propio páncreas.
La tripsina puede activarse así misma. Son proteasas, rompen enlaces
liberando péptidos más pequeños. La tripsina y quimotripsina son
carboxiterminal y carboxipeptidasa eliminan el carboxi terminal.
o Alfa-amilasa: Que rompe el almidón liberando disacárido maltosa. Se secreta
activa, no requiere la activación.
o Lipasas: que actúan sobre lípidos, triacilgliceridos, colesterol, digieren grasas.
o Ribonucleasas y desoxirribonucleasas que son capaces de romper el ADN y el
ARN liberando los nucleótidos.
o Colagenasa, elastasa, etc…
3. Regulación de la secreción de jugo pancreático.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
A diferencia, para el jugo gástrico en este caso los componentes acuosos o enzimático se
regulan de manera independiente de tal manera que el componente puede variar mucho, de 1
a 10% porque se regulan independiente.
El primer estimulo fisiológico para la secreción del componente acuoso del jugo pancreático es
la SECRETINA (estimulan las células de los conductos extralobulares para producir este
componente acuoso rico en bicarbonato) La secretina se forma pro las células S que están en
la pared del duodeno y primera mitad del yeyuno y liberan secretina en respuesta a un pH
ácido en esa zona (prox 4,5=
En el caso del componente enzimático, es estimulado por vía nerviosa del nervio vago que
produce acetilcolina y estimulan las células acilares que producen componente enzimático y es
por la presencia de alimentos. También las gastrina estimula la secreción de componente
enzimático. Pero el principal estimulo fisiológico para la formación de componente enzimático
es la CCK-PZ colescitokinina – pancreozinina, es formada en presencia de ciertos productos de
digestión sobre todo de aminoácidos esenciales y de aminoácidos de cadena larga (es
producido en yeyuno y duodeno). Y la producción es inhibida por la presencia de tripsina en el
duodeno, y se limita la secreción de componente enzimático.
La regulación se produce en tres fases:
1. Fase cefálica: la estimulación la lleva el nervio vago (vista, sabor, olor..)
2. Fase gástrica: cuando los alimentos están en el estomago donde la secreción la lleva la
gastrina.
3. Fase intestinal: aquí se produce la mayoría gracias a la secreción de secretina
(componente acuoso) y CCK (componente enzimático) ambos en el duodeno.
SECRECCIONES INTESTINALES
La mucosa intestinal desde el duodeno hasta el ano va a producir secreciones con electrolitos,
mucus, agua y suele tener un pH alcalino el mucos sirve para proteger la mucosa de agresiones
mecánicas, química y el agua da un substrato para la absorción de nutrientes. No son iguales
todas las secreciones:
- Secrecciones duodenales (glándulas de Brunner): se produce un moco alcalino y
viscoso que protege la mucosa del ácido del estomago.
- Secreciones del intestino delgado: liquido isotónico con pocas enzimas.
- Secreciones del colon: menor volumen, con más mucus, mas espesos para proteger
más porque son zonas con mayor ardor.
En general están estimuladas por el vago (estimulación nerviosa) o secretina (estimulación
normal)
TEMA 34: ALTERACIONES DE LAS SECRECIONES DIGESTIVAS
1. HIPERSECRECIÓN GÁSTRICA. ÚLCERA PÉPTICA.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Las úlceras pépticas son lesiones de la mucosa dudodenal o gástrica, debidas a la acción de
digestión sobre la misma del ácido y la pepsina del propio jugo gástrico que digiere la propia
mucosa.
Las úlceras suponen la rotura de la mucosa o submucosa y puede llegar a la capa muscular,
puede llegar a la perforación. Se acompañan siempre de una gastritis crónica de la mucosa
gástrica.
Causas de la úlcera péptica
1. Hipersecreción de ácido por la mucosa gástrica (en úlcera duodenal):
Aumento del número de células parietales (oxínticas, las que producen HCl)
Aumento de su sensibilidad al estímulo de la gastrina (gastrina = principal
estimulo para la secreción de ácido)
Hipersecreción de gastrina (mucha estimulación de ácido)
Aumento del tono vagal (la estimulación del vago produce ácido)
Gastrinoma o síndorme de Zollinger-Ellison: es un tumor que produce gastrina.
Suele ser un tumor pancreático, induce una secreción de gastrina descontrolada.
En el caso del estómago se produce:
2. Desequilibrio entre factores agresores y protectores de la mucosa (en úlcera
gástrica):
Infección por Helicobacter pylori: presente en el 95% de personas con úlceras
pepiticas. Lo que hace es disgregar la capa protectora de la mucosa y daña
produciendo las úlceras. Deja desprotegida la célula y el ácido ataca. También
responsable de la gastritis crónica.
Gastritis por: fármacos antiinflamatorios no esteroideos (aspirina) que por un
lado inhiben la producción del gel flexible y por otro lado estimula la secreción
gástrica, alcohol, vinagre, sales biliares, tabaco que estimula la secreción de
acido e inhibe la secreción de bicarbonato y retrasa así la cicatrización de
úlceras.…
Puede dar lugar a situaciones de emergencia. Los dolores abdominales fuertes, con o sin
evidencia de sangrado, pueden ser indicio de una perforación de la úlcera en el estómago o
duodeno. El vómito de una sustancia semejante a café (hematemesis: eliminación de sangre
del tubo digestivo) o la presencia de heces negras (melena: heces con sangre) pueden ser
indicio del sangrado.
Gastroscopia: se ubica un endoscopio (pequeño tubo flexible con cámara y luz) dentro del
estómago y duodeno para buscar anormalidades. Se pueden obtener muestras de tejido para
determinar la presencia de H.pylori. Las úlceras sangrantes se pueden cauterizar (se sellan los
vasos sanguíneos con un instrumento que quema) durante la gastroscopia.
2. ALTERACIONES DE LA SECRECCIÓN PANCREÁTICA. PANCREATITIS.
Inflamación del páncreas.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Pancreatitis aguda (en un momento determinado): autodigestión del páncreas por activación
prematura del tripsinógeno en las células acinares. Puede ser:
Edematosa (severidad baja/media), con edema (acumulación de liquido)
intersticial, inflamación e infiltración leucocitaria.
Necrotizante (severidad alta) además hay hemorragia y necrosis.
Etiología: cálculos biliares, alcohol (consumo abusivo de alcohol)
Manifestaciones: dolor abdominal, fiebre, vómitos. Leucocitosis, aumento de enzimas
pancreáticas en plasma. Puede llevar a muerte por fallo multiorgánico.
Pancreatitis crónica: inflamación continua del páncreas, con alteración morfológica (durante
meses (años) (fibrosis) y funcional irreversible
Etiología: alcohol
Manifestaciones: disminuye la secreción de jugo pancreático al duodeno maladigestión.
3. DIARREA. TIPOS Y CONSECUENCIAS
Diarrea: trastorno intestinal caracterizado por la emisión de heces poco consistentes, con
deposiciones frecuentes. >200 g heces/día, con alto contenido en agua.
El intestino delgado tiene una gran absorción de este líquido total, aproximadamente absorbe
de esos 9 L, 7L, y el resto lo absorbe el colon. El riñón va hacer posible la regulación de la
perdida de agua del organismo.
Tipos de diarrea
Diarrea osmótica (defecto en la absorción del agua en el intestino)
Productos no absorbidos que retienen agua por acción osmótica. Se puede
deber a una maldigestión o malabsorción, sobre todo por hidratos de carbono
como por ejemplo el caso de la lactosa (cuando hay déficit de lactasa)
Algunos laxantes retienen agua y aumentan el volumen de las heces.
Diarrea secretora (predominio de la secreción sobre la absorción, es decir hay un exceso de
secreción)
Por secretagogos normales en exceso: ácidos biliares (diarrea cológena),
ácidos grasos, gastrinoma. Un secretagogo es una sustancia que estimula la
secreción, por ejemplo los ácidos biliares que se absorben en el íleo, pero si se
da el caso de que en una persona no tiene íleo, llegan al intestino grueso y
producen la secreción intestinal, la llamada diarrea cológena.
Por secretagogos patológicos: enterotoxinas bacterianas (toxina colérica del
Vibrio cólera) el caso más significativo es la toxina colérica producida por el
Vibrio cólera que se produce gran pérdida de agua por la heces por lo tanto
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
gran deshidratación (15L de agua al día) Esta bacteria estimula las paredes del
intestino delgado.
Por lesión de las vellosidades intestinales (enteritis por virus) enteritis:
inflamación de la mucosa del intestino por diferentes virus, que producen
lesión en las vellosidades intestinales.
Diarrea motora (aceleración del tránsito intestinal, no da tiempo a la absorción)
En diabetes, hipertiroidismo, intestino irritable. En estos casos está acelerado
el tránsito intestinal.
Consecuencias de la diarrea
Perdida de sodio y agua. Hipovolemia que desencadena el Shock circulatorio. Hipopotasemia
por la pérdida de potasio y acidosis metabólica por la pérdida de bicarbonato
TEMA 35: FISIOLOGÍA DEL SISTEMA BILIAR
Sales biliares Contra la vesícula
Bilis Hígado alcalino Colesterol Vago CCK Estimula SB
Fosfolípidos Secretina Estimula agua y HCO3
1. Papel fisiológico de la función biliar
Digestiva:
Tampón pH, lubricación, emulsión de las grases de la dieta, activador de lipasas,
absorción de lípidos y vitaminas liposolubles
Excretor:
Pigmentos biliares, colesterol y xenobioticos
Defensivo:
Flujo biliar descendente, efecto bactericida de los ácidos biliares y IgA
La bilis es importante para:
1. La digestión y la absorción de las grasas de la dieta: las sales biliares contribuyen a
emulsionar las grandes partículas de grasa en otros alimentos, que pueden sufrir el
ataque de la enzima lipasa que segregada en el tubo digestivo. Además participa en el
transporte de absorción de productos terminales digeridos de la grasa hacia y a través
de la membrana hacia la mucosa intestinal.
2. La eliminación de productos de desecho por la sangre: la bilis sirve como medio de
excreción de algunos productos de desecho importantes de la sangre, principalmente
la bilirrubina, un producto terminal de la Hb y del exceso de colesterol sintetizado por
los hepatocitos.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
El sistema biliar también se llama árbol biliar y tiene una vesícula biliar asociada. Las funciones
de esta vesícula biliar son: almacenamiento y liberación a duodeno, concentración, secreción.
Tipos de conductos:
- Conducto colédoco
- Conducto hepático
- Conducto cístico
- Conducto pancreático
2. Composición de la Bilis Vesicular Humana (%en peso)
La bilis está formada en mayor cantidad por ácidos biliares (51%), por fosfolípidos (25%),
electrolitos, otros pigmentos, glutatión, xenobioticos, fármacos, etc (18%) y por bilirrubina y
colesterol en muy pequeñas concentraciones.
3. Tipos de ácidos biliares
Primarios Secundarios
Colico Desoxicolico
Quenodesoxicolico Litocolico
Los ácidos biliares conjugados con glicina o taurina, pero no con otros aminoácidos, son
resistentes a las carboxipeptidasas presentes en la secreción pancreática. Por lo tanto, ácidos
biliares conjugados no son digeribles y no absorbibles de forma pasiva.
Tipos de bombas:
Son bombas de colesterol, sin las micelas el colesterol precipita y se formarían cálculos biliares.
Para quitar colesterol se pueden expulsar el colesterol con micelas o transfórmalas en ácidos
biliares para que las excreten. Todas consumen ATP y forman ADP mas fosfato inorgánico.
- BSEP
- BCRP
- MRP2
- MDR3
- ABCG5, ABCG8
4. Papel fisiológico de los ácidos 3. Modulan la biosíntesis de
biliares colesterol
4. Regulan el número de receptores
En el hígado de membrana para las
1. Generan una fracción importante lipoproteínas
del flujo biliar (BADF) 5. Activan al catabolismo de
2. Inducen la secreción biliar de Protoporfiria a bilirrubina
lípidos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
6. Modulan la inserción de
transportadores de la membrana
canalicular
7. Modulan la expresión de
transportadores de la membrana
sinusoidal
En la bilis
1. Forman micelas que transportan
sustancias hidrofobias
2. Actúan como buffer para calcio
3. Modulan la función secretora de
los colangiocitos
4. Estimulan la secreción de
glicoproteínas por la vesícula biliar
5. Acción antibacteriana frente a
infecciones ascendentes
6. Favorecen la secreción de IgA
En el intestino
1. Forman micelas que permiten la
emulsión de grasas
2. Activan lipasas
3. Aceleran el transporte de lípidos
4. Modulan la motilidad intestinal
5. Modulan la perfusión intestinal
6. Modula la secreción de hormonas
gastrointestinales
7. Inducen la secreción de agua y
electrolitos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
5. Sistema de transporte biliar
BSEP (bomba exportadora de ácidos biliares) Regulación por retirada e inserción en la
membrana plasmática de transportadores de ácidos biliares. Los hepatocitos retira bombas de
la membrana las coloca en regiones perinucleares y cuando se necesitan llegan ácidos biliares
y se vuelven a activar. La señal es leída por FXR (receptor nuclear) lee que hay muchos
hepatocitos y esa señal va a ser igual a la cantidad de ácidos biliares.
Regulación por cambio de expresión de transportadores de ácidos biliares (MRP3 y MRP4)
permite que se regurgite (regurgitación sinusoidal de componentes biliares) a la sangre ácidos
biliares. El hígado modifica esas sustancias tóxicas para que el riñón pueda secretar en orina.
6. Regulación de la función biliar
Regulación nerviosa: SNV-PS por el nervio vago.
Regulación hormonal: el duodeno manda señales hormonales, la CCK, va por la sangre y
favorece el vaciado de la vesícula biliar, esta hormona va a todos los sitios, en el hipotálamo
activa la saciedad (ej. Al consumir grasas)
También la presencia de quimo activan las células S que liberan la Secretina por el pH ácido del
quimo. La secretina estimula al hígado al árbol biliar para producir bicarbonato. El pH de la bilis
es alcalino para secreter y poner el pH al punto más óptimo.
Regulación autocrina/paracrina: ácidos biliares son producidos por los hepatocitos. Los
colangiocitos también responden a los ácidos biliares.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
TEMA 36: FISIOPATOLOGÍA DEL SISTEMA BILIAR
1. COLESTASIS
Reducción o ausencia de llegada del flujo biliar al duodeno por falta de secreción por el hígado
o retención en el sistema biliar y como consecuencia aparece regurgitación a la sangre de
algunos de los componentes normales de la bilis
Tipos de colestasis
LOCALIZACIÓN PIGMENTACIÓN EVOLUCIÓN
EXTRAHEPÁTICA ICTERICA AGUDA
INTRAHEPÁTICA ANICTERICA CRÓNICA
Etiología y etiopatogenia de la colestasis
LOCALIZACIÓN PATOGENIA CAUSAS
EXTRAHEPÁTICA Obstrucción de los conductos Cálculos, estenosis, atresia,
biliares: parasitosis, quiste coledocal,
A) Extraparietal (tumores de colangitis ascendente, colangitis
la cabeza del páncreas)
primaria y secundaria
B) Parietal (tumores,
esclerosante, carcinoma de
cicatrices)
C) Intraluminal (cálculos) páncreas o de vías biliares
INTRAHEPÁTICA Obstrucción de los conductos Cálculos tumores, abscesos,
biliares parasitosis, atresia, colangitis
esclerosante.
HEPATOCELULAR (afecta a la
formación de la bilis)
a) Lesión hepatocitaria Necrosis, hepatitis vírica aguda,
global hepatitis alcohólica aguda,
hepatitis tóxica
b) Disfunción del aparato Síndromes de Rotor, Síndromes
secretor biliar de Dubin-Johnson, displasia
arteriohepática, cirrosis,
colestasis étnica
c) Daño en el canalículo Fármacos (esteroides),
Protoporfiria eritrohepática,
enfermedad de Hodgkin’s,
genético (colestasis familiar)
d) Lesión subcelular Deficiencia de alfa-1-antripsina,
galactosemia, tirosinemia, otros.
Características diferenciales entre colestasis extrahepática e intrahepática
Colestasis extrahepáticas
- La obstrucción tiende a ser completa
- El remedio suele ser quirúrgico
Colestasis intrahepáticas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- La colestasis es generalmente incompleta
o No todas las vías biliares se han obstruido
o Ni todos los hepatocitos han dejado de fabricar la bilis
- El tratamiento quirúrgico no tiene sentido, salvo el trasplante.
Consecuencias clínicas de la disfunción biliar
SIGNOS Y SÍNTOMAS MANIFESTACIONES TÉCNIAS DE IMAGEN
BIOQUÍMICAS
Ictericia Bilirrubinemia Ecografía
- Total TAC (hepatomegalia, dilatación
Heces hipocólicas o acólicas - Libre o indirecta árbol biliar, ley de Courvoissier-
- Conjugada o terrier)
Coluria directa
Colanemia Endoscopia
Prurito: Colesterolemia Laparoscopia
- Leve
- Moderado Fosfatasa alcalina Radiología
- Grave GGT Cálculos opacos
Bradicardia (por depresión 5’NU Cálculos transparentes
del nodo senoauricular)
Colangiografía
Maladigestión y Colecistografías
malabsorción (sobre todo de
grasas)
Prueba de coagulación
Se produce hiperbilirrubinemia, en el caso de la colestasis es bilirrubina conjugada. En el caso
de la anemia hemolítica ocurre un aumento de bilirrubina libre en este caso.
COLESTASIS INTRAHEPÁTICAS HEPATOCELULAS HEREDITARIAS
Características generales:
- Hasta los 70 se diagnosticaban como hepatitis neonatal idiopática
- Enfermedades poco frecuentes
- Generalmente diagnosticadas por el pediatra
- Con sintomatología de leve a muy grave
- A veces la única solución es el trasplante
Clasificación
BRIC (BRIC1, BRIC2, BRIC 3)
- Crisis recurrentes de prurito severo
- Pérdida de peso
- No evolucionan a estados de daño hepático severo o cirrosis
PFIC (PFIC1, PFIC2, PFIC3)
- En principio colestasis recurrente
- Posteriormente permanente y de gravedad progresiva
- Esteatorrea, hepatomegalia y retraso del crecimiento
- Progresa a cirrosis hepática
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Finalmente se requiere trasplante.
2. LITIASIS BILIAR
Formación de cálculos biliares. Prevalencia 5-15% (mayor en mujeres)
Tipos de cálculos según su composición:
Colesterol (50-60%)
Factores de nucleación (mucinas, IgA)
Dismotilidad vesicular (gestación, nutrición parenteral)
Otros (falta de ejercicio, genéticos, síndrome metabólico, diabetes mellitus
tipo 2, obesidad, edad avanzada)
Pigmentarios negros (20-30%)
Cristales de bilirrubina más carbonatos cálcico, sin colesterol
Asociados a hemolisis crónica y cirrosis
Pigmentarios marrones (<30%)
Bilurrubinato cálcio + colesterol + palmitato cálcico + estearato
Asociados a infección, colangitis esclerosante, parasitosis
Patología según la localización de los cálculos
COLELITIASIS
(Cálculos en la vesícula)
COLEDOCOLITIASIS (ya han salido de la vesícula y paran en el colédoco)
(Cálculos en el colédoco)
Riesgo de colangitis
Riesgo de pancreatitis aguda (25-36%)
Tratamiento de la litiasis biliar
Colecistectomía (extirpación de la vesícula biliar)
Litotricia endoscopia
Litotricia extracorpórea (onda de choque)
Farmacológico (ácido ursodesoxicólico)
CÓLICO BILIAR
- Obstrucción de la vesícula
- Dolor de intensidad variable e irradiado a omoplato derecho
- Nauseas y vómitos
- Desencadenado tras 1-2h de una comida grasa
- Ecografía
COLECISTITIS
- Inflamación del árbol biliar final (vesícula biliar y conductos hepatícos, cístico y
colédoco)
- Obstrucción por cálculos
- Acción agresiva de los ácidos biliares
- Infección bacteriana ascendente
- Dolor intenso y prologando
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Puede irradiarse hacia la escapula derecha
- Fiebre
TUMOR MALIGNO DEL ÁRBOL BILIAR (COLANGIOCARCINOMA)
- Mucho menos frecuente que el Hepatocarcinoma
- Afecta a personas mayores ( aprox. 70 años de media)
- Se trata de un tumor muy agresivo que se detecta tarde
- En personas con otras patologías: diabetes, insuficiencia cardiaca, etc
- Tienen un pronóstico funesto (pocas expectativas de vida)
- No suelen asociarse a cirrosis y no tiene diferente incidencia entre ambos sexos
- Manifestaciones clínicas: dolor abdominal, pérdida de peso, frecuentemente signos de
obstrucción biliar (ictericia, coluria, pruritus)
- Factores de riesgo: desórdenes inflamatorios crónicos (colangitis esclerosante,
hepatolitiasis, etc), infecciones por trematodos hepáticos..
TEMA 37: FISIOPATOLOGÍA HEPÁTICA
Recordatorio sobre las funciones del hígado
1. Función digestiva: producción de bilis, que ayuda a emulsionar las grasas.
2. Función excretora: destoxificación de endobióticos como la bilirrubina y el colesterol y
xenobioticos como fármacos, toxinas.
3. Función metabólica:
a. Metabolismo de carbohidratos
b. Metabolismo de lípidos
c. Metabolismo del amonio
d. Síntesis de proteínas plasmáticas (albúmina, lipoproteínas)
4. Papel en la coagulación sanguínea (síntesis de factores de coagulación)
5. Función endocrina:
a. Síntesis y activación de hormonas
b. Degradación de hormonas
6. Función de almacén: glucógeno y vitaminas, Fe, Cu, etc
7. Función hematopoyética: en la vida fetal
1. EXPLORACIÓN DE LA FUNCIÓN HEPÁTICA
Exploración física:
- Palpación: a veces ocurre la hepatomegalia es decir el aumento del hígado y puede
palparse.
- Técnicas de imagen: ecografía, gammagrafía, TAC, fibroscan, etc.…
- Técnicas invasivas: laparoscopia, biopsia (se coge una muestra de tejido hepático para
analizarlo en el laboratorio)
Exploración funcional (bioquímicas)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- Pruebas analíticas (perfil hepático):
o Transaminasas (GOT y GPT) Lisis de hepatocitos
o Gamma glutamil transpeptidasa (GGT) cuando GPT y FA están aumentadas
indican colestasis
o Fosfatasa alcalina (FA)
o Bilirrubina (en suero y orina)
o Proteínas (albúmina)
- Pruebas de coagulación sanguínea.
- Pruebas funcionales: aclaramiento de bromosulfoftaleína (BSP)
2. HEPATITIS
Inflamación del hígado (lo más frecuentes son por virus pero hay una etiología múltiple)
Etiología múltiple:
Infección viral, agresión tóxica, autoinmune, trastornos isquémicos (que no llega sangre a la
zona del hígado), trastornos metabólicos:
o Acumulación de grasa en esteatohepatitis (por consumo abusivo de alcohol)
o Acumulación de metales (Fe, Cu)
Sintomatología: escasa e inespecífica (astenia, anorexia, febrícula) Presenta síntomas escasos y
muy poco específicos puesto que los que presentan pueden ser presentados por muchas otras
enfermedades.
HEPATITIS VÍRICAS: la inflamación es producida por virus
Característica Hepatitis A y E Hepatitis B y D Hepatitis C y G
Virus VHA VHB VHC
Transmisión Orofecal (por mal Parenteral, sexual Parenteral
estado (transmisión vertical
sociosanitario) de madre a feto)
Daño por Citopático (el virus Citolisis inmune (los Mixto (tanto por vía
mata a las células) linfocitos matan a la citopática como por
células) Citolisis inmune)
Cronificación No Sí Sí
Hepatocarcinoma No Sí Sí
Sí el sistema inmune no es capaz de destruir todos los virus va a producir hepatitis crónica y
cronificación y con el tiempo produce una cirrosis y produce Hepatocarcinoma como es en el
caso de las dos últimas.
Cualquiera de ella puede producir la muerte fulminante.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
- La hepatitis A es la responsable de la mitad de hepatitis aguda. Son las más
sintomáticas, producen trastornos digestivos, vómitos, diarrea, ictericia… Es capaz el SI
de eliminar la infección, se curan pero también se puede producir la muerte.
- En el caso de la hepatitis B es la más común, en nuestro entorno hay menos
prevalencia por la existencia de vacunas de la cual estamos vacunados. Si se adquiere
muy pronto en la vida se produce la cronificación y la formación de Hepatocarcinoma.
- Por última de la hepatitis C destacar que durante muchos años no se identificó, se ha
transmitido mucho a lo largo de la historia por transfusiones de sangre, receptores de
órganos… Es muy problemática porque no hay vacuna, y porque hasta recientemente
no ha habido tratamiento, hoy en día lo hay pero es caro.
3. CIRROSIS
Enfermedad crónica y difusa del hígado (es decir afecta a todo el hígado), que altera su
estructura (fibrosis: acumulo de tejido conectivo) y función. Estadio final e irreversible de las
lesiones hepáticas crónicas.
Causas de cirrosis:
- Fármacos y tóxicos (alcohol 50%)
- Virus hepatotóxicos (Hepatitis B, C,D)
- Obstrucción biliar
o Primaria (cirrosis biliar primaria, se cierran los conductos biliares)
o Secundaria (litiasis)
- Acumulación excesiva de metales:
o Hemocromatosis (acumulo de Fe), enfermedad de Wilson (acumulo de Cu)
- Vasculares
- Alteraciones genéticas
- Idiopática (hepatitis autoinmune, no se sabe la causa pero inicialmente es por hepatitis
autoinmune)
- NASH o esteatohepatitis no alcohólica, en el caso de la gente la cual tiene el hígado
graso.
Manifestaciones de cirrosis
- Triada de signos (pregunta de examen, define cirrosis): Necrosis celular (muerte celular),
fibrosis (respuesta defensiva del hígado y se produce acumulo de tejido conectivo por
deposición del tejido conectivo de forma alterada y desordenada) y nódulos de
regeneración (el hígado tiene capacidad de regenerarse, las células que quedan se
regeneran pero por el problema de fibrosis quedan atrapadas formando los nódulos
de regeneración que no se colocan en sus sitio)
- Hipertensión portal: por la desorganización de la fibrosis.
- Alteraciones funcionales que afectan a:
o Regulación del metabolismo energético
o Síntesis de proteínas séricas, urea, lípidos y lipoproteínas
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
o Generación del flujo de bilis
o Destoxificación de compuestos endógenos y xenobioticos
o Degradación de hormonas
o Almacenamiento de vitaminas
4. HIPERTENSIÓN PORTAL
Incremento de la presión venosa portal, que da lugar a la formación de una red extensa de
colaterales porto-sistemáticas, que derivan la sangre desde el territorio portal a la circulación
sistemática, evitando que pase por el hígado. (Mirar dibujo)
Causas
Primero se produce un aumento de la resistencia vascular:
Bloqueo presinusoidal (antes del hígado)
Bloque sinusoidal, es lo más frecuente por la desorganización y comprime la vena
porta y aumenta la presión (intrahepático), en cirrosis
Y como consecuencia del aumento de la resistencia vascular se produce un incremento del
flujo sanguíneo (hiperemia esplácnica, retención de sangre en los órganos esplácnicos porque
se produce vasodilatación por elevación del glucagón y vasodilatadores locales)
Elevación de los niveles circulantes de agentes vasodilatadores: glucagón,
vasodilatadores locales (óxido nítrico)
La sangre va a buscar vías alternativas, esas alternativas es la formación de nuevos vasos
sanguíneos de tal manera que se evita el paso por el hígado
Manifestaciones
Varices esofágicas
Ascitis
Encefalopatía hepática
4.1 VARICES ESOFÁGICAS
Varices esofágicas: son dilataciones de las venas del esófago. Producidas por anastomosis
entre las venas del estómago y las venas esofágicas
Manifestaciones:
- Sangrado: (hematemesis, gran complicación, muerte el 50%)
- Deposiciones de color negro (melena)
- Lipotimia o desmayo
- Anemia crónica
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
4.2 ASCITIS
Ascitis: acumulación de líquido en la cavidad abdominal
Manifestaciones
- Abultamiento del abdomen
- Aumento de peso
- Hinchazón de las piernas por retención de líquido
Es el primer signo de descompensación en la mayoría de los pacientes cirróticos. Se asocia con
un mal pronóstico. Cuando se produce una descompensación cirrótica el problema ya es grave.
4.3 ENCEFALOPATÍA HEPÁTICA
Encefalopatía hepática: conjunto de manifestaciones neurológicas, mentales y
electroencefalográficas, que se observa en:
Hipertensión portal: la circulación colateral porto-cava permite el acceso a la
circulación general (y al cerebro) de ciertos productos tóxicos (amoniaco, es el más culpable)
procedentes del intestino.
Insuficiencia hepática aguda
Manifestaciones:
- Astérixis (temblor aleteante, incapacidad de mantener los brazos abiertos)
- Hipertonía muscular
- Dificultad habla y escritura
- Inversión del ritmo del sueño
- Estupor, coma y muerte por edema cerebral
5. INSUFICIENCIA HEPÁTICA
Incapacidad del hígado para llevar a cabo sus funciones, implica el fracaso de todas ellas.
Causas
Destrucción de hepatocitos por agentes agresores:
Anoxia (en insuficiencia circulatoria)
Virus hepatotropos
Tóxicos (alcohol, micotoxinas, fármacos)
Hemocromatosis. Enfermedad de Wilson (acumulo de Cu)
Niveles elevados de ácidos biliares, en colestasis
Destrucción de hepatocitos por procesos auntoinmunes
Consecuencias
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Hipoglucemia, alteraciones hidroelectrolíticas
Complicaciones hemodinámicas y renales
Encefalopatía hepática
Coma y muerte (por edema cerebral progresivo)
TEMA 38: FISIOPATOLOGÍA DEL GRUPO HEMO
1. PORFIRIAS ( patologías de la síntesis del hemo)
Conjunto de alteraciones del metabolismo del grupo hemo. Deficiencia funcional de una de las
enzimas de la síntesis del hemo, que resulta parcialmente bloqueada. Su acumulan
precursores anteriores al paso afectado, con o sin deficiencia neta de síntesis de hemo. Esta
acumulación es la causa de los síntomas. Recalcar que es una deficiencia parcial funcional de
algunas de las síntesis del hemo, por lo que va haber diferentes enfermedades relacionadas
dependiendo del paso de la síntesis al que afecte.
Sí hay una deficiencia total el individuo no sería viable en su crecimiento.
Causas de las porfirias (las más frecuentes son las congénitas)
Porfirias congénitas (hereditarias): defecto enzimático de la síntesis del grupo hemo
Porfirias adquiridas:
Intoxicación por fenoles colorados que inhiben la síntesis del hemo
Intoxicación por plomo (saturnismo, se altera una de las enzimas de la síntesis
del hemo)
Deficiencias nutricionales de Fe y piridoxina
Colestasis o hepatitis virales agudas.
Manifestaciones de las porfirias
Neurológicas: crisis episódicas acompañadas de dolor abdominal agudo. Se producen por la
acumulación de los primeros metabolitos de la síntesis, es decir de los más pequeños.
(Agitación, confusión, delirio). En casos graves puede llegar a parada respiratoria y muerte
Hepáticas: cirrosis y tumores
Cutáneas: Cuando se acumulan ya precursores grandes. Fotosensibilización
Clasificación de las porfirias congénitas
La síntesis más importante del hemo se produce en la medula ósea y en el hígado.
Dependiendo del lugar de la alteración enzimática pueden ser:
Porfirias hepáticas (déficit enzimático en el hígado) Y a su vez pueden ser:
Porfirias agudas:
- Porfiria aguda intermitente (PAI)
- Porfiria de Dosse o plumboporfiria
Porfiria cutánea tarda (PCT): La que más se manifiesta. Es una manifestación cutánea tarda
(solo saberse el nombre de este tipo)
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Porfirias mixtas (tanto cutáneas como neurológicas)
- Coroporfiria hereditaria (CPH)
- Porfiria variegata (PV)
Porfirias eritropoyeticas (el déficit enzimático afecta sobre todo a la medula ósea)
- Porfiria eritropoyética congénita (PEC) o de Gunther: primera
porfirina que se descubrió también se llama porfiria motilante
produce daños graves en la piel... Caso muy raro.
- Protoporfiria eritrohepática (PPEH) (problemas con la luz solar)
Recordatorio del metabolismo de la Bilirrubina
Se forma a partir de la hemoglobina. La hemoglobina se separa por un lado la globina y por
otro el grupo hemo. Ese grupo hemo pasa a porfirina y de ahí a bilirrubina conjugada que es
poco soluble. Después se lleva al hígado unida con la albúmina y en los hepatocitos ya es
conjugada por una enzima UDP-gluconil-transferasa. La proteína transportadora es la MRP2
2. HIPERBILIRRUBINEMIAS (elevada concentración de bilirrubina en sangre)
Etiología de las hiperbilirrubinemias: depende de las alteraciones en diferentes puntos
Por aumento de la producción del pigmento. Cuando hay:
o Hemólisis (en anemias hemolíticas) se libera tanta hemoglobina que al
hígado no le da tiempo a secretar. Se acumula bilirrubina libre
Por alteraciones del transporte plasmático del pigmento
o Fármacos que desplazan a la Br de su unión con la albúmina. Se une el
fármaco a la albúmina y se acumula Br libre.
Por defectos en la conjugación del pigmento (problema en la enzima)
o Hiperbilirrubinemia neonatal: conocida como ictericia fisiológica del
recién nacido. Prácticamente todos los neonatos experimentan una
subida de Br que se debe a que la enzima es muy inmadura. Se agrava
cuanto más prematuro sea el niño.
o Síndrome de Gilbert: deficiencia congénita parcial de la enzima
conjugante. Afecta entre 2-5%. Se transmite por herencia dominante.
o Síndrome de Cliger-Najjar: hay dos tipos: el I que hay una deficiencia
total de la enzima conjugante, es muy grave. Y II que es una deficiencia
parcial. Es de herencia recesiva. Se acumula bilirrubina libre
Por trastornos en la excreción biliar del pigmento
o Colestasis obstructiva: aquí ya se produce acumulo de Br conjugada
o Síndrome de Dubin-Johnson: deficiencia en el transportador MRP2
o Síndrome de Rotor: deficiencia en el transporte intracelular del
pigmento. En estos casos se produce acumulo de Br conjugada.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Manifestaciones de las hiperbilirrubinemias
Ictericia: cuando los niveles de bilirrubina suben por encima de > 2mg/dl lo primero
que se aprecia es la ictericia (coloración amarilla de la piel y las mucosas por
acumulación en ellas de bilirrubina) se aprecia sobre todo en la esclerótica del ojo
Bilirrubina en orina (coluria): parte de la bilirrubina y sobre todo la conjugada se va a
secretar por la orina
Heces poco pigmentadas (hipocolia o acolia) ausencia de bilis. O heces bien
pigmentadas (pleicrómicas) cuando se produce exceso de producción de bilirrubina
También se produce un problema grave que es la encefalopatía por bilirrubina
(Kernícterus), cuando los niveles de Bilirrubina en sangre aumentan mucho >20mh/dl.
En este caso la Br es capaz de atravesar la barrera hematoencefálica y se une a las
neuronas y inhibe la respiración neuronal, da lugar a veces a la muerte o si el niño
sobrevive da lugar a un retraso mental irreversible.
Recordatorio de la dinámica del hierro en el organismo
El hierro se capta de manera activa en el enterocito, se transporta por la apotransferrina que
da lugar a la tranferrina y lleva el hierro a donde se necesite, bazo, medula, hígado…
Nos interesa la parte del hígado, el hierro se almacena en el hígado por la Ferritina. Hay que
destacar que se puede intercambiar cuando quiera con el plasma. Cuando hay más acumulo de
hierro se forma la hemosiderina (hemosiderosis: acumulación excesiva de hemosiderina en el
hígado). Si aumenta aún mas se deposita el ión hierro tal cual en los hepatocitos y es una
situación de hemocromatosis.
3. HEMOCROMATOSIS
La hemocromatosis si se diagnostica pronto no da problemas. Tratamiento: extracción de
sangre
Causas de hemocromatosis
Origen genético: mutación en una proteína que controla la absorción intestinal
del hierro
o Excesiva absorción intestinal de hierro
Aporte excesivo de hierro:
o Transfusiones repetidas, alimentos contaminados
Consecuencias de la hemocromatosis
El acúmulo de hierro libre en el hígado genera radicales libres (produce estrés oxidativo que
supone un daño persistente que a la larga va a producir cirrosis y las personas con cirrosis
multiplica x200 el riesgo de cáncer hepático (Hepatocarcinoma)
TEMA 39: FISIOLOGÍA Y FISIOPATOLOGÍA DE LA DIGESTIÓN Y LA ABSORCIÓN
1. LUGARES Y VÍAS DE ABSORCIÓN
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
La mayor parte de la absorción de nutrientes se produce en el intestino delgado. En la boca no
hay apenas absorción de nutrientes, desde el punto de vista de la nutrición la absorción en la
boca, esófago y estomago no hay apenas absorción. Sólo se absorben en el estómago
sustancias muy liposolubles como el alcohol o fármacos como la aspirina.
La mucosa del intestino delgado está especializada para dicha absorción porque representa
una serie de pliegues:
• Válvulas conniventes que multiplican x3 la superficie de absorción (sobretodo
profundas en el duodeno y yeyuno)
• Toda la mucosa está recubierta por vellosidades intestinales que miden
aproximadamente 1mm que multiplica x10 la superficie de absorción (estas
vellosidades no están en el estómago) y dentro de ellas hay vasos sanguíneos,
capilares, de tal manera que lo que se absorbe va a pasar a la sangre venosa,
por la venas mesentéricas, de ahí a la porta y al hígado.
Un quilifero es un vaso linfocito y de ahí pasa a la linfa. Los enterocitos son células que tapizan
el intestino y a su vez estos enterocitos tienen en la membrana apical, la que da a la luz, tiene
el borde en cepillo porque presentan una microvellosidades (1um) que multiplica x20 la
superficie de absorción. En conjunto se ha calculado que la superficie de absorción es de unos
250cm2 gracias a estos elementos.
Además de las microvellosidades tienen filamentos de actina que va a facilitar la interacción y
absorción. La absorción de nutrientes se produce sobre todo en el duodeno y yeyuno de tal
manera que al íleo no llega casi, es más bien una zona de reserva absortiva por si falla.
Pero el íleo es muy importante porque se absorben 2 cosas muy importantes. Por un lado la
vitB12 y los ácidos biliares.
Para absorberse un nutriente tiene que atravesar la membrana apical (barrera en forma de
cepillo) luego el enterocito, luego la membrana basal y de ahí al intestino y luego a la sangre.
Puede haber diferentes transportadores para una sustancia.
2. ABSORCIÓN DE CARBOHIDRATOS
Los hidratos de carbono más importantes son polisacáridos como el almidón (vegetal) y el
glucógeno (animal), celulosa su unión es en beta de tal menara que nuestras enzimas no
pueden degrada, con lo cual la celulosa forma parte de la fibra alimenticia. También son
importantes los disacáridos como la lactosa de la leche y la sacarosa. Los monosacáridos como
glucosa y fructosa principalmente. Para los polímeros de glucosa la digestión se lleva a cabo
por las α-amilasas, hemos visto la ptialina o α-amilasa para la digestión pero esta tiempo poca
importante porque se inactivaba rápidamente. Si es importante la amilasa del jugo pancreático
que produce maltosa, maltotriosa o glucosa pequeña tipo dextrinas.
Estos disacáridos se digieren por las disacarasas que están en la membrana apical de los
enterocitos. Habrá malta que rompe la maltosa, sacarasa que da glucosa y fructosa y lactasa
que da glucosa y galactosa. De tal manera que se completa la digestión de los glúcidos
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
La absorción de glúcidos tiene lugar en el duodeno y primera parte del yeyuno. La glucosa y la
galactosa entran en el enterocito transportados por Na+ (SGLT1) es un trasporte activo
secundario porque el sodio entra por un gradiente produciendo por una Na+/K+ ATPasa en la
membrana apical. Una vez en el enterocito, la otra membrana la basal se lleva por GLUT2 que
este es difusión facilitada a favor de gradiente en el caso de la fructosa utiliza GLUT5. El
transporte de glucosa en el intestino es bastante independiente de insulina, no está afectada
en personas con diabetes.
3. ABSORCIÓN DE PROTEÍNAS
Estas proteínas no solo proceden de la dieta, además también están las de las secreciones
intestinales y también muchas que proceden de las células que se descaminan de la mucosa.
Las proteínas para digerirlas se transforman en aminoácidos y para eso están las proteasas. La
inmensa mayoría de estas proteasas son endopeptidasas que rompen los enlaces peptidicos
en medio de la proteína. Mientras que algunas son exopeptidasas que rompen el enlace por el
extremo (ej: carboxi terminal o amino terminal). Tiene lugar en el duodeno y la primera mitad
del yeyuno.
Estos péptidos producen los péptidos pequeños y las que finalizan la ruptura, es la membrana
en forma de cepillo lo que pasa a aminoácidos más pequeños. Hay diferentes sistemas de
transporte cada uno tiene su propio sistema, hay 20 aminoácidos diferentes cada uno con su
sistema de transporte.
También se pueden absorber al enterocito tripeptidos y dipeptidos y luego dentro de la célula
hay peptidasas que las rompen y liberan aminoácidos que pasa ya a la sangre. Y también es
posible algunas péptidos pequeños no digeridos de todo y englobarlos en una membrana por
pinocitosis y se produce endocitosis. En el caso de naonatos se puede llevar a cabo esto
descrito, la mucosa neonatal por pinocitosis es capaz de incorporar las proteínas enteras.
Sobre todo en el calostro.
4. ABSORCIÓN DE LÍPIDOS
Los más abundantes en la dieta son los triacilgliceridos también fosfolipidos, colesterol,
vitaminas liposolubles, esteres vegetales. La digestión de lípidos es la más compleja.
Principalmente la digestión de triacilgliceridos la hacen las lipasas que son abundantes en el
jugo pancreático que da lugar a monogliceridos y ácidos grasos libres. Pero para que las lipasas
actúen se requiere que se emulsionen gracias a ácidos biliares (las gotas de grasas se juntan
con los ácidos grasos dando lugar a esta emulsión en gota pequeñas de grasas) para que luego
las enzimas sean capaces de actuar. Esos monogliceridos y ácidos grasos van a formas micelas
mixtas. Las micelas se aproximan a la membrana en borde de cepillo y facilita la absorción de
lípidos. Se absorben por difusión de la membrana. No se absorbe toda la micela, solo los
componentes lipídicos.
Dentro del enterocito hay que volver a ensamblar los triacilgliceridos también el colesterol se
esterifica. Y estos lípidos ya pasan al aparato de Golgi donde se van a ensamblar los
quilomicrones. Estos quilomicrones salen ya por exocitosis y pasan a la linfa (por poros). Las
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
únicas que no se ensamblan de nuevo son los ácidos grasos de cadena corta. La absorción
lipídica tiene lugar en el yeyuno y finales del duodeno.
5. ABSORCIÓN DE AGUA, ELECTROLITOS Y VITAMINAS
La absorción de agua se hace siguiendo osmóticamente a los electrolitos fundamentalmente al
sodio y al cloro. El Na+ se absorbe ayudando a la absorción de nutrientes (ej: NA+ -- glucosa,
Na+ -- aminoácidos, ó intercambiándose con los protones consumiendo ATP) El cloro entra
intercambiándose con bicarbonato.
El agua va a pasar a través de “tight junctions” o uniones estrechas entre las células, que son
permeables al agua, la permeabilidad va disminuyendo en el íleo y el colon. Las acuaporinas
son canales para el agua. En cuanto a las vitaminas, las vitaminas liposolubles se absorben
como los lípidos, de tal manera que se degradan de la emulsión de grasas por ácidos biliares.
Las vitaminas hidrosolubles varían de unas a otras y suelen tener su propio transporte. Y la
vitB12 para absorberse tiene que unirse al factor intrínseco y va a absorberse en el íleo.
6. SÍNDROME DE MALADIGESTIÓN Y MALABSORCIÓN
Síntomas y signos originados por el déficit de sustancias nutritivas que se produce cuando se
alteran procesos fisiológicos necesarios para la correcta digestión y absorción de los
nutrientes.
Causas de Maladigestión: alteración de los procesos de digestión
Origen gástrico: resecciones gástricas (le quitan parte del estomago de forma que pasa
al intestino partículas más grandes y no se produce bien la digestión.
Origen pancreático: pancreatitis crónicas (se libera menos jugo pancreáticos y dificulta
la digestión)
Déficit de sales biliares: colestasis, resección del íleon (el íleo es como ya vimos el
lugar específico donde se absorben los ácidos biliares)
Causas de Malabsorción: alteración ya en el proceso final de nutrientes
Disminución de la superficie de absorción: resección quirúrgica (amplias)
Lesiones de la pared intestinal: enfermedades inflamatorias crónicas y intolerancia al
gluten (enfermedad celiaca) que se produce daño en la mucosa cuando se toma gluten
Aporte sanguíneo insuficiente u obstrucción a vasos linfáticos
Consecuencias de Maladigestión y Malabsorción
La primera que se pone de manifiesto es la diarrea y que recibe un nombre especial cuando se
trata de heces ricas en grasa Esteatorrea. Y como consecuencia desnutrición y…
Déficit de absorción de: Síntoma o signo:
Vitamina D y Ca Osteomalacia, tetania
Vitamina K Hemorragias
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Hierro Anemia ferropénica
Vit B12 y ácido fólico Anemia megaloblástica
Agua y electrolitos Deshidratación, diarrea
Grasas Esteatorrea. Pérdida de peso
Hidratos de carbono Diarrea acuosa. Pérdida de peso
Proteínas Pérdida de masa muscular. Edemas
También se produce retraso en el crecimiento en caso de niños.
7. ENFERMEDADES INFLAMATORIAS DEL INTESTINO
Hace referencia a inflamaciones crónicas de la mucosa o submucosa. La colitis ulcera es de las
más peligrosa porque también está asociada con incidencia el cáncer de colon (diagnosticado
en personas jóvenes de 15-30 años)
Características ENFERMEDAD DE CROHN COLITIS ULCEROSA
Localización Submucosa Mucosa
Extensión Lesiones diseminadas Lesiones continuas
Zona Ileon, colon Recto y colon
Diarrea Común Común
Sangre en heces Rara Común
Fístulas y abscesos Comunes Raros
Aparación de cáncer Rara Común
Se utiliza el colondoscopio para hacer colondoscopias para ver si existen o no lesiones
TEMA 40: ASPECTOS FISIOLÓGICOS DEL METABOLISMO
1. METABOLISMO ENERGÉTICO
Metabolismo: conjunto de procesos químicos y físicos implicados en:
- Producción de energía a partir de fuentes endógenas y exógenas
- Síntesis y degradación de componentes estructurales y funcionales de los tejidos
- Eliminación de los productos de deshecho
Aporte de energía (alimentos9: 2500 kcal/día (rango 1500-5000)
Gasto de energía: 39 kcal/kg (hombre), 34 kcal/kg (mujer). De estas:
- 20 kcal/kg en metabolismo basal, en completo reposo
- 15% más tras las comidas (acción dinámica específica de los alimentos)
En una actividad física alta se produce un aumento entre un 30-35% el consumo de calorías. En
el caso de personas que su ejercicio es nulo se puede bajar entre 10-15%
Alimento Ingesta diaria (g) Energía aportada
Hidratos de carbono 150 4
Grasas 100 9
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Proteínas 100 (con 35 sería sufic.) 4
2. HOMEOSTASIS GLUCÍDICA
En el metabolismo glucídico el componente central es la glucosa y el hígado el órgano clave.
La glucosa la quemamos para obtener lactato, por el proceso denominado glucolisis
anaerobia, que se produce en glóbulos rojos, medula renal y musculo esquelético que son
productores de lactato. En el caso de la glucolisis aerobia se da en el sistema nervioso,
músculo esquelético, tejido adiposo y muchos otros órganos. Cuando hay mucha glucosa
vamos a almacenar esa glucosa en forma de glucógeno, proceso denominado glucogénesis
que permite como hemos dicho almacenar ese exceso de glucosa. Es un proceso reversible, su
proceso reversible se llamada glucogenolisis, hay una particularidad, y es que el músculo la
glucosa que almacena la etiqueta de tal manera que no va a compartir pero tanto el hígado
como la médula renal mandan la glucosa a la sangre y a los órganos que la necesiten.
Se puede obtener glucosa a partir de fuentes no glucídicas, este proceso se denomina
gluconeogénesis (hígado y medula renal), se puede hacer a partir de aminoácidos, glicerol y
lactato. Está muy bien regulado.
3. HOMEOSTASIS LIPÍDICA
Los lípidos también son componentes esenciales en la dieta, los triglicéridos son los más
importantes, también destaca el colesterol porque a partir de él se sintetizan las sales biliares y
hormonas esteroideas. El tejido donde más se produce la síntesis de triglicéridos a partir de
glicerol y de ácidos grasos es en el tejido adiposo por un proceso denominado lipogénesis. El
tejido adiposo va a proteger a muchos órganos del cuerpo y también hay una capa de grasa
que actúa como aislante térmico.
El proceso de lipolisis consiste en la ruptura de triglicéridos para dar ácidos grasos y glicerol.
Esos ácidos grasos se mandan al músculo la mayor parte, ya que consigue energía con la β-
oxidación para producir después CoA. Y ese CoA es utilizado por el hígado para producir
cuerpos cetónicos (el cerebro los utiliza como alternativa)
4. HOMEOSTASIS DE LAS PROTEÍNAS
La síntesis de proteínas es básica y se da en todas las células del cuerpo. Hay dos órganos, el
musculo y el hígado, que realizan la síntesis más importante. Los aminoácidos los obtenemos
de las proteínas de los alimentos, hay 8 aminoácidos esenciales y el resto se pueden producir
por transaminación. La transaminación consiste en juntar un grupo amino con otro y dar así
los aminoácidos.
Los aminoácidos pueden quemarse para dar energía, el grupo amino si no se utiliza para la
transaminación, se convierte en amonio y ese amonio se elimina por la urea.
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
lOMoARcPSD|2558484
Su distribución está prohibida | Descargado por yesica sauñe tapia (ysaunetapia@gmail.com)
You might also like
- Hipertension Pulmonar Presentacion AcbDocument24 pagesHipertension Pulmonar Presentacion AcbAlexis Fco Cerda BizamaNo ratings yet
- Pancreatitis AgudaDocument32 pagesPancreatitis AgudaGastrocirugia SIGLO XXINo ratings yet
- Muerte SubitaDocument39 pagesMuerte SubitaYohana Orozco RestrepoNo ratings yet
- Cardiopatia HipertensivaDocument20 pagesCardiopatia HipertensivaCelim ChauNo ratings yet
- Manejo de crisis hipertensivaDocument6 pagesManejo de crisis hipertensivapetraNo ratings yet
- Casos Clinicos de InfartoDocument5 pagesCasos Clinicos de Infartoalfonso soledispaNo ratings yet
- Resumen Epoc Con Gold 2019 OkDocument11 pagesResumen Epoc Con Gold 2019 OkTania Moreno100% (1)
- Formacion de La OrinaDocument5 pagesFormacion de La OrinaFernanda OvandoNo ratings yet
- Evaluación prequirúrgica pacientes adultosDocument14 pagesEvaluación prequirúrgica pacientes adultosPanchito2000No ratings yet
- Tarea 6Document75 pagesTarea 6GIBRAN gutierrezNo ratings yet
- Insuficiencia Cardiaca Seminario Med VIDocument17 pagesInsuficiencia Cardiaca Seminario Med VIAbel BriceñoNo ratings yet
- Historia Clínica Cardiovascular: Datos DemográficosDocument54 pagesHistoria Clínica Cardiovascular: Datos DemográficosDante_Must_Die_No ratings yet
- Banco de PreguntasDocument4 pagesBanco de PreguntasJP Anthony Fuertes100% (1)
- Insuficiencia CardíacaDocument10 pagesInsuficiencia CardíacaMelissa T100% (1)
- HiponatremiaDocument8 pagesHiponatremiaMiguel Espinosa SaenzNo ratings yet
- Infecto Pal Insecto 4Document132 pagesInfecto Pal Insecto 4RodrigoNo ratings yet
- Aneurisma AortaDocument31 pagesAneurisma AortaRonnyNo ratings yet
- Apunte ITU MedichiDocument12 pagesApunte ITU MedichiFranco SaavedraNo ratings yet
- Sindrome Nefrítico-NefroticoDocument12 pagesSindrome Nefrítico-NefroticokeyberliNo ratings yet
- Endocrino PDFDocument53 pagesEndocrino PDFCristi RojasNo ratings yet
- Introducción a las enfermedades infecciosas y su impactoDocument129 pagesIntroducción a las enfermedades infecciosas y su impactoRodrigoNo ratings yet
- IS en El Paciente Que Ingresa, Qué Suspender y Qué MantenerDocument8 pagesIS en El Paciente Que Ingresa, Qué Suspender y Qué MantenerCristi RojasNo ratings yet
- Cerebro Perdedor de SalDocument37 pagesCerebro Perdedor de SalMEAPCO100% (1)
- Medicina Interna Renal ResumenDocument54 pagesMedicina Interna Renal ResumenSharan MalkaniNo ratings yet
- Tema 52 Anatomía y Fisiología de Los Aparatos Digestivo y Urinario Humanos. Hábitos Saludables. Principales EnfermedadesDocument18 pagesTema 52 Anatomía y Fisiología de Los Aparatos Digestivo y Urinario Humanos. Hábitos Saludables. Principales EnfermedadesFranTraseira0% (1)
- Infecto Pal Insecto 2Document136 pagesInfecto Pal Insecto 2RodrigoNo ratings yet
- Seminarios de InfectoDocument91 pagesSeminarios de InfectoRodrigoNo ratings yet
- Minilibro MedintDocument108 pagesMinilibro MedintanoNo ratings yet
- Copia de Resumen ICDocument42 pagesCopia de Resumen ICBarbara BlancoNo ratings yet
- Alteraciones Del Equilibrio Hidrosalino DR RoesslerDocument19 pagesAlteraciones Del Equilibrio Hidrosalino DR RoesslerSofia SimpertigueNo ratings yet
- TumoresAnorectalesDocument70 pagesTumoresAnorectalesKarolineJaraNo ratings yet
- Dislipemias AmfDocument12 pagesDislipemias AmfMiguel RobresNo ratings yet
- Tratamiento de La Tuberculosis PulmonarDocument32 pagesTratamiento de La Tuberculosis PulmonarLuis Daniel Valladares VijilNo ratings yet
- Enfermedades de La AortaDocument17 pagesEnfermedades de La AortaDiana Chura Sequeiros50% (2)
- Ab - Fsp-Pràctica Acido Base-Whc-2020Document9 pagesAb - Fsp-Pràctica Acido Base-Whc-2020Bastian Muller0% (1)
- Sindrome de Stevens JhonsonDocument6 pagesSindrome de Stevens Jhonsonreynaldo100% (3)
- Diagnóstico y tratamiento de la tuberculosisDocument12 pagesDiagnóstico y tratamiento de la tuberculosisLuisa Adriana Ríos CandilaNo ratings yet
- Guía completa del EKGDocument82 pagesGuía completa del EKGAndres PalaciosNo ratings yet
- Resumen Medicina Interna I Examen Teórico 1 PDFDocument100 pagesResumen Medicina Interna I Examen Teórico 1 PDFViicky SoledadNo ratings yet
- Casos Clinicos en Medicina Interna GastroDocument5 pagesCasos Clinicos en Medicina Interna GastroLuz Estefany Huaman MachacaNo ratings yet
- CardiopatiaisquemicaDocument54 pagesCardiopatiaisquemicaSofíaBejaranoIngarNo ratings yet
- Casos Clinicos - Medicina IiDocument45 pagesCasos Clinicos - Medicina IiJhosep Quispe NuñuveroNo ratings yet
- Tratamiento pancreatitis agudaDocument10 pagesTratamiento pancreatitis agudaYearim Montecinos FernándezNo ratings yet
- Semiologia CardiovascularDocument74 pagesSemiologia CardiovascularDiego Omar Toledo MercadoNo ratings yet
- Semiología Cardíaca PatológicaDocument55 pagesSemiología Cardíaca PatológicaAndres HuamánNo ratings yet
- Hipotiroidismo SubclinicoDocument6 pagesHipotiroidismo SubclinicoJuan NamikazeNo ratings yet
- Mieloma Multiple TratamientoDocument80 pagesMieloma Multiple TratamientoAlexis VegaNo ratings yet
- Sindrome Hiperglucemico Hiperosmolar No CetosicoDocument5 pagesSindrome Hiperglucemico Hiperosmolar No CetosicoHeiser LlanosNo ratings yet
- Neumonía de Focos MultiplesDocument17 pagesNeumonía de Focos MultiplesedgarfooNo ratings yet
- U.M.A.E. Hospital DE Especialidades DR. Antonio Fraga MouretDocument30 pagesU.M.A.E. Hospital DE Especialidades DR. Antonio Fraga MouretalfjargarNo ratings yet
- Retinopati Üa Diabe Ütica y EmbarazoDocument15 pagesRetinopati Üa Diabe Ütica y EmbarazoInternational Medical PublisherNo ratings yet
- Caso Clínico N°1 Hemodinamia (Fisiología II)Document4 pagesCaso Clínico N°1 Hemodinamia (Fisiología II)Andres HernandezNo ratings yet
- Podevin2014 PDFDocument6 pagesPodevin2014 PDFFernando FariasNo ratings yet
- HIPONATREMIADocument14 pagesHIPONATREMIAGustavo CarraroNo ratings yet
- Cardiopatías Congénitas CianóticasDocument15 pagesCardiopatías Congénitas CianóticasConstanza Barrera Riquelme100% (1)
- 02.021 Protocolo Diagnóstico y Terapéutico Del Coma MixedematosoDocument3 pages02.021 Protocolo Diagnóstico y Terapéutico Del Coma MixedematosoGustavo AraujoNo ratings yet
- Cómo conseguir un observership médicoDocument2 pagesCómo conseguir un observership médicoDavid De Jesus Ramirez FrontanyNo ratings yet
- HipocalcemiaDocument44 pagesHipocalcemiaCariTo MondacaNo ratings yet
- Jcaminero Taller TB 19Document89 pagesJcaminero Taller TB 19Lulu Mendoza RodriguezNo ratings yet
- Respiratorio Semiología y GasesDocument8 pagesRespiratorio Semiología y GasesCatalina JavieraNo ratings yet
- GigantismoDocument15 pagesGigantismosheccidcaarpetNo ratings yet
- WW ApUNTES URINARIO Y HOMEOSTASISDocument9 pagesWW ApUNTES URINARIO Y HOMEOSTASISalvaroNo ratings yet
- 02 - Evolución de Los Derechos HumanosDocument25 pages02 - Evolución de Los Derechos HumanosYesica StNo ratings yet
- 2poweritu 131107095543 Phpapp01Document57 pages2poweritu 131107095543 Phpapp01mesiah666No ratings yet
- Seminario 3 Bacteriología 2° Cuatrimestre 2017 PDFDocument67 pagesSeminario 3 Bacteriología 2° Cuatrimestre 2017 PDFShintia FiorelaNo ratings yet
- Resumen Microbiologia GeneralidadesDocument152 pagesResumen Microbiologia GeneralidadesYesica StNo ratings yet
- Asis 2018Document6 pagesAsis 2018Yesica StNo ratings yet
- Fármacos Diuréticos y AntidiuréticosDocument17 pagesFármacos Diuréticos y AntidiuréticosonenytaNo ratings yet
- Aparato UrinarioDocument49 pagesAparato UrinarioYesica StNo ratings yet
- Seminario 3 Bacteriología 2° Cuatrimestre 2017 PDFDocument67 pagesSeminario 3 Bacteriología 2° Cuatrimestre 2017 PDFShintia FiorelaNo ratings yet
- Ética y MoralDocument7 pagesÉtica y MoralYesica StNo ratings yet
- IR PosrrenalDocument2 pagesIR PosrrenalYesica StNo ratings yet
- Ejercicio 1 2Document2 pagesEjercicio 1 2Yesica StNo ratings yet
- 3594 14943 4 PBDocument2 pages3594 14943 4 PBYesica StNo ratings yet
- Tesis Protocolo de Atención en Pacientes Con Enfermedad Tiroidea 2007 Ursula MartínDocument87 pagesTesis Protocolo de Atención en Pacientes Con Enfermedad Tiroidea 2007 Ursula MartínYesica StNo ratings yet
- Practica General Ne FroDocument4 pagesPractica General Ne FroPerla Carrasco BatistaNo ratings yet
- Formacion de La OrinaDocument2 pagesFormacion de La OrinaAlonso PMNo ratings yet
- Sistema NefrourológicoDocument36 pagesSistema NefrourológicoOscar ChavezNo ratings yet
- Marco Teorico Del RiñonDocument8 pagesMarco Teorico Del RiñonLorena Estefani Cespedes ChavezNo ratings yet
- Filtración glomerular: proceso renal claveDocument11 pagesFiltración glomerular: proceso renal claveAracelly ReyesNo ratings yet
- El Aparato ExcretorDocument6 pagesEl Aparato ExcretorSidia Marleny Pineda OrtizNo ratings yet
- Fisiología RenalDocument19 pagesFisiología Renaljuan pablo ospinaNo ratings yet
- TESIS. CAPITULO I y II Con Cuadro CorregidoDocument26 pagesTESIS. CAPITULO I y II Con Cuadro Corregidoblack_angel_swanNo ratings yet
- Fisiología RenalDocument28 pagesFisiología RenalValeria Abigail Vega ReynaNo ratings yet
- Anatomía - NefronaDocument7 pagesAnatomía - NefronaMariela VQ100% (1)
- Componentes Del Sistema UrinarioDocument3 pagesComponentes Del Sistema UrinarioNidia Millán Salazar50% (2)
- Anatomía y Fisiología AnimalDocument30 pagesAnatomía y Fisiología AnimalGerson GrNo ratings yet
- Guía de Práctica de HistologíaDocument79 pagesGuía de Práctica de HistologíaPiero Eduardo Ponce Lingán100% (1)
- Cto Medicina 2022/23Document50 pagesCto Medicina 2022/23LauraNo ratings yet
- Documento Tarea AnatomiaDocument6 pagesDocumento Tarea AnatomiaYoceling Lisbeth Pinto OrdoñezNo ratings yet
- O A ExcretorDocument11 pagesO A ExcretorSamuel De La CruzNo ratings yet
- Examen de Ciencias NaturalesDocument15 pagesExamen de Ciencias NaturalesIGHNAONo ratings yet
- Informe Sistema RenalDocument4 pagesInforme Sistema RenalPauloNo ratings yet
- Marcia RenalDocument27 pagesMarcia Renaltienda ecoNo ratings yet
- Formacion de La OrinaDocument9 pagesFormacion de La OrinaLuzmila Levano VillanuevaNo ratings yet
- Funciones: Vena Cava AortaDocument11 pagesFunciones: Vena Cava AortaMonse AlcalaNo ratings yet
- Glomerulonefritis Post InfecciosaDocument16 pagesGlomerulonefritis Post InfecciosaFrancisco Javier Madrid RuizNo ratings yet
- Fisiología Del Aparato RenalDocument150 pagesFisiología Del Aparato RenalValeriaNo ratings yet
- Nefrona, Partes e HistologíaDocument2 pagesNefrona, Partes e HistologíaSaul Flores OcampoNo ratings yet
- Fisiología RenalDocument6 pagesFisiología RenalMaria Fernanda julioNo ratings yet
- Anatomía sistema respiratorioDocument30 pagesAnatomía sistema respiratorioyoglen100% (1)