Professional Documents
Culture Documents
123dok Penerapan+Metode+Spektrofotometri+Ultraviolet+Pada+Penetapan+Amlodipin+Besilat+dalam+Sediaan+Tablet PDF
Uploaded by
Khaerul Fadlil MOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
123dok Penerapan+Metode+Spektrofotometri+Ultraviolet+Pada+Penetapan+Amlodipin+Besilat+dalam+Sediaan+Tablet PDF
Uploaded by
Khaerul Fadlil MCopyright:
Available Formats
Lampiran 1.
Perhitungan Persamaan Regresi Amlodipin Besilat BPFI
No X Y XY X2 Y2
1 0 0 0 0 0
2 16 0,187 2,992 256 0,035
3 24 0,261 6,264 576 0,068
4 33 0,347 11,104 1024 0,119
5 40 0,437 17,48 1600 0,196
6 48 0,517 24,816 2304 0,269
Σ 160 1,749 62,656 5760 0,687
Rata-rata 26,67
n∑ XY − ∑ X ∑ Y
a=
n∑ X 2 − (∑ X ) 2
6 × 62,656 − 160 × 1,746
=
6(5760) − (160) 2
= 0,010778
b= Y −aX
= 0,291- (0,010778) (26,67)
= -0,003764
Maka persamaan regresinya adalahY= 0,010778 x-0,003764
∑ XY − ∑ X .∑ Y / n
[∑ X − ∑ ( X ) / n][Y −∑ (Y ) ]
r=
2 2 2 2
/n
62,656 − 160 × 1,746 6
=
5760 − (160)2
0,687 − 1,74612
6 6
16,096
= = 0,9992
16,108
41
Universitas Sumatera Utara
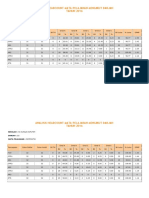
Lampiran 2. Data Kadar Amlodipin Besilat Sediaan Tablet
Penimbang Konsentrasi Konsentrasi
Nama Setara Absorban
an Teoritis Perolehan Kadar%
Sediaan (mg) si
(mg) (mcg/ml) (mcg/ml)
Amlodipin 584 19,98 0,3723 35,96 34,19 94,71
besilat 585 20,02 0,3755 36,04 34,49 95,70
Generik 583 19,94 0,3755 35,90 34,49 95,73
(PT. 585 20,01 0,3683 36,03 33,82 93,56
Hexpharm 584 19,98 0,3783 35,95 34,75 96,26
Jaya) 584 19,98 0,3765 35,97 34,58 95,79
203 20,29 0,3875 36,52 35,60 97,11
204 20,38 0,3817 36,68 35,06 95,22
Tensivask
205 20,40 0,3779 36,72 34.71 94,16
(Dexa
203 20,28 0,3676 36,50 33,75 92,11
Medika)
204 20,29 0,3804 36,68 34,94 95,31
203 20,29 0,3774 36,52 34,66 94,54
357 20,01 0,3763 36,01 34,56 95,60
358 20,04 0,3783 36,07 34,07 95,97
Normoten 359 20,10 0,3710 36,18 35,42 93,81
(Soho) 358 20,04 0,3856 36,07 34,28 97,82
359 20,10 0,3733 36,18 34,28 94,38
357 19,98 0,3733 35,96 34,32 94,96
256 20,06 0,3838 36,10 35,26 97,28
Lopiten 258 20,22 0,3838 36,26 35,26 96,52
(Guardian 255 19,98 0,3783 35,96 34,75 96,26
Pharmata 256 20,06 0,3718 36,10 34,14 94,19
ma 257 20,14 0,3810 36,25 35,00 96,18
255 19,98 0,3792 35,96 34,83 96,48
42
Universitas Sumatera Utara
Lampiran 3. Perhitungan Statistik Kadar Amlodipin Besilat Pada Generik
Hexpharm Jaya
No Kadar [ X ] (%) X−X (X − X ) 2
1 94,71 -0,581 0,337561
2 95,70 0,409 0,167201
3 95,73 0,439 0,192721
4 93,56 -0,731 2,996361
5 96,26 0,969 0,938961
6 95,79 0,499 0,249001
X = 95,291 ∑ = 4,881886
SD =
∑ ( X − Xi) 2
=
4,881886
= 0,9881
n −1 6 −1
Jika taraf kepercayaan 99% dengan nilai α = 0,01 ;=6, dk =5, dari daftar tabel
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t =
SD
n
t hitung 1 : − 0,581 = −1,4402
0,4034
t hitung 2 :
0,409 = 1,0138
0,4034
t hitung 3 :
0,439 = 1,0882
0,4034
t hitung 4 :
− 1,731 = −4,2910 (data ditolak)
0,4034
t hitung 5 :
0,969 = 2,4020
0,4034
t hitung 6 :
0,499 = 1,2369
0,4034
43
Universitas Sumatera Utara
Lampiran 3. (Lanjutan)
Karena thitung 4 ≤ ttabel maka data ditolak, selanjutnya dilakukan pengujian
terhadap data yang dianggap tidak menyimpang.
No Kadar [ X ] (%) X−X (X − X ) 2
1 94,71 -0,928 0,861184
2 95,70 0,062 0,003849
3 95,73 0,092 0,008464
4 96,26 0,622 0,386884
5 95,79 0,152 0,023104
X = 95,638 ∑ = 1,28348
SD =
∑(X − X ) 2
=
1,28348
= 0,5664
n −1 5
Jika taraf kepercayaan 99% dengan nilai α = 0,01; n = 5; dk = 4, dari daftar tabel
distribusi t di peroleh ttabel = 4,6040
X−X
t =
SD
n
t hitung 1 : − 0,928 = −3,6636
0,2533
t hitung 2 :
0,062 = 0,2447
0,2533
t hitung 3 :
0,092 = 0,3632
0,2533
t hitung 4 :
0,622 = 2,45555
0,2533
t hitung 5 :
0,152 = 0,6000
0,2533
44
Universitas Sumatera Utara
Lampiran 3. (Lanjutan)
Karena thitung ≤ ttabel maka data diterima, maka kadar sebenarnya terletak antara :
SD
µ = X ± t(1-1/2α)dk x
n
0,5564
= 95,638 ± ( 4,6040 x )
5
= 95,638% ± 1,1454%
45
Universitas Sumatera Utara
Lampiran 4. Perhitungan Statistik Kadar Amlodipin Besilat Dalam Tablet Tensivask PT.
Dexa Medika
No Kadar [ X ] (%) X−X (X − X ) 2
1 97,11 2,37 5,6169
2 95,22 0,48 0,2304
3 93,81 -0,58 0,3364
4 97,82 -2,63 6,9169
5 94,96 0,57 0,3249
6 94,96 -0,2 0,04
X =95,42 ∑ = 13,4655
SD =
∑ ( X − Xi) 2
=
13,4655
= 1,6410
n −1 5
Jika taraf kepercayaan 99% dengan nilai α = 0,01 ;=6, dk = 5, dari daftar tabel
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t =
SD
n
t hitung 1 : 2,37 = 3,5378
0,6699
t hitung 2 :
0,48 = 0,7165
0,6699
t hitung 3 :
− 0,58 = −0,8658
0,6699
t hitung 4 :
− 2,63 = −3,9259
0,6699
t hitung 5 :
0,57 = 0,8508
0,6699
t hitung 6 :
− 0,2 = −0,2985
0,6699
46
Universitas Sumatera Utara
Lampiran 4. (Lanjutan)
Karena semua data thitung ≤ ttabel, maka data diterima
Maka kadar sebenarnya terletak antara:
μ= X ± t (1−1 / 2α ) dk x SD / n
1,6410
= 94,74 % ± 4,0321 × %
6
= 94,74% ± 2,7011%
47
Universitas Sumatera Utara
Lampiran 5. Perhitungan Statistik Kadar Amlodipin Besilat Dalam Tablet Normoten
(Soho)
No Kadar [ X ] (%) X−X (X − X ) 2
1 95,60 0,18 0,0324
2 95,97 0,55 0,3025
3 93,81 -1,61 2,5921
4 97,82 2,4 5,76
5 94,38 -1,04 1,0816
6 95,96 -0,46 0,2116
X =95,42 ∑ = 9,9802
SD =
∑ ( X − Xi) 2
=
9,9802
= 1,4128
n −1 5
Jika taraf kepercayaan 99% dengan nilai α = 0,01 ;=6, dk=5, dari daftar tabel
distribusi t diperoleh nilai t tabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t =
SD
n
t hitung 1 : 0,18 = 0,3121
0,5767
t hitung 2 :
0,55 = 0,9537
0,5767
t hitung 3 :
− 1,61 = −2,7917
0,5767
t hitung 4 :
2,4 = 4,1616 (data ditolak)
0,5767
t hitung 5 :
− 1,04 = −1,8033
0,5767
t hitung 6 :
− 0,46 = −0,7976
0,5767
48
Universitas Sumatera Utara
Lampiran 5. (Lanjutan)
Karena thitung ≤ ttabel maka data ditolak, selanjutnya dilakukan pengujian terhadap
data yang dianggap tidak menyimpang.
No Kadar [ X ] (%) X−X (X − X ) 2
1 95,60 0,66 0,4356
2 95,97 -1,03 1,0609
3 93,81 -1,13 1,2769
4 94,38 -0,56 0,3136
5 95,96 -0,02 0,0004
X =94,94 ∑ = 3,0874
SD =
∑(X − X ) 2
=
3,0874
= 0,8785
n −1 4
Jika taraf kepercayaan 99% dengan nilai α = 0,01; n = 5; dk = 4, dari daftar tabel
distribusi t diperoleh nilai ttabel = 4,6040
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t hitung =
SD / n
t hitung 1 : 0,66 = 2,6695
0,4233
t hitung 2 :
1,03 = 2,6221
0,4233
t hitung 3 :
0,56 = −1,4256
0,4233
49
Universitas Sumatera Utara
t hitung 4 :
− 0,56 = −1,4256
0,4233
t hitung 5 :
− 0,22 = 0,0509
0,4233
Lampiran 5. (Lanjutan)
Karena semua data thitung ≤ ttabel maka data ditolak, selanjutnya dilakukan
pengujian terhadap data yang dianggap tidak menyimpang.
Maka kadar sebenarnya terletak antara:
μ= X ± t (1−1 / 2α ) dk x SD / n
0,8785
= 94,94 % ± 4,6040 × %
5
= 94,94% ± 1,8084 %
50
Universitas Sumatera Utara
Lampiran 6. Perhitungan Statistik Kadar Amlodipin Besilat Dalam Tablet Lopiten
(Guardian Pharmatama)
No Kadar [ X ] (%) X−X (X − X ) 2
1 97,28 1,13 1,2769
2 96,52 0,37 0,1369
3 96,26 0,11 0,0121
4 94,19 -1,96 3,8416
5 96,18 0,03 0,0009
6 96,48 0,33 0,1089
X =96,15 ∑ = 5,3773
SD =
∑ ( X − Xi) 2
=
5,3773
= 1,0370
n −1 5
Jika taraf kepercayaan 99% dengan nilai α = 0,01 ;=6, dk=5, dari daftar tabel
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t =
SD
n
t hitung 1 : 1,13 = 2,6695
0,4233
t hitung 2 :
0,37 = 0,8740
0,4233
t hitung 3 :
0,11 = 0,2598
0,4233
t hitung 4 :
− 1,96 = −4,6302 (data ditolak)
0,4233
t hitung 5 :
0,03 = 0,0708
0,4233
51
Universitas Sumatera Utara
t hitung 6 :
0,33 = 0,7795
0,4233
Lampiran 6. (Lanjutan)
Karena thitung ≤ ttabel maka data ditolak, selanjutnya dilakukan pengujian terhadap
data yang dianggap tidak menyimpang.
No Kadar [ X ] (%) X−X (X − X ) 2
1 97,28 0,736 0,5416
2 96,52 -0,024 0,0005
3 96,26 -0,284 0,0806
4 96,18 -0,364 0,1324
5 96,48 -0,064 0,0040
X =96,544 ∑ = 0,75952
SD =
∑(X − X ) 2
=
0,75952
= 0,4357
n −1 4
Jika taraf kepercayaan 99% dengan nilai α = 0,01; n = 5; dk = 4, dari daftar tabel
distribusi t diperoleh nilai ttabel = 4,6040
Data ditolak jika thitung ≥ ttabel atau thitung ≤ -ttabel
X−X
t hitung =
SD / n
t hitung 1 : 0,73 = 3,7782
0,1942
t hitung 2 :
− 0,02 = −0,1232
0,1942
t hitung 3 :
− 0,28 = −1.4579
0,1942
t hitung 4 :
0,36 = −1,8685
0,1942
t hitung 5 :
0,05 = −0,3285
0,1942
52
Universitas Sumatera Utara
Lampiran 6. (Lanjutan)
Karena semua data ttabel ≤ thitung atau≤ ttabel maka data diterima.
Maka kadar sebenarnya terletak antara:
μ= X ± t (1−1 / 2α ) dk x SD / n
0,4357
= 96,54 % ± 4,6040 × %
5
= 96,54% ± 0,896 %
53
Universitas Sumatera Utara
Lampiran 7. Perhitungan Konsentrasi Pengukuran
Diketahui : Nilai Absorptivitas spesifik (A 11 = 119a)
Tebal sel (b) = 1cm
A
c = 1
A xb
1
0,4343
c = = 0,036495 g/ml
119.1
c = 3649 μg/ml
c = 36,49 μg/ml
Konsentrasi untuk pengukuran panjang gelombang digunakan 36,49 mcg/ml.
54
Universitas Sumatera Utara
Lampiran 8.Contoh Perhitungan Penimbangan Sampel
Berat 20 tablet = 3539,2 g
Kandungan Amlodipin Besilat pada etiket = 10 mg
Dibuat larutan uji dengan kadar lebih kurang 36 μg/ml.
Ditimbang serbuk setara dengan 20 mg amlodipin besilat, maka berat sampel yang
20mg
ditimbang adalah = × 3539,2mg
20 × 13,87
= 255,16 mg
Sampel yang telah ditimbang dimasukkan dalam labu ukur 50 ml, lalu dilarutkan dalam
metanol dan cukupkan dengan akudes sampai garis tanda, dikocok homogen.
20,06mg
Kadar larutan uji = × 1000 = 402,2 µg / ml
50ml
Kemudian dipipet 4,5 ml dari larutan uji, lalu dimasukkan kedalam labu ukur 50 ml,
dilarutkan dengan pelarut Metanol, dicukupkan dengan akuades sampai garis tanda dan
dikocok sampai homogen.
55
Universitas Sumatera Utara
Lampiran 9. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Persamaan garis regresi: Y =0,010778 X – 0,003764
Konsentrasi Luas
No (µg/ml) Puncak Yi Y - Yi (Y – Yi)2
X Y
1. 0 0 0 0 0
2. 16 0,187 0,1769 0,0101 0,00010201
3. 24 0,261 0,2624 -0,0014 0,00000196
4. 32 0,347 0,3485 -0,0015 0,00000225
5. 40 0,437 0,4348 0,0022 0,00000484
6. 48 0,517 0,5211 -0,0041 0,00001681
Ʃ 160 1,749 0,00012787
Rata-rata
∑ (Y − Yi)
2
S = n−2
0,00012786
=
6−2
= 0,0056
LOD = 3 xSB LOQ = 10 xSB
Slope Slope
3x0,0056 10x0,0056
= =
0,010778 0,010778
= 1,5587 µg/ml = 5,1957 µg/m
56
Universitas Sumatera Utara
14. Nilai Distribusi t
Lampiran 10.
57
Universitas Sumatera Utara
14. Nilai Distribusi t
Lampiran 10.
58
Universitas Sumatera Utara
Lampiran 10.Tabel Distribusi t
59
Universitas Sumatera Utara
Lampiran . Gambar Timbangan analitik
Gambar 5. Timbangan Analitik
60
Universitas Sumatera Utara
DAFTAR PUSTAKA
Anonim. (2010). Epidemilogi Hipertensi di Indonesia. Tanggal 28 Agustus 2010.
http://www.hiperensiindonesia.or.id
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen
Kesehatan Republik Indonesia. Hal. 1133
Day, R.A., dan Underwood, A.L. (1999). Analisis Kimia Kuantitatif. Penerjemah:
Pujaatmaka Edisi ke V. Jakarta: Erlangga. Hal. 393.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi.
Padang: Andalas University Press. Hal. 1.
Gandjar, I.G., dan Rohman, A. (2009). Kimia Farmasi Analisis. Cetakan IV.
Yogyakarta: Pustaka Pelajar. Hal. 13.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian.1 (3):117-
133.
Holme, D.J., dan Peck, H. (1983). Analytical Niochemistry. London: Longman.
Hal. 40.
ISFI. (2008). ISO Farmakoterapi. Jakarta: Penerbit PT. ISFI. Hal. 119.
Katzung, B.G. (2001). Farmakologi Dasar dan Klinik. Penerjemah dan Editor
Bagian Farmakologi Fakultas Kedokteran Universitas Airlangga. Edisi I.
Jakarta: Penerbit Salemba Medika. Hal. 158.
Moffat, A.C. (2005). Clark`s Isolation and Identification of Drugs and Poisons.
Edisi 3. London: The Pharmaceutical Press. Hal. 1157-1158.
Mycek, M.J., Harvey, R.A., dan Champe, C.C. (2001). Farmakologi Ulasan
Bergambar. Lippincott`s Illustrated Reviews: Pharmacology. Penerjemah
Azwar Agoes. Edisi II. Jakarta: Penerbit Widya Medka. Hal. 411-412.
Roth, J.H., dan Blaschke, G. (1998). Analisis Farmasi. Penerjemah: Kisman.
Yogyakarta: UGM Press. Hal. 355-357.
Shargel, L. (1985). Biofarmasetika Dan Farmakokinetika Terapan. Edisi II
Penerjemah Fasich. Surabaya: Penerbit Universitas Airlangga. Hal. 16.
Satiadarma, K. (2004). Azas Pengembangan Prosedur Analisis. Surabaya:
Airlangga University Press. Hal. 87-91.
39
Universitas Sumatera Utara
Tan, T.H., dan Rahardja. K (2002). Obat-obat Penting. Jakarta: Penerbit PT. Elek
Media Komputindo. Hal. 308-313.
The United States Pharmacopeia. (2009).The National Formulary. Edisi 31. The
United States Pharmacopoeia Convention. Hal 1400-1401.
WHO. (1992). The Validation of Analytical Procedures Used in Examination of
Pharmaceitical Materials. Germany: WHO Technical Report Series. Hal.
288-298.
40
Universitas Sumatera Utara
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah metode deskriptif. Penelitian ini
dilaksanakan diLaboratorium Kimia Farmasi Kuantitatif Fakultas Farmasi
Universitas Sumatera Utara.
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah satu unit
Spektrofotometer UV-Vis (Shimadzu mini 1240), neraca analitik (AND GF- 200),
dan alat-alat gelas seperti labu takar, gelas ukur, beaker glass.
3.2 Bahan-bahan
Bahan yang digunakan dalam penelitian ini adalah Amlodipin Besilat
BPFI, akuades (E-Merck), Metanol (E-Merck). Sampel yang digunakan adalah
tablet generik Amlodipin (Hexparm), Normoten® (Soho), Tensivask® (Dexa
Medika), Lopiten® (Guardian Pharmatama).
3.3 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu tanpa
membandingkan antara satu sampel dengan sampel yang lain, karena sampel
dianggap homogen. Sampel yang digunakan adalah tablet amlodipin generik dan
nama dagang dengan jumlah zat aktif 10 ���������
3.4 Prosedur Penelitian
3.4.1 Pembuatan Larutan Induk BPFI
Sebanyak 50 mg amlodipin BPFI ditimbang seksama, dimasukkan ke
dalam labu tentukur 50 ml, ditambah dengan 5 ml metanol dikocok hingga larut
28
Universitas Sumatera Utara
dan dicukupkan dengan akuades sampai garis tanda, diperoleh larutan induk
dengan konsentrasi 1000 µg/ml, larutan ini disebut Larutan Induk Baku I (LIB I).
Dari larutan ini dipipet 10 ml dimasukkan ke dalam labu tentukur 50 ml,
diencerkan dengan akuades sampai garis tanda, lalu dikocok homogen sehingga
diperoleh larutan dengan konsentrasi 200 µg/ml (LIB II).
3.4.2 Penetapan Panjang Gelombang Serapan Maksimum
Dipipet sebanyak 4,5 ml Larutan induk Baku (LIB II) 200 µg/ml,
dimasukkan ke dalam labu tentukur 25 ml (36 µg/ml), kemudian dicukupkan
dengan akuades sampai garis tanda, serapan diukur pada panjang gelombang 200 -
400 nm.
3.4.3Penetapan dan Penentuan Linearitas Kurva Kalibrasi
Dipipet Larutan Induk Baku II (LIB II) BPFI (200 µg/ml) sebanyak 2 ml,3
ml,4 ml,5 ml,6 ml, masing-masing dimasukkan kedalam labu tentukur 25 ml,
ditambahkan akuades sampai garis tanda. Lalu dikocok homogen. Diperoleh
larutan dengan dengan konsentrasi 16µg/ml, 24 µg/ml,32µg/ml, 40 µg/ml, 48
µg/ml. Kemudian diukur serapannya pada panjang gelombang maksimum yang
diperoleh. Hasil dapat dilihat pada Tabel 2 (Halaman 22).
3.4.4 Uji Validasi Dengan Parameter Akurasi, Presisi, Batas Deteksi, Dan
batas kuantitasi
3.4.4.1 Uji Akurasi dengan persen perolehan kembali (% Recovery)
Uji akurasi dilakukan dengan metode penambahan baku (Standard
Addition Method) yaitu bahan baku yang ditambahkan pada sampel yaitu
9,00 µg/ml, uji recovery dilakukan 6 kali replikasi, kemudian dianalisi
dengan perlakuan yang sama seperti pada penetapan kadar sampel. pada
29
Universitas Sumatera Utara
penetapan kadar sampel. Persen perolehan kembali (% recovery) dapat
dihitung dengan rumus sebagai berikut:
A− B
% Recovery = x 100%
C
Keterangan:
A= Konsentrasi sampel yang diperoleh setelah penambahan bahan baku
B= Konsentrasi sampel sebelum penambahan bahan baku.
C= Konsentrasi bahan baku yang ditambahkan
3.4.4.2 Uji Presisi
Menurut Rohman (2007), Uji presisi (keseksamaan) merupakan ukuran
ketepatan relatif ditentukan dengan parameter RSD (Relative Standard Deviation)
dan umumnya dinyatakan dalam persen. RSD dirumuskan dengan persaman :
SD
RSD = x100%
X
Keterangan:
RSD = Relatif Standar Deviasi
SD = Standar Deviasi
X = Kadar rata-rata Amlodipin dalam sampel
Menurut Jones, (2002), untuk menghitung standar Deviasi (SD) digunakan
rumus :
SD =
∑ ( X − Xi) 2
Keterangan : n −1
SD = Standar deviasi tidak diketahui
X = kadar rata-rata sampel
X = kadar sampeln = jumlah perlakuan
30
Universitas Sumatera Utara
3.4.4.3 Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Untuk menentukan batas deteksi (LOD) dan batas kuantitasi (LOQ) dapat
digunakan rumus :
Sy (Y − Yi) 2
=
X n−2
10 × sy
LOQ = x
Slope
3 × sy
LOD = X
Slope
Keterangan:
��
� = Simpangan baku
LOD = Batas Deteksi
LOQ = Batas Kuantitasi
3.4.5 Penentuan Kadar Amlodipin Dalam Sediaan Tablet
Ditimbang 20 tablet dan diserbukkan dari 20 tablet. Ditimbang seksama
sejumlah serbuk setara dengan 20 mg amlodipin (Penimbangan serbuk sebanyak 6
kali pengulangan), dimasukkan ke dalam labu tentukur 50 ml. Kemudian
ditambah 5 ml metanol kemudian encerkan dengan akuades sampai garis tanda.
Kemudian disaring, 5 ml filtrat pertama dibuang. Dipipet filtrat dipipet sebanyak
4,5 ml larutan, dimasukkan kedalam labu tentukur 50 ml. Lalu dicukupkan dengan
akuades sampai garis tanda, kocok homogen dan diukur serapannya pada panjang
gelombang maksimum yang diperoleh. Penetapan kadar ditentukan dengan
menggunakan persamaan regresi yaitu: Y=aX + b.
31
Universitas Sumatera Utara
3.4.6 Analisis Data Secara Statistik
Kadar amlodipin besilat dapat dihitung dengan persamaan garis regresi
dan untuk menentukan apakah data diterima atau ditolak digunakan rumus seperti
di bawah ini:
X−X
t=
SD
n
Dasar penolakan data jika -thitung≤ dan bila thitung≤-ttabel.
Untuk mencari kadar sebenarnya dengan taraf kepercayaan 99%, dengan derajat
kebebasan dk = n -1, digunakan rumus:
μ= X ± t (1− 1 / 2α )dk x SD / n
Keterangan:
μ = interval kepercayaan
X = kadar rata-rata sampel
X = kadar sampel
t = harga t tabel sesuai dengan dk = n -1a
α = tingkat kepercayaan
dk = derajat kebebasan
SD = standar deviasi tidak diketahui
n = jumlah perlakuan
32
Universitas Sumatera Utara
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Panjang Gelombang Serapan Maksimum Amlodipin Besilat
BPFI.
Penetuan panjang gelombang ini dilakukan pada konsentrasi yang
memberikan serapan dengan kesalahan fotometrik terkecil yaitu ± 0,4343 . Untuk
mendapatkan konsentrasi tersebut dapat dihitung menggunakan nilai absorptivitas
spesifik Amlodipin besilat (A 11 = 119) dari literatur. Contoh perhitungan dapat
dilihat pada Lampiran 8.
Dari perhitungan didapatkan konsentrasi pengukuran adalah 36 µg/ml dan
dari hasil pengukuran diperoleh panjang gelombang maksimum, pada 364 nm.
seperti terlihat pada Gambar 1 dan Tabel 1.
Gambar 1. Kurva serapan Amlodipin Besilat Baku Pembanding Farmakope
Indonesia (Konsentrasi 36 µg/ml)
33
Universitas Sumatera Utara
Tabel 1. Data Absorbansi Dari Kurva Serapan Maksimum
Panjang Gelombang Absorbansi
maksimum
364.0 0.4368
239.0 1.1356
Panjang gelombang metode analisis menurut PPOM yaitu 364,0 nm.
Panjang gelombang yang diperoleh ini seterusnya digunakan untuk penentuan
kadar amlodipin besilat dalam tablet.
4.2 Pembuatan dan Penetuan Linieritas Kurva Kalibrasi
Linieritas merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan
antara respon (Y) dengan konsentrasi (X).Penentuan linieritas kurva kalibrasi Amlodipin
besilat BPFI dalam pelarut metanol dengan konsentrasi 16,0 µg/ml, 24,0 µg/ml,
32,0µg/ml, 40,0µg/ml, 48,0 µg/ml pada panjang gelombang 364 nm. Data dan kurva
kalibrasi dapat pada dilihat pada Tabel 2 dan Gambar 2 dibawah ini.
Tabel 2. Data Kurva kalibrasi dari Amlodipin Besilat BPFI
No. Conc. ABS
1. 0.0000 0.000
2. 16.000 0.187
3. 24.000 0.261
4. 32.000 0.347
5. 40.000 0.437
6. 48.000 0.517
34
Universitas Sumatera Utara
Gambar 2. Kurva Kalibrasi amlodipin besilat BPFI
Dari hasil pembuatan kurva kalibrasi amlodipin besilat BPFI diperoleh
hubungan yang linier antara konsentrasi dan serapan dengan koefisien korelasi (r)
= 0,9992 dan persamaan garis regresi Y = 0,010788x - 0,003764. Koefisien
korelasi yang diperoleh memenuhi kriteria penerimaan untuk korelasi adalah r ≥
0,995 (Moffat, 2004).
4.3 Uji Validasi Metode Spektrofotometri Ultraviolet
Pada penelitian ini dilakukan uji validasi dengan metode penambahan
bahan baku (Standard Addition Method) terhadap sampel tablet lopiten (PT.
Guardian Pratama) yang meliputi uji akurasi dengan parameter persen perolehan
kembali (% recovery), uji presisi dengan parameter RSD (Relative Standard
Deviation), batas deteksi (LOD) dan batas kuantitasi (LOQ) (WHO, 1992;
Indriyanto dan Yuwono, 2003). Uji akurasi dengan parameter persen perolehan
kembali dilakukan dengan membuat 6 kali replikasi, kemudian dianalisis dengan
perlakuan yang sama seperti pada tabel dibawah ini.
35
Universitas Sumatera Utara
Tabel 3. Data Hasil Pengujian Perolehan Kembali Lopiten dengan Metode
Penambahan Bahan Baku (Standard Addition Method).
Konsentrasi Bahan baku Persen
Berat Setelah Sebelum yang Perolehan
No Serapan
sampel/serbuk penambahan penambahan ditambahkan A− B
(A) x100%
mg bahan baku bahan baku (C) C
(A) (B) µg/ml
1 256,1 0,4792 44,11 34,87 9,00 102,6
2 254,9 0,4759 43,80 34,87 9,00 99,22
3 255,6 0,4765 43,86 34,87 9,00 99,88
4 256,2 0,4762 43,83 34,87 9,00 99,55
5 255,8 0,4701 43,26 34,87 9,00 93,22
6 256,4 0,4810 44,27 34,87 9,00 104,44
Kadar rata-rata (% recovery) 99,81
Standar Deviasi (SD) 3,8228
Relatif Standar Deviasi (%) 3,8300
Jumlah tablet 20 berat 20 tablet = 3539,2 mg
Tiap tablet lopiten 10 mg mengandung amlodipin besilat 13,87 mg setara dengan
amlodipin 10 mg
10mg
Berat serbuk setara 10 mg = x 3539,2 mg = 255,16 mg
13,87 mg
Dari data di atas didapatkan persen perolehan kembali (% recovery)
99,81% dengan standar deviasi (SD) sebesar 3,8228. Persen perolehan kembali ini
dapat diterima karena memenuhi syarat akurasi dimana rentang rata-rata hasil
perolehan kembali adalah 98-102%. Sedangkan dari hasil uji presisi dengan
parameter relatif standar deviasi (RSD) adalah 3,8300%. Nilai Relatif Standar
Deviasi (RSD) yang diperoleh dari pengukuran sediaan tablet yang dianalisis telah
≤5% untuk senyawa
memenuhi syarat RSD yaitu -senyawa dengan kadar
sekelumit (Rohman, 2007). Dapat disimpulkan bahwa metode yang digunakan
memenuhi persyaratan uji validasi metode sehingga dapat digunakan
36
Universitas Sumatera Utara
untukpenetapan kadar amlodipin dalam tablet. Batas deteksi (LOD) sebesar
1,5587 µg/ml dan batas kuantitasi (LOQ) sebesar 3,1957 µg/ml.
4.4 Penentuan Kadar Amlodipin Besilat dalam Sediaan Tablet
Hasil penentuan kadar amlodipin besilat dalam sediaan tablet dapat dilihat
pada Tabel4 dibawah ini. Data lengkap dapat dilihat pada Lampiran 2 halaman 30.
Tabel 4. Persentase Kadar Rata-rata dan Kadar Sebenarnya Amlodipin besilat
dalam sediaan tablet.
Kadar Rata-rata Kadar Sebenarnya
No Nama Sediaan
(%)s (%)
Amlodipin besilat generik
1 95,63 95,63 ± 1,14
(PT. Hexpharm Jaya)
Tensivask
2 94,74 94,74 ± 2,70
(Dexa Medika)
Normoten
3 94,94 94,94 ± 1,81
(Soho)
Lopiten
4 96,54 96,54 ± 0,90
(Guardian Pharmatama)
Dari data di atas menunjukkan, kadar amlodipin besilat dalam sediaan
tablet generik maupun nama dagang, memenuhi persyaratan kadar tablet pada
umumnya yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0 % dari jumlah
yang tertera pada etiket.
37
Universitas Sumatera Utara
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Metode Spektrofotometri Ultraviolet dapat digunakan untuk penetapan
kadar Amlodipin besilat dalam sediaan tablet karena pada hasil uji
validasi, metode ini menunjukkan akurasi dan presisi yang baik dengan
batas deteksi (LOD) 1,5587 µg/ml dan batas kuantitasi (LOQ) 5,1957
µg/ml.
2. Hasil penetapan kadar dari tablet generik dan nama dagang diperoleh,
untuk tablet Amlodipin Generik (PT. Hexpharm Jaya) sebesar 95,63 % ±
1,14%, tablet Tensivask® (Dexa Medica) 94,74% ± 2,70%, Normoten®
(Soho) 94,94% ± 1,81%, Lopiten® (Guardian Pharmatama) 96,54% ±
0,90%.
3. Dari hasil penelitian menunjukkan bahwa semua tablet yang diperiksa baik
yang generik maupun nama dagang memenuhi persyaratan kadar tablet
pada umumnya yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada etiket.
5.2 Saran
1. Disarankan kepada peneliti lainnya agar dapat menentukan kadar Amlodipin
besilat dengan metode lainnya seperti KCKT dan Kromatografi Gas.
2. Disarankan kepada peneliti lainnya agar dapat menentukan kadar obat turunan
arilasetat lainnnya yang beredar dipasaran secara Spektrofotometri Ultraviolet
38
Universitas Sumatera Utara
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sifat
2.1.1 Sifat Fisikokimia
Rumus Struktur
H
H3C N NH2
O
H3CO O CH3 O O
S
O O OH
Cl
Rumus molekul : C20H25ClN2O5, C6H6SO3
Nama Kimia : 3,5-pyridinedicarboxylic acid,
2-[(2Aminoethoxy)methyl]-4-(o –chlorophenyl)
1,4–dihydro–6–methyl–3–ethyl 5–methyl ester, monobenzensulfonate.
Berat Molekul : 567,05
Pemerian : Serbuk hablur, putih atau hampir putih, tidak atau hampirtidak
berbau.
Kelarutan : Mudah larut dalam etanol, dalam kloroform, dan
dalam eter, praktis tidak larut dalam air.
Penetapan kadar bahan baku : Dilakukan secara acidimetri
Penetapan kadar tablet : Dilakukan dengan metode kromatografi cair kinerja
tinggi, kromatografi gas dan spektrofotometri
ultra violet.
2.1.2 Farmakologi
17
Universitas Sumatera Utara
Hipertensi merupahkan penyakit heterogen yang dapat disebabkan oleh penyakit
spesifik (hipertensi sekunder) atau mekanisme patofisiologi yang tidak diketahui
penyebabnya (hipertensi primer atau ensensial). Pada umumnya kasus hipertensi
sekunder disebabkan oleh penyakit gagal ginjal kronik. Penyebab utama kematian
pada hipertensi adalahkardiovascular, dan gagal ginjal.Kemudian kematian
prematur ada korelasinya dengan meningkatkan tekanan darah (ISFI, 2008).
Berdasarkan struktur kimianya Amlodipin merupakan antagonis kalsium
golongan dihidropiridin (antagonis ion kalsium) yang menghambat influks
(masuknya) ion kalsium melalui membran kedalam otot polos vascular dan
otot.Amlodipin absorpsinya lambat, efeknya lebih lama, waktu paruh plasma 35
sampai 50 jam, serta efek dan kadar dalam plasma meningkat selama 7-10 hari
terapi. Amlodipin menghasilkan vasodilatasi arteri perifer dan dilatasi koroner
yang profil hemodinamiknya.Namum amlodipin menyebabkan takikardia reflex
mungkin karena waktu paruhnya yang lama menyebabkan puncak minimumdalam
konsentrasi plasma (Goodman dan Gilman, 2008).
Efek antihipertensi amlodipin adalah dengan bekerja langsung sebagai
vasodilator arteriperifer yang dapat menyebabkan penurunan resisten vaskular
serta penurunan tekanan darah.Dosis satu kali sehari akan menghasilkan
penurunan tekanan darah yang berlangsung selama 24 jam. Onset kerja amlodipin
adalah perlahan-lahan, sehingga tidak menyebabkan terjadinya hipotensi
akut.Efek antiangina amlodipin adalah melalui dilatasi arteriol perifer sehingga
dapat menurunkan resistensi perifer total (afterload).Karena amlodipin tidak
mempengaruhi frekuensi denyut jantung, pengurangan beban jantung akan
menyebabkan penurunan kebutuhan oksigen miokardial serta kebutuhan energi.
18
Universitas Sumatera Utara
Amlodipin menyebabkan dilatasi arteri baik pada keadaan oksigenisasi normal
maupun keadaan iskemia. Pada pasien angina, dosis amlodipin satu kali sehari
dapat meningkatkan waktu latihan, waktu timbulnya angina, waktutimbulnya
depresi segmen ST dan menurunkan frekuensi seranganangina serta penggunaan
tablet nitrogliserin. Amlodipin tidak menimbulkan perubahan kadar lemak plasma
dan dapat digunakan pada pasien asma, diabetes serta gout (Anonim, 2010).
Amlodipin (derivate dihidropiridin) efektif dalam menurunkan tekanan
darah. Perbedaan hemidinamik diantara penghambatan kanal kalsium bisa
mempengaruhi obat tertentu. Aktivitas reflex simpatis dengan takikardia ringan
akan mempertahankan atau meningkatkan curah jantung (Katzung, 1994).
2.1.3 Efek Samping
Efek samping umum yang dapat ditimbulkan oleh amlodipin diantaranya
pusing, nyeri kepala, rasa panas di muka dan terutama pada derivat-piridin dan
udema pergelangan kaki (akibat vasodilatasi perifer). Umumnya, efek ini bersifat
sementara (Tan dan Raharja, 2002).
2.1.4 Dosis
Hipertensi dan angina variant/stabil 1 dd 5 mg (besilat=benzosulfonat),
maksimum 10 mg (Tan dan Raharja, 2002).
2.2 Spektrofotometri Ultraviolet
19
Universitas Sumatera Utara
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara
radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia. Teknik yang
sering digunakan dalam analisis farmasi meliputi spektrofotometri ultraviolet,
cahaya tampak, infra merah dan serapan atom.Jangkauan panjang
gelombanguntuk daerah ultraviolet adalah 190-380 nm(Ditjen POM, 1995).
Gugus fungsi yang menyerap radiasi di daerah ultraviolet dekat dan daerah
tampak disebut kromofor dan hampir semua kromofor mempunyai ikatan tak
jenuh. Pada kromofor jenis initransisi terjadi dari π→ π*, yang menyerap pada λ
max kecil dari 200nm (tidak terkonyugasi), misalnya pada >C=< dan –C ≡ C -
.Kromofor ini merupakan tipe transisi dari sistem yang mengandung elektron
πpada orbital molekulnya.Untuk senyawa yang mempunyai system konyugasi,
perbedaan energi antara keadaan dasar dan keadaan tereksitasi menjadi lebih kecil
sehingga penyerapan terjadi pada panjang gelombang yang lebih besar
(Dachriyanus, 2004).
Gugus fungsi seperti –OH, -NH2, dan –Cl yang memberikan transisi n→
π* disebut gugus auksokrom. Gugus ini adalah gugus yang tidak dapat menyerap
radiasi ultraviolet-sinar tampak, tetapi apabila gugus ini terikat pada gugus
kromofor mengakibatkan pergeseran panjang gelombang ke arah yang lebih besar
(efekbatokromik).
Hal-hal yang harus diperhatikan dalam analisis spektrofotometri
ultraviolet:
a. Pemilihan panjang gelombang maksimum
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang
gelombang dimana terjadi serapan maksimum. Untuk memperolehpanjang
gelombang maksimum, dilakukan dengan membuat kurva hubungan antara
20
Universitas Sumatera Utara
absorbansi dengan panjang gelombang dari suatu larutan baku pada
konsentrasi tertentu.Ada beberapa alasan mengapa harus menggunakan
panjang gelombang maksimum, yaitu:
• Pada panjang gelombang maksimum, kepekaannya juga maksimum karena
pada panjang gelombang maksimum tersebut, perubahan absorbansi untuk
setiap satuan konsentrasi adalah yang paling besar.
• Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar
dan pada kondisi tersebut hukum Lambert-Beer akan terpenuhi.
• Jika dilakukan pengukuran ulang maka kesalahan yang terjadi pada
pengulangan akan kecil sekali, karena digunakan panjang gelombang
maksimum.
b. Pembuatan kurva kalibrasi
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai
konsentrasi. Masing-masing absorbansi larutan dengan berbagai konsentrasi
diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi
dengan konsentrasi. Bila hukum Lamber-Beer terpenuhi maka kurva kalibrasi
merupakan garis lurus.
c. Pembacaan absorbansi sampel atau cuplikan
Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2-0,6.
Anjuran ini berdasarkan anggapan bahwa pada kisaran nilai absorbansi tersebut,
kesalahan fotometrik yang terjadi adalah paling minimal (Gandjar dan Rohman,
2007)
2.2.1 Hukum Lambert-Beer
21
Universitas Sumatera Utara
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel
yang disinari. Menurut Hukum Beer, yang hanya berlaku untuk cahaya
monokromatik dan larutan yang sangat encer, serapan berbanding lurus dengan
konsentrasi (banyak molekul zat). Kedua pernyataan ini dapat dijadikan satu
dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus
terhadap konsentrasi dan ketebalan sel, yang dapat ditulis dengan persamaan :
A= a.b.c g/liter atau A= ε. b. c mol/liter
Dimana: A = serapan
a = absorptivitas
b = ketebalan sel
c = konsentrasi
ε = absorptivitas molar
Jadi dengan Hukum Lambert-Beer konsentrasi dapat dihitung dari
ketebalan sel dan serapan. Absorptivitas merupakan suatu tetapan dan spesifik
untuk setiap molekul pada panjang gelombang dan pelarut tertentu.
Menurut Roth dan Blaschke (1981), absorptivitas spesifik juga sering
digunakan sebagai ganti absorptivitas. Harga ini, memberikan serapan larutan 1 %
(b/v) dengan ketebalan sel 1 cm, sehingga dapat diperoleh persamaan:
A = A 11 . b. c
Dimana : A 11 = absorptivitas spesifik (ml g -1cm-1)
b = ketebalan sel (cm)
c = konsentrasi senyawa terlarut (g/100ml larutan)
2.2.2 Penggunan Spektrofotometri Ultraviolet
22
Universitas Sumatera Utara
Spektrofotometri ultraviolet digunakan dalam analisis senyawa organik
yaitu:
1. Analisis kualitatif
Secara eksperimental, sangat mudah untuk mengukur banyaknya radiasi
yang diserap oleh suatu molekul sebagai fungsi frekuensi radiasi. Suatu grafik
yang menghubungkan antara banyaknya sinar yang diserap dengan frekuensi
(panjang gelombang) sinar merupakan spektrum absorpsi. Transisi yang terjadi
untuk suatu molekul dengan struktur kimia yang berbeda tidaklah sama sehingga
spektrum absorpsinya juga berbeda. Dengan demikian, spektrum dapat digunakan
sebagai bahan informasi yang bermanfaat untuk analisis kualitatif (Rohman dan
Gandjar, 2007).
2. Analisis kuantitatif
Penggunaan utama spektrofotometri ultraviolet adalah dalam analisis
kuantitatif. Apabila dalam alur spektrofotometer terdapat senyawa yang
mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai
detektor. Parameter kekuatan energi radiasi khas yang diabsorpsi oleh molekul
adalah absorban (A) yang dalam batas konsentrasi tertentu nilainya sebanding
dengan banyaknya molekul yang mengabsorpsi radiasi dan merupakan
dasaranalisis kuantitatif. Konsentrasi larutan analit umumnya 10 sampai 20
µg/ml, tetapi untuk senyawa yang nilai absorptivitasnya besar dapat diukur pada
konsentrasi yang lebih rendah. Senyawa yang tidak mengabsorpsi radiasi
ultraviolet-sinar tampak dapat juga ditentukan dengan spektrofotometri
ultraviolet-sinar tampak, apabila ada reaksi kimia yang dapat mengubahnya
23
Universitas Sumatera Utara
menjadi kromofor atau dapat disambungkan dengan suatu pereaksi kromofor
(Satiadarma, 2004).
Analisis kuantitatif secara spektrofotometri ultraviolet dapat dilakukan
dengan metode regresi dan pendekatan
1. Metode Regresi
Analsis kuantitatif dengan metode regresi yaitu dengan menggunakan
persamaan regresi yang didasarkan pada harga serapan dan konsentrasi standar
yang dibuat dalam beberapa konsentrasi, paling sedikit menggunakan 5 rentang
konsentrasi yang meningkat yang dapat memberikan serapan yang
linier,kemudian diplot menghasilkan suatu kurva yang disebut dengan kurva
kalibrasi. Konsentrasi suatu sampel dapat dihitung berdasarkan kurva tersebut.
2. Metode Penekatan
Analisis kuantitatif dengan cara ini dilakukan dengan membandingkan
serapan standar yang konsentrasinya diketahui dengan serapan sampel.
Konsentrasi sampel dapat dihitung melalui rumus perbandingan
AsxCb
C=
Ab
dimana As = serapan sampel, Ab = serapan standar, Cb = konsentrasi
standar, dan C = konsentrasi sampel (Holme dan Peck, 1983).
2.2.3 Peralatan Spektrofotometri Ultraviolet
Spektrofotometer adalah alat untuk mengukur transmitans atau serapan
suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan
penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang
menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan
24
Universitas Sumatera Utara
fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang
diabsorpsi (Day dan Underwood, 1999).
Unsur-unsur terpenting suatu spektrofotometer adalah sebagai
berikut(Khopkar, 1990):
1. Sumber-sumber lampu; lampu deuterium digunakan untuk daerah UV pada
panjang gelombang dari 190-350 nm, sementara lampu halogen kuarsa atau
lampu tungsten digunakan untuk daerah visibel pada panjang gelombang
antara 350- 900 nm.
2. Monokromotor: digunakan untuk memperoleh sumber sinar yang
monokromatis. Alatnya dapat berupa prisma maupun grating. Untuk
mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian.
3. Kuvet: Pada pengukuran di daerah tampak, kuvet kaca atau kuvet kaca corex
dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus
menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini.
Umumnya tebal kuvet adalah 10 mm, tetapi yang lebih kecil ataupun yang
lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi,
tetapi bentuk silinder dapat juga digunakan. Kuvet yang tertutup digunakan
untuk pelarut organik. Sel yang baik adalah kuarsa atau gelas hasil leburan
yang homogen.
4. Detektor: Peranan detector penerima adalah memberikan respon terhadap
cahaya pada berbagai panjang gelombang.
5. Suatu amplifier (penguat) dan rangkaian yang berkaitan yang membuat isyarat
listrik dapat diamati.
6. Sistem pembacaan yang memperlihatkan besarnya listrik.
25
Universitas Sumatera Utara
2.3 Validasi
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada
prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut
memenuhi persyaratan untuk penggunaannya (Harmita, 2004).Parameter analisis
yang ditentukan pada validasi adalah akurasi, presisi, kespesifikan, limit deteksi,
limit kuantitasi, kelinieran dan rentang.
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan
melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode
penambahan bahan baku (standard addition method). Dalam metode simulasi,
sejumlah analit bahan murni (senyawa pembanding kimia) ditambahkan kedalam
campuran bahan sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar standar yang ditambahkan (kadar
sebenarnya). Dalam metode adisi (penambahan bahan baku), sampel dianalisis
lalu sejumlah tertentu analit yang diperiksa ditambahkan kedalam sampel,
dicampur dan dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar
yang sebenarnya (hasil yang diharapkan). Dalam kedua metode tersebut, persen
perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan
hasil yang sebenarnya.
A− B
% PerolehanKembali = x100%
C
Keterangan : A = Konsentrasi sampel yang diperoleh setelah penambahanbaku
B = Konsentrasi sampel sebelum penambahan baku
C = Konsentrasi baku yang ditambahkan
26
Universitas Sumatera Utara
Presisi (keseksamaan) adalah derajat kesesuain diantara masing-masing
hasil uji, jika prosedur analisis diterapkan berulang kali pada sejumlah cuplikan
yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai deviasi
standar atau deviasi standar relative (koefisien variasi). Presisi dapat diartikan
pula sebagai derajat reprodusibilitas (ketertiruan) atau repeatabilitas
(keterulangan).
Batas deteksi adalah nilai parameter, yaitu konsentrasi analit terendah
yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan
dengan blanko. Batas deteksi dapat dihitung dengan rumus sebagai berikut:
3 xSB
Batas deteksi =
Slope
Batas kuantitasi adalah jumlah analit terkecil dalam sampel yang masih
dapat diukur dalam kondisi percobaan yang sama dan memenuhi kriteria cermat
dan seksama.
10 xSB
Batas Kuantitasi =
Slope
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan
bahwa nilai hasil uji langsung atau setelah diolah secara secara matematika,
proporsional dengan konsentrasi analit dalam sampel dalam batas rentang
konsentrasi tertentu.
Rentang suatu metode analisis adalah interval antara batas konsentrasi
tertinggi dan konsentrasi terendah analit yang dapat ditentukan dengan presisi,
akurasi dan kelinieran (Satiadarma, 2004; WHO, 1992)
27
Universitas Sumatera Utara
BAB I
PENDAHULUAN
1.1 Latar Belakang
Darah tinggi (Hipertensi) kini menjadi masalah global karena prevalensi
yang terus meningkat sejalan dengan perubahan gaya hidup seperti merokok,
obesitas, inaktivitas fisik, dan stress.Hampir di setiap Negara hipertensi
menduduki peringkat pertama sebagai penyakit paling sering dijumpai (Anonim,
2010).
Amlodipin tablet diindikasikan untuk pengobatan hipertensi, dapat
digunakan untuk mengontrol tekanan darah pada sebagian besar penderita
hipertensi.Penderita hipertensi yang tidak cukup terkontrol jika hanya
menggunakan anti hipertensi tunggal akan sangat menguntungkan dengan
pemberian amlodipin yang dikombinasikan dengan diuretik thiazida, inhibitor β-
adrenoreseptor, atau inhibitor angiotensin converting enzyme.Amlodipin juga
diindikasikan untuk pengobatan iskemia myokardial, baik karena obstruksi fixed
(angina stabil), maupun karena vasokonstriksi (angina varian) dari pembuluh
darah koroner. Dalam perdagangan amlodipin tablet terdapat dalam bentuk
generik dan nama dagang (Anonim, 2001).
Monorgafi amlodipin dalam sedian tablet tidak terdapat dalam FI edisi IV
sedangkan monografi amlodipin dalam bahan baku terdapat dalam United State
Pharmacopoeia XXXI, 2009 (USP) dengan penetapan kadar secara KCKT.
Menurut metode analisis BPOM no 01/08/02 amlodipin tablet dapatditentukan
14
Universitas Sumatera Utara
secara spektrofotometri ultraviolet dalam pelarut metanol air dimana serapan
maksimum pada panjang gelombang ± 365 nm.
Menurut Moffat, (2004) amlodipin besilat memiliki serapan maksimum
panjang gelombang 236nm dalam basa dan dalam larutan asam NH2SO4 239 nm.
Dalam sertifikat pengujian Badan POM RI, amlodipin besilat memiliki panjang
1
gelombang 360nm ( A1 = 119) dalam pelarut metanol.
Berdasarkan hal tersebut diatas peneliti mencoba menggunakan metode
spektrofotometri ultraviolet pada penentuan kadar amlodipin dalam tablet metode
ini relatif lebih murah dan sederhana dibandingkan dengan metode KCKT.
Untuk menguji validitas dari metode ini dilakukan pengujian antara lain
uji akurasi dengan parameter % recovery, uji presisi dengan parameter Standar
Deviasi Relatif (RSD), uji sensitifitas dengan parameter limit deteksi (LOD) dan
limit kuantitasi (LOQ) (WHO, 1989).
1.2 Perumusan Masalah
a. Apakah amlodipin dalam sediaan tablet dapat ditentukan kadarnya secara
spektofotometri ultraviolet dan memenuhi persyaratan uji validasi?
b. Apakah kadar amlodipin besilat dalam tablet generik dan nama dagang
memenuhi persyaratan kadar umumnya suatu tablet.
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah:
a. Amlodipin besilat dalam sediaan tablet dapat ditentukan kadarnya secara
spektrofotometri ultraviolet dan memenuhi uji validasi metode.
b. Kadar amlodipin besilat dalam sedian tablet generik dan nama dagang
memenuhi persyaratan kadar umumnya suatu tablet.
15
Universitas Sumatera Utara
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Untuk Menentukan tingkat validasi metode spektrofotometri
ultravioletpada penetapan kadar amlodipin besilat dalam sediaan tablet.
b. Untuk Mengetahui kesesuaian kadar tablet generik dan nama dagang
dengan persyaratan kadar umumya suatu tablet.
1.5 Manfaat Penelitian
Sebagai metode sederhana dalam Industri Farmasi pada penetapan kadar
amlodipin besilat dalam tablet.
16
Universitas Sumatera Utara
Penerapan Metode Spektrofotometri Ultraviolet
Pada Penetapan Kadar Amlodipin Besilat dalam Sediaan Tablet
Abstrak
Amlodipintermasukantagoniskalsiumgolongandihidropiridin yang berkerja
menghambatmasuknya ion kalsiummelaluimembrankedalamotot polos vaskular
danototjantung. Tujuan penelitian ini adalah untuk mendapatkan metode alternatif
pada penetapan kadar tablet amlodipin yang relatif lebih murah dan mudah dalam
pelaksanaannya, namun memberikan hasil dengan akurasi dan presisi yang baik
dan sekaligus menentukan kadar tablet amlodipin generik dan nama dagang yang
beredar di pasaran.
Metode yang digunakanpadapenelitianiniyaitusecaraspektrofotometri
ultraviolet dalam pelarut metanol pada panjang gelombang 364 nm. Metode ini
memenuhi persyaratan uji validasi dengan persen perolehan kembali 100,51%
danrelatifstandardeviasi (RSD) 3,7975%, batasdeteksi (LOD) 1,5587 µg/ml
danbataskuantitasi (LOQ) 5,1957 µg/ml.
Dari hasilpenelitiandiperolehkadartablet amlodipin generik (Hexpharm)
sebesar 95,63% ± 1,145% dan tablet namadagang Tensivask® (DexaMedika)
sebesar 94,74% ± 2,70%, Normoten® (Soho) sebesar 94,94% ± 1,81%, Lopiten®
(Guardian Pharmatama) sebesar 96,54% ± 0,90%.
Hasilpenelitianmenunjukkankadaramlodipindalamsediaan tablet
generikdannama dagangmemenuhipersyaratan tablet
padaumumnyayaitutidakkurang dari 90,0% dantidaklebih dari 110,0% darijumlah
yang terterapadaetiket.
Kata kunci : Amlodipin, penetapan kadar, spektrofotometri ultraviolet, validasi
metode
Universitas Sumatera Utara
Application of Ultraviolet Spectrophotometry Method on Determination of
Amlodipine Besilat in Tablet Preparations
Abstract
Amolodipine is one of antagonis calcium the group of dihidropiridin
which inhibit the entry of calcium ions through the membrane into the vascular
smooth muscle and cardiac muscle. The purpose of this study to find an
alternative method to determination of amlodipine tablets which are relatively
cheap and easy in implementation, but it gives results with good accuracy and
precision and olso to determine the levels of amlodipine tablet generic and trade
names on the market.
The name as the method which is used to the study is ultraviolet of
spectrophotometry with solvent of methanol at a wavelength of 364 nm. This
method meets the requirements validation test with the recovery percent is
100,51% and deviation standard of relative (RSD) is 3,7975%, detection of limit
(LOD) is, 1.5587 g/ml and quantitation of limit (LOQ) is, 5.1957 g/ml.
From the study were obtained the generic rate of amlodipine tablets
(Hespharm) equal to 95.63% ± 1.145% and the trade names Tensivask® tablets
(Dexa Medika) equal to 94.74% ± 2.70%, Normoten® (Soho) equal to 94.94% ±
1.81%, Lopiten® (Guardian Pharmatama) amounted to 96.54% ± 0.90%.
The study showed that levels of amlodipine in tablet dosage generic and
trade name meets the requirements of tablets in the general are not less than
90.0% and not more than 110.0% of the listed amount on the label.
Key words:amlodipine, determination, spectrophotometry ulraviolet, validation
methods.
Universitas Sumatera Utara
PENERAPAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET PADA PENETAPAN KADAR
AMLODIPIN BESILAT DALAM SEDIAAN TABLET
SKRIPSI
OLEH:
SURYANI NURJAMAL
NIM 071524074
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
Universitas Sumatera Utara
PENERAPAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET PADA PENETAPAN KADAR
AMLODIPIN BESILAT DALAM SEDIAN TABLET
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SURYANI NURJAMAL
NIM 071524074
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
Universitas Sumatera Utara
PENGESAHAN SKRIPSI
PENERAPAN METODE SPEKTROFOTOMETRI
ULTRAVIOLET PADA PENETAPAN KADAR
AMLODIPIN BESILAT DALAM SEDIAN TABLET
OLEH:
SURYANI NURJAML
NIM 071524074
Dipertahankan di Hadapan Panitia Penguji Skripsi
Fakultas Farmasi
Universitas Sumatera Utara
Pada tanggal :8Agustus 2013
Pembimbing Panitia Penguji,
Drs. Fathur Rahman Harun, M.Si., Apt. Prof. Dr. rer. nat E. De Lux Putra, S.U., Apt.
NIP 19521041980031002 NIP 19530619183031001
Drs. Fathur Rahman Harun, M.Si., Apt.
Pembimbing II, NIP 195201041980031002
Drs. Syafruddin, MS., Apt. Drs. Nahitma Ginting, M.Si., Apt.
NIP 194811111976031003 NIP 195409101983032001
Dra. Nurmadjuzita, M.Si., Apt.
NIP 194809041974122001
Medan, Agustus 2015
Fakultas Farmasi
Universitas Sumatera Utara
Dekan,
Prof. Dr. Sumadio Hadisahputra, Apt.
NIP 195311281983031002
Universitas Sumatera Utara
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan nikmat,
rahmat, karunia dan ridhoNya, sehingga penulis dapat menyelesaikan skripsi yang
berjudul "Penerapan Metode Spektrofotometri Ultraviolet Pada Penetapan
Amlodipin Besilat Dalam Sediaan Tablet". Skripsi ini diajukan sebagai salah satu
syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara.
Pada kesempatan ini penulis hendak menyampaikan rasa hormat dan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara,
Bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan Bapak Drs. Syafruddin, M.S.,
Apt., yang telah banyak memberikan bimbingan dan bantuan selama penelitian
dan penulisan skripsi ini berlangsung, juga kepada Bapak Prof. Dr. rer. nat.
Effendy De Lux Putra, S.U., Apt., Ibu Dra. Nurmadjuzita, M.Si., Apt., Bapak Drs.
Nahitma Ginting, M.Si., Apt., selaku dosen penguji yang telah memberikan
masukan dalam penyusunan skripsi ini.
Penulis juga tidak lupa mengucapkan terima kasih dan penghargaan yang
tulus kepada kedua orang tua, Ayahanda Djamalluddin dan Ibunda Nurasiah Sirait
tercinta, adik-adikku tersayang Fajar dan Wale atas doa, dorongan dan
pengorbanan baik moril maupun materil dalam penyelesaian skripsi ini. Juga
kepada sahabat-sahabatku tersayang David Monandar, Astri, Andre, Agnes,
Nasril, Desi, Faula, Ratna, Suci, Iyum dkk yang selalu ada memberi semangat dan
pikiran selama penelitian dan penyusunan skripsi ini. Tidak lupa penulis ingin
Universitas Sumatera Utara
mengucapkan terima kasih kepada teman-teman stambuk 2007 yang tidak dapat
disebutkan namanya satu persatu, atas segala dorongan, motivasi dan bantuannya
kepada penulis sehingga skripsi ini dapat selesai.
Pada kesempatan ini penulis hendak menyampaikan rasa hormat dan
terima kasih.
Medan, Agustus2015
Penulis,
Suryani Nurjamal
NIM 071524074
Universitas Sumatera Utara
Penerapan Metode Spektrofotometri Ultraviolet
Pada Penetapan Kadar Amlodipin Besilat dalam Sediaan Tablet
Abstrak
Amlodipintermasukantagoniskalsiumgolongandihidropiridin yang berkerja
menghambatmasuknya ion kalsiummelaluimembrankedalamotot polos vaskular
danototjantung. Tujuan penelitian ini adalah untuk mendapatkan metode alternatif
pada penetapan kadar tablet amlodipin yang relatif lebih murah dan mudah dalam
pelaksanaannya, namun memberikan hasil dengan akurasi dan presisi yang baik
dan sekaligus menentukan kadar tablet amlodipin generik dan nama dagang yang
beredar di pasaran.
Metode yang digunakanpadapenelitianiniyaitusecaraspektrofotometri
ultraviolet dalam pelarut metanol pada panjang gelombang 364 nm. Metode ini
memenuhi persyaratan uji validasi dengan persen perolehan kembali 100,51%
danrelatifstandardeviasi (RSD) 3,7975%, batasdeteksi (LOD) 1,5587 µg/ml
danbataskuantitasi (LOQ) 5,1957 µg/ml.
Dari hasilpenelitiandiperolehkadartablet amlodipin generik (Hexpharm)
sebesar 95,63% ± 1,145% dan tablet namadagang Tensivask® (DexaMedika)
sebesar 94,74% ± 2,70%, Normoten® (Soho) sebesar 94,94% ± 1,81%, Lopiten®
(Guardian Pharmatama) sebesar 96,54% ± 0,90%.
Hasilpenelitianmenunjukkankadaramlodipindalamsediaan tablet
generikdannama dagangmemenuhipersyaratan tablet
padaumumnyayaitutidakkurang dari 90,0% dantidaklebih dari 110,0% darijumlah
yang terterapadaetiket.
Kata kunci : Amlodipin, penetapan kadar, spektrofotometri ultraviolet, validasi
metode
Universitas Sumatera Utara
Application of Ultraviolet Spectrophotometry Method on Determination of
Amlodipine Besilat in Tablet Preparations
Abstract
Amolodipine is one of antagonis calcium the group of dihidropiridin
which inhibit the entry of calcium ions through the membrane into the vascular
smooth muscle and cardiac muscle. The purpose of this study to find an
alternative method to determination of amlodipine tablets which are relatively
cheap and easy in implementation, but it gives results with good accuracy and
precision and olso to determine the levels of amlodipine tablet generic and trade
names on the market.
The name as the method which is used to the study is ultraviolet of
spectrophotometry with solvent of methanol at a wavelength of 364 nm. This
method meets the requirements validation test with the recovery percent is
100,51% and deviation standard of relative (RSD) is 3,7975%, detection of limit
(LOD) is, 1.5587 g/ml and quantitation of limit (LOQ) is, 5.1957 g/ml.
From the study were obtained the generic rate of amlodipine tablets
(Hespharm) equal to 95.63% ± 1.145% and the trade names Tensivask® tablets
(Dexa Medika) equal to 94.74% ± 2.70%, Normoten® (Soho) equal to 94.94% ±
1.81%, Lopiten® (Guardian Pharmatama) amounted to 96.54% ± 0.90%.
The study showed that levels of amlodipine in tablet dosage generic and
trade name meets the requirements of tablets in the general are not less than
90.0% and not more than 110.0% of the listed amount on the label.
Key words:amlodipine, determination, spectrophotometry ulraviolet, validation
methods.
Universitas Sumatera Utara
DAFTAR ISI
Halaman
JUDUL ...................................................................................................... i
PENGESAHAN SKRIPSI ........................................................................ iii
KATA PENGANTAR .............................................................................. iv
ABSTRAK ................................................................................................ vi
ABSTRACT .............................................................................................. vii
DAFTAR ISI ............................................................................................. viii
DAFTAR TABEL ..................................................................................... xii
DAFTAR GAMBAR ................................................................................ xiii
DAFTAR LAMPIRAN .............................................................................. xiv
BAB I PENDAHULUAN
1.1 Latar Belakang ........................................................................ 1
1.2 Perumusan Masalah ............................................................... 2
1.3 Hipotesis ................................................................................ 2
1.4 Tujuan Penelitian ................................................................... 3
BAB IITINJAUAN PUSTAKA
2.1 Uraian Sifat ............................................................................ 4
2.1.1 Sifat Fisika Kimia ...................................................... 4
2.1.2 Farmakologi ............................................................... 5
2.1.3 Efek Samping ............................................................ 6
2.1.4 Dosis .......................................................................... 6
2.2 Spektrofotometri Ultraviolet .................................................. 7
2.2.1 Hukum Lambert Beer ................................................ 9
Universitas Sumatera Utara
2.2.2 Penggunanan Spektrofotometri Ultraviolet .............. 10
2.2.3 Peralatan Untuk Spektrofotometri Ultraviolet ........... 12
2.3 Validasi .................................................................................. 13
BAB III METODE PENELITIAN
3.1 Alat–Alat ............................................................................... 16
3.2 Bahan-Bahan ......................................................................... 16
3.3 Pengambilan Sampel ............................................................. 16
3.4 Prosedur Penelitian ................................................................ 17
3.4.1 Pembuatan Larutan Induk Amlodipin Besilat BPFI .. 17
3.4.2 Penetapan Panjang Gelombang Serapan Maksimum 17
3.4.4 Uji Validasi Dengan Parameter Akurasi, Presisi,
Batas Deteksi dan Batas Kuantitasi ......................... 18
3.4.4.1 Uji Akurasi dengan Persen Perolehan
Kembali (%Recovery).................................. 18
3.4.4.2 Uji Presisi ................................................... .......... 18
3.4.4.3 Penentuaan Batas Deteksi (LOD)dan Batas
Kuantitasi (LOQ) ........................................ 19
3.4.5 Penetuan Kadar Amlodipin Besilat dalam Sedian
Tablet .......................................................................... 19
3.4.5 Analisis Data Secara Stastistik ................................. 20
BAB IV HASIL DAN PEMBAHASAN
4.1 Penentuan Panjang Gelombang Serapan Maksimum
Amlodipin Besilat BPFI ..................................................... 21
4.2 Pembuatan Kurva Kalibrasi ................................................ 22
4.3 Uji Validasi Metode Spektrofotometri Ultraviolet ............. 23
4.4 Penentuaan Kadar Amlodipin Besilat dalam Sediaan
Tablet .................................................................................. 25
Universitas Sumatera Utara
BAB V KESIMPULAN DAN SARAN ................................................... 26
5.1 Kesimpulan ............................................................................. 26
5.2 Saran ........................................................................................ 26
DAFTAR PUSTAKA
LAMPIRAN
10
Universitas Sumatera Utara
DAFTAR TABEL
Halaman
Tabel 1.Data Absorbansi dari Kurva Serapan Maksimum ....................... 22
Tabel 2. Data Kurva Kalibrasi dari Amlodipin Besilat BPFI ................... 22
Tabel 3. Data Hasil Pengujian Perolehan Kembali Dari Tablet
Amlodipin Besilat Dengan Metode Penambahan Baku .......... 24
Tabel 4. Persentase Kadar rata-rata dan Kadar Sebenarnya Amlodipin
Besilat Sediaan Tablet .............................................................. 25
11
Universitas Sumatera Utara
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Serapan Amlodipin Besilat BPFI .............................. 21
Gambar 2. Kurva Kalibrasi Amlodipin Besilat BPFI ............................ 23
12
Universitas Sumatera Utara
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Persamaan Regresi Amlodipin Besilat ...... 30
Lampiran 2. Data Kadar Amlodipin Besilat Dalam Sediaan Tablet .. 31
Lampiran 3. Perhitungan Statistik Kadar Amlodipin Besilat Pada
Tablet Generik (Hexpharm Jaya) ................................... 32
Lampiran 4. Perhitungan Stasistik Kadar Amlodipin Besilat Pada
Tablet Tensivask® (Dexa Medika) ................................ 35
Lampiran 5. Perhitungan Stasistik Kadar Amlodipin Besilat Pada
Tablet Normoten® (Soho) .............................................. 37
Lampiran 6. Perhitungan Stasistik Kadar Amlodipin Besilat Pada
Tablet Lopiten® (Guardian Pharmatama) ...................... 40
Lampiran 7. Perhitungan Konsentrasi Pengukuran Sampel ............... 43
Lampiran 8. Perhitungan Penimbangan Sampel dari tablet Lopiten®
(Guardian Pharmatama) ................................................. 44
Lampiran 9. Contoh Perhitungan Batas Deteksi (LOD) dan batas
Kuantitasi (LOQ) ........................................................... 45
Lampiran 10. Nilai Distribusi t ............................................................. 46
Lampiran 11. Sertifikat Bahan Baku POM ........................................... 47
Lampiran 12. Sertikitat Bahan Baku Amlodipin Besilat dari
PT.Indofarma ................................................................ 48
Lampiran 13. Gambar Perangkat Penelitian ......................................... 49
13
Universitas Sumatera Utara
You might also like
- Perhitungan 100 BenihDocument10 pagesPerhitungan 100 BenihNail AbyathNo ratings yet
- Roi Andarasi Manullang - 2102031 - Uji T Dan KorelasiDocument7 pagesRoi Andarasi Manullang - 2102031 - Uji T Dan Korelasiruben528No ratings yet
- 3.5 Curah Hujan RencanaDocument14 pages3.5 Curah Hujan RencanaDimas Manggala Putra AnnasNo ratings yet
- Modul Cuti Sekolah MatematikDocument17 pagesModul Cuti Sekolah MatematikZairi JeryNo ratings yet
- Jurnal Fisdas GMBDocument7 pagesJurnal Fisdas GMBAsri ElcrushNo ratings yet
- Contoh Soal Dan Pembahasan Estimasi Parameter Interval Konfidensi Dan Uji HipotesisDocument9 pagesContoh Soal Dan Pembahasan Estimasi Parameter Interval Konfidensi Dan Uji HipotesisHanz PetersburgNo ratings yet
- Laporan Akhir Kimklin SGPTDocument5 pagesLaporan Akhir Kimklin SGPTNovi RianiNo ratings yet
- TR 2 Proglin - Adinda Sahira - 4181111013 - PSPM C 2018Document10 pagesTR 2 Proglin - Adinda Sahira - 4181111013 - PSPM C 2018Yusni Utami TariganNo ratings yet
- BAB 4 FiltrasiDocument9 pagesBAB 4 FiltrasiZahrana BintangNo ratings yet
- IntravenaDocument5 pagesIntravenaFAIRUZ 1No ratings yet
- Calculator Add MathDocument4 pagesCalculator Add MathMuhd ZakuanNo ratings yet
- Topic 4 SSQL1113 Sem 11 Sesi 2022 2023Document20 pagesTopic 4 SSQL1113 Sem 11 Sesi 2022 2023HUSNA NADEELA BINTI HUSSAIN MoeNo ratings yet
- Matematik Perniagaan - PB-1Document17 pagesMatematik Perniagaan - PB-1TAECHIM.l.0% (1)
- Okky Indra Prawirayuda 09040722061 AsttDocument5 pagesOkky Indra Prawirayuda 09040722061 AsttnanaNo ratings yet
- Post-Mortem SK SerdangDocument8 pagesPost-Mortem SK Serdangkhoirulnizam75No ratings yet
- EXCEL Perhitungan PembesianDocument12 pagesEXCEL Perhitungan PembesianJefri100% (1)
- Presentation Math GRP 1Document26 pagesPresentation Math GRP 1MOHAMAD FIRDAUS BIN KHAIRUL NIZAT MoeNo ratings yet
- Analisis Headcount Math Mengikut DarjahDocument6 pagesAnalisis Headcount Math Mengikut DarjahAmySharizaBtAllauddinNo ratings yet
- 2022 Pengisian Amalan Baik 2022 Sehingga 7 Jun 2022Document16 pages2022 Pengisian Amalan Baik 2022 Sehingga 7 Jun 2022Uminurain YusofNo ratings yet
- Contoh Perhitungan Lentur, Tarik Dan TekanDocument7 pagesContoh Perhitungan Lentur, Tarik Dan TekanDana Guna SatrioNo ratings yet
- Tabel Pengisian Bahan Peledak Pada Lokasi N4 Floor T115Document4 pagesTabel Pengisian Bahan Peledak Pada Lokasi N4 Floor T115Indah Putrika RezkyNo ratings yet
- Contoh Statistika LihatDocument2 pagesContoh Statistika LihatAlis wandiNo ratings yet
- Grid Contoh Soal 2 Edit 061022 - Tgs 3Document43 pagesGrid Contoh Soal 2 Edit 061022 - Tgs 3Nabila FairuzNo ratings yet
- Aturan Simpson 3Document1 pageAturan Simpson 3Andre MulanaNo ratings yet
- Analisis Headcount Mata Pelajaran Mengikut DarjahDocument67 pagesAnalisis Headcount Mata Pelajaran Mengikut Darjahnoraisa isaNo ratings yet
- TUGASDocument8 pagesTUGASIne Nadia AprilianiNo ratings yet
- Tugas 51Document6 pagesTugas 51radssNo ratings yet
- Tugas 2 Hidrodinamika - SLTM - Muhammad Hafidh Pramudana - 043118400000048Document52 pagesTugas 2 Hidrodinamika - SLTM - Muhammad Hafidh Pramudana - 043118400000048muhammad hafidhNo ratings yet
- 50 Soal LCCMDocument39 pages50 Soal LCCMDeni ElendraNo ratings yet
- Rencanakan Komponen Struktur TekanDocument3 pagesRencanakan Komponen Struktur TekanAdindafitritamarsiNo ratings yet
- Kuda KudaDocument9 pagesKuda KudaReiza GinanjarNo ratings yet
- Tugas BetonDocument9 pagesTugas Betonfaza izbikNo ratings yet
- UAS Helsa StatistikDocument8 pagesUAS Helsa StatistikHelsa Feby KurniaNo ratings yet
- Tugas Fisika Abdul Rahim& RAGILDocument8 pagesTugas Fisika Abdul Rahim& RAGILM FandilaNo ratings yet
- Jundi Ihsan Perancangan AbsorberDocument15 pagesJundi Ihsan Perancangan AbsorberJundi IhsanNo ratings yet
- Calculation FinalDocument12 pagesCalculation FinalFadzir AmirNo ratings yet
- Teknik Darab Kekisi Dan Bahagi Suur 2Document5 pagesTeknik Darab Kekisi Dan Bahagi Suur 2Harliza Mohamad ArifinNo ratings yet
- Analisis Percubaan SPM 2020 (LKTW)Document27 pagesAnalisis Percubaan SPM 2020 (LKTW)SitiRohimahMahmadRejabNo ratings yet
- Bahagi 02Document8 pagesBahagi 02Wan AizatulNo ratings yet
- T ParlayDocument2 pagesT ParlayDeri LugianaNo ratings yet
- PF Marketing Rate A4 FINALDocument1 pagePF Marketing Rate A4 FINALSyaharawi IshakNo ratings yet
- Geometrik JalanDocument2 pagesGeometrik JalanRzky KyyNo ratings yet
- TUGAS 3 Hari Pratama Sura 170405002 Termodinamika TK IIDocument8 pagesTUGAS 3 Hari Pratama Sura 170405002 Termodinamika TK IIsultan akbar100% (1)
- Perhitungan Manual ANOVA 1Document4 pagesPerhitungan Manual ANOVA 1Risky AndreasNo ratings yet
- Worksheet Matematika IDocument7 pagesWorksheet Matematika IWellyanto Randuklangi'No ratings yet
- Form Bab 9 TabelDocument3 pagesForm Bab 9 TabelRizaNo ratings yet
- Jawapan Latihan 3BDocument6 pagesJawapan Latihan 3BSITI NURSYAKIRAH BINTI ZAINUDDINNo ratings yet
- Bor Layanan 2019Document1 pageBor Layanan 2019N S FazriNo ratings yet
- Laporan MingguanDocument21 pagesLaporan MingguanAbdi ParintakNo ratings yet
- Perhitungan Neraca Panas Evaporator1Document3 pagesPerhitungan Neraca Panas Evaporator1panzurliNo ratings yet
- Tabel-T SementaraDocument8 pagesTabel-T SementaraAjmila SalsabilaNo ratings yet
- DKH MandaongDocument175 pagesDKH Mandaongnanank utomoNo ratings yet
- PR StatisikDocument4 pagesPR Statisikprilya lintangNo ratings yet
- Contoh Perhitungan Proyeksi Penduduk +kebutuhan AirDocument11 pagesContoh Perhitungan Proyeksi Penduduk +kebutuhan Airnuelsrg2303No ratings yet
- Ketengikan MinyakDocument9 pagesKetengikan Minyakellen cristyNo ratings yet
- Metode Numerik - Interpolasi KubikDocument4 pagesMetode Numerik - Interpolasi KubikFajrin Siddiq100% (2)
- Laporan Struktur Statis Tak TentuDocument35 pagesLaporan Struktur Statis Tak TentuAzyumarni Azra Hanifah HanifahNo ratings yet
- Sifir BahagiDocument12 pagesSifir BahagiNoor ArinahNo ratings yet