Professional Documents
Culture Documents
Solução saturada de ácido bórico
Uploaded by
Alex Cardozo0 ratings0% found this document useful (0 votes)
3K views3 pagesOriginal Title
Lista de exercícios de química 3 ano
Copyright
© Attribution Non-Commercial (BY-NC)
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
3K views3 pagesSolução saturada de ácido bórico
Uploaded by
Alex CardozoCopyright:
Attribution Non-Commercial (BY-NC)
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 3
LISTA DE EXERCÍCIOS DE Adicionando-se 200g de H3BO3
QUÍMICA em 1,00kg de água, a 20°C,
quantos gramas do ácido restam
1) Uma solução saturada de na fase sólida?
nitrato de potássio (KNO3)
constituída, além do sal, por 4) O gráfico adiante mostra a
100g de água, está à solubilidade (S) de K2Cr2O7 sólido
temperatura de 70°C. Essa em água, em função da
solução é resfriada a 40°C, temperatura (t). Uma mistura
ocorrendo precipitação de parte constituída de 30g de K2Cr2O7 e
do sal dissolvido. Calcule: 50g de água, a uma temperatura a) Qual a menor quantidade de A partir da análise desse gráfico,
a) a massa do sal que precipitou. inicial de 90°C, foi deixada água necessária para dissolver é CORRETO afirmar que os dois
b) a massa do sal que esfriar lentamente e com completamente, a 60°C, 120g de sistemas em que há precipitado
permaneceu em solução. A agitação. A que temperatura B? são:
seguir, o gráfico da solubilidade aproximada deve começar a b) Qual a massa de A necessária a) I e II. c) IV e V.
do nitrato de potássio em função cristalizar o K2Cr2O7? para preparar, a 0°C, com 100g b) I e III. d) V e VI.
da temperatura. de água, uma solução saturada
(I) e outra solução insaturada 7) Uma solução contendo 14g de
2) A 10°C a solubilidade do (II)? cloreto de sódio dissolvidos em
nitrato de potássio é de 200mL de água foi deixada em
20,0g/100g H‚O. Uma solução 6) Seis soluções aquosas de um frasco aberto, a 30°C. Após
contendo 18,0g de nitrato de nitrato de sódio, NaNO3, algum tempo, começou a
potássio em 50,0g de água a numeradas de I a VI, foram cristalizar o soluto. Qual volume
25°C é resfriada a 10°C. Quantos preparadas, em diferentes mínimo e aproximado, em mL,
gramas do sal permanecem temperaturas, dissolvendo-se de água deve ter evaporado
dissolvidos na água? diferentes massas de NaNO3 em quando se iniciou a cristalização?
a) 25°C d) 70°C 100g de água. Em alguns casos, Dados: solubilidade, a 30°C, do
3) Considere o gráfico, b) 45°C e) 80°C o NaNO3 não se dissolveu cloreto de sódio = 35g/100g de
representativo da curva de c) 60°C completamente. Este gráfico água; densidade da água a 30°C
solubilidade do ácido bórico em representa a curva de = 1,0g/mL.
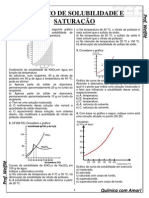
água. 5) Observe o gráfico a seguir e solubilidade de NaNO3, em a) 20. d) 100.
responda às questões que se função da temperatura, e seis b) 40. e) 160.
seguem. pontos, que correspondem aos c) 80.
sistemas preparados:
8) A solubilidade do oxalato de
cálcio a 20°C é de 33,0 g por 100
g de água. Qual a massa, em
gramas, de CaC2O4 depositada
no fundo do recipiente quando
100 g de CaC2O4(s) são
adicionados em 200 g de água a
20°C?
utilizando dicromato de potássio
9) A curva do gráfico a seguir sólido e água pura em diferentes
mostra a solubilidade de um temperaturas, conforme o
certo soluto em água. esquema:
( ) a situação B aconteceria
caso a solução inicial fosse
insaturada;
( ) a situação B aconteceria
caso a solução inicial fosse
saturada;
* salmoura = solução aquosa ( ) a situação A ocorreria caso a
saturada de cloreto de sódio solução inicial fosse saturada;
Ao final de uma eletrólise de ( ) ocorreria o demonstrado em
Responda às perguntas a seguir, Após a estabilização dessas salmoura, retiraram-se da cuba C caso a solução inicial estivesse
justificando sua resposta. misturas, o número de sistemas eletrolítica, a 90 °C, 310 g de supersaturada;
a) Qual ou quais dos pontos do homogêneos e o número de solução aquosa saturada tanto ( ) caso a solução inicial
gráfico representam uma sistemas heterogêneos formados de cloreto de sódio quanto de estivesse insaturada,
solução saturada homogênea? correspondem, respectivamente, clorato de sódio. Essa amostra poderíamos observar a situação
b) Indique em que pontos do a: foi resfriada a 25 °C, ocorrendo a A após a adição do cristal.
gráfico existem soluções a) 5 – 1 c) 3 – 3 separação de material sólido.
saturadas heterogêneas. b) 4 – 2 d) 1 – 5 13) Adicionou-se 1,360 g de
c) Através do conceito de a) Quais as massas de cloreto de sulfato de cálcio a 200 mL de
solução insaturada, aponte no 11) Industrialmente, o clorato de sódio e de clorato de sódio água, obtendo-se uma solução X.
gráfico o(s) ponto(s) onde esta sódio é produzido pela eletrólise presentes nos 310 g da amostra O sólido não dissolvido foi
situação ocorre. da salmoura* aquecida, em uma retirada a 90 °C? Explique. separado por filtração e, depois
d) Que procedimentos podem cuba eletrolítica, de tal maneira b) No sólido formado pelo de seco, pesado. Quantos
ser utilizados para precipitar que o cloro formado no anodo se resfriamento da amostra a 25 °C, gramas de sulfato de cálcio são
(cristalizar) parte do soluto da misture e reaja com o hidróxido qual o grau de pureza (% em recuperados depois da filtração?
solução D, sem alterar as de sódio formado no catodo. A massa) do composto presente a) 1,224 g d)
quantidades do solvente e do solução resultante contém em maior quantidade? 0,136 g
soluto da referida solução? cloreto de sódio e clorato de c) A dissolução, em água, do b) 1,360 g e)
sódio. clorato de sódio libera ou 1,088 g
10) O gráfico a seguir, que absorve calor? Explique. c) 5,10 g
mostra a variação da 2NaCl(aq) + 2H2O(l) Cl2(g) + Massa molar (g/mol): CaSO4 =
solubilidade do dicromato de 2NaOH(aq) + H2(g) 12) Um único cristal de um 136; solubilidade do CaSO4 =
potássio na água em função da sólido é adicionado a um béquer 5.10–3 mol/L de água
temperatura, foi apresentado em 3Cl2(g) + 6 NaOH(aq) 5NaCl(aq) + contendo uma solução
uma aula prática sobre misturas NaClO3(aq) + 3H2O(l) daquele mesmo sólido. 14) A 50ºC o coeficiente de
e suas classificações. Em Considerando as situações solubilidade do NaCl é 37 g de
seguida, foram preparadas seis abaixo, é correto afirmar que: NaCl por 100 g de H2O; a 100°C
misturas sob agitação enérgica, é de 39,8g de NaCl por 100 g de
H2O. A figura abaixo ilustra a
dissolução de 39g de NaCl em
100 g de H2O a 100°C.
Após o exame do quadro,
considere
as afirmações:
Deixando-se o sistema resfriar I. A solução aquosa B, de
em repouso absoluto até 50°C, concentração 488 g/L, deixa de
todo o NaCl continua dissolvido. ser saturada quando aquecida a
Acrescentando ao sistema um 60ºC.
cristal de NaCl (germe de II. Nem todas as substâncias são
precipitação) ocorre a mais solúveis em água mais
precipitação de 2,0 g de NaCl. quente.
I, II e III são, respectivamente, III. A uma dada temperatura, o
soluções: coeficiente de solubilidade de
a) supersaturada, insaturada, um soluto é a quantidade
saturada máxima que se dissolve numa
b) insaturada, supersaturada, quantidade padrão de solvente.
saturada IV. A solubilidade de uma
c) saturada, supersaturada, substância em determinado
insaturada solvente independe da
d) insaturada, saturada, temperatura.
supersaturada É certo concluir que:
a) apenas a I e a II estão
15) Em algumas situações do corretas; d) apenas a II e a IV
dia-a-dia, pode-se perceber que estão corretas;
a solubilidade de uma substância b) apenas a I e a III estão
numa massa fixa de solvente corretas; e) apenas a III e a IV
depende das condições do meio. estão corretas.
Em função desse fato, é possível c) apenas a II e a III estão
construir quadros que corretas;
relacionam a solubilidade de
uma substância a temperaturas
diferentes.
Examine o quadro a seguir:
You might also like
- Exercícios de Soluções - Profº Agamenon RobertoDocument39 pagesExercícios de Soluções - Profº Agamenon Robertocb_penatrujillo56% (18)
- BetoneiraDocument31 pagesBetoneiraGiuliano ArzamendiaNo ratings yet
- Relatório sobre a Máquina de AtwoodDocument14 pagesRelatório sobre a Máquina de Atwoodrodrigo_alves_55No ratings yet
- Exercicios de Coeficiente de Solubilidade PDFDocument4 pagesExercicios de Coeficiente de Solubilidade PDFLeandro Mendes HappatschNo ratings yet
- Cbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaDocument79 pagesCbae4ae1 Db5c 4fc9 8184 5115d78789b8 Fisico QuimicaNina Bob Brown100% (1)
- 2-Relatório ExperimetosDocument6 pages2-Relatório ExperimetosMarcelo Oliveira Melo100% (1)
- Exercicios de COEFICIENTE DE SOLUBILIDADE e SoluçõesDocument26 pagesExercicios de COEFICIENTE DE SOLUBILIDADE e Soluçõeslardiao0% (1)
- Estados físicos da matériaDocument2 pagesEstados físicos da matériasilfisica100% (2)
- Geometria Analítica e Álgebra Linear: Produto EscalarDocument28 pagesGeometria Analítica e Álgebra Linear: Produto EscalarFelipe RomoliniNo ratings yet
- Prensa HidráulicaDocument9 pagesPrensa HidráulicaArtaxerxes Saint'sNo ratings yet
- Química: 3 Lista de ResoluçãoDocument5 pagesQuímica: 3 Lista de ResoluçãoJader Pereira de AraujoNo ratings yet
- aula de resolução de questões soluções quimicasDocument5 pagesaula de resolução de questões soluções quimicasi46555497No ratings yet
- Alista 16 - Solucoes I A Solubilidade Das SubstanciasDocument7 pagesAlista 16 - Solucoes I A Solubilidade Das SubstanciasHeitorNo ratings yet
- Exercicios de Coeficiente de SolubilidadeDocument4 pagesExercicios de Coeficiente de SolubilidadeJardson Ramos SilvaNo ratings yet
- LE - Dispersão e SolubilidadeDocument3 pagesLE - Dispersão e SolubilidadeMatheus PetryNo ratings yet
- ListaExercíciosQuímicaSoluçõesDocument5 pagesListaExercíciosQuímicaSoluçõesAna Ester CavalcanteNo ratings yet
- Lista de Exercícios - SolubilidadeDocument3 pagesLista de Exercícios - Solubilidadealexchacal100% (2)
- Exercicios de SolubilidadeDocument6 pagesExercicios de Solubilidadesua mae de 4No ratings yet
- Lista de SolubilidadeDocument2 pagesLista de SolubilidadeRtyu IuytNo ratings yet
- 16 SolubilidadeDocument7 pages16 SolubilidadeFRANKE MERO TESTENo ratings yet
- Solubilidade de saisDocument4 pagesSolubilidade de saisCleber SerafinNo ratings yet
- Exercicios Coeficiente de SolubilidadeDocument4 pagesExercicios Coeficiente de SolubilidadeAndré Luís Della VolpeNo ratings yet
- Solubilidade Das Soluções PDFDocument10 pagesSolubilidade Das Soluções PDFreykonpalNo ratings yet
- Fisico Quimica Solubilidade Exercicios Gabarito PDFDocument10 pagesFisico Quimica Solubilidade Exercicios Gabarito PDFEmerson JuniorNo ratings yet
- Química Lista de ExercíciosDocument4 pagesQuímica Lista de Exercícioshtq87rbdjgNo ratings yet
- 1a Lista de Exercicios de Fisico Quimica !Document2 pages1a Lista de Exercicios de Fisico Quimica !Bruna RomeroNo ratings yet
- Graficos Solubilidade 2 Ano 2Document1 pageGraficos Solubilidade 2 Ano 2lopesqui1766No ratings yet
- 16 SolubilidadeDocument6 pages16 SolubilidadeEverton FisicoNo ratings yet
- Exercícios Físico-Química SolubilidadeDocument3 pagesExercícios Físico-Química SolubilidadeAlfredo Sahade VespaNo ratings yet
- Solucoes PDFDocument15 pagesSolucoes PDFThiago Magno Tavares Machado100% (1)
- Lista de exercícios sobre solubilidade e concentraçãoDocument6 pagesLista de exercícios sobre solubilidade e concentraçãoFarmacia Artur NogueiraNo ratings yet
- Solubilidade Sal KNO3Document8 pagesSolubilidade Sal KNO3Rafael MottaNo ratings yet
- DispersõeDocument5 pagesDispersõeHelton ClistenesNo ratings yet
- Solubilidade e curvas de solubilidadeDocument19 pagesSolubilidade e curvas de solubilidadeJoão PauloNo ratings yet
- Lista SoluçoesDocument2 pagesLista SoluçoesVitor GabrielNo ratings yet
- CoeficienteDocument12 pagesCoeficienteOtoazevedo OtoazevedoNo ratings yet
- Coeficiente de SolubilidadeDocument5 pagesCoeficiente de SolubilidadeRubia MariathNo ratings yet
- Coeficientes de solubilidade e concentrações de soluçõesDocument6 pagesCoeficientes de solubilidade e concentrações de soluçõesÉrica LimaNo ratings yet
- Solução aquosa saturada de saisDocument4 pagesSolução aquosa saturada de saisMarko Aurelio Ferreira Da CostaNo ratings yet
- Coeficiente de solubilidade de saisDocument48 pagesCoeficiente de solubilidade de saisandreik83100% (1)
- Solubilidade de saisDocument4 pagesSolubilidade de saisEng Renato De Marchi Vieira Dos SantosNo ratings yet
- Lista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesDocument2 pagesLista de Exercicios 12 - Revisao para A 2 Avaliacao - Hidrolise Salina e Solubilidade - 3 Bimestre 2013 - 3 SeriesJosimar Lima FerreiraNo ratings yet
- Fisico Quimica Solubilidade ExerciciosDocument10 pagesFisico Quimica Solubilidade ExerciciosRubia MariathNo ratings yet
- Lista 1 QG 1-19Document6 pagesLista 1 QG 1-19schottbpNo ratings yet
- Lista Solubilidade BásicoDocument3 pagesLista Solubilidade BásicoProf. Maych Melo QuímicaNo ratings yet
- Lista+de+exercícios+para+1 +prova+Quimica+AnalíticaDocument5 pagesLista+de+exercícios+para+1 +prova+Quimica+Analíticabenedito.nasaNo ratings yet
- 31-Soluções e SolubilidadeDocument4 pages31-Soluções e Solubilidadenv77vnm100% (2)
- Curva de SolubilidadeDocument5 pagesCurva de Solubilidadealexchacal100% (2)
- Atividade 5 de Abril - Pré ProvaDocument5 pagesAtividade 5 de Abril - Pré ProvaAlfredo Sahade VespaNo ratings yet
- Coeficiente de Solubilidade e Tipos de SaturaçãoDocument5 pagesCoeficiente de Solubilidade e Tipos de SaturaçãoWelff Junior100% (2)
- Solubilidade de sais: conceitos e curvas de solubilidadeDocument12 pagesSolubilidade de sais: conceitos e curvas de solubilidadeCarolynne MourãoNo ratings yet
- Apostila QUÍMICA Com GabaritoDocument39 pagesApostila QUÍMICA Com GabaritoMichelle Alkmim50% (2)
- Lista de Exercicio de Quimica Introducao As SolucoesDocument3 pagesLista de Exercicio de Quimica Introducao As SolucoesEtiany Oliveira SantosNo ratings yet
- Atividade (Sol)Document2 pagesAtividade (Sol)rafael andradeNo ratings yet
- Lista de Exerc DensidadeDocument6 pagesLista de Exerc DensidadeRtyu IuytNo ratings yet
- ExercÍcios de To em QuÍmicaDocument4 pagesExercÍcios de To em QuÍmicaanon-585283No ratings yet
- Solubilidade de sais e açúcares: curvas e fatores que influenciamDocument22 pagesSolubilidade de sais e açúcares: curvas e fatores que influenciamRebecaNo ratings yet
- Exercícios 1 de SoluçõesDocument3 pagesExercícios 1 de SoluçõesMatheus HenriqueNo ratings yet
- Estudo Das Solucoes Coeficiente de SolubilidadeDocument13 pagesEstudo Das Solucoes Coeficiente de SolubilidadeGildo Silva100% (1)
- Solubilidade de sais e efeitos da temperaturaDocument10 pagesSolubilidade de sais e efeitos da temperaturaLuana GregórioNo ratings yet
- Solubilidade e curvas de solubilidadeDocument2 pagesSolubilidade e curvas de solubilidadethata_vilarinhoNo ratings yet
- Soluções saturadas de sais: propriedades e aplicaçõesDocument2 pagesSoluções saturadas de sais: propriedades e aplicaçõesromezioh7716No ratings yet
- Curvasde SolubilidadeDocument2 pagesCurvasde SolubilidadeMarcos AurelioNo ratings yet
- Manual de Instruções Pressostato B700Document5 pagesManual de Instruções Pressostato B700Mariano MacchiNo ratings yet
- Forças concorrentesDocument8 pagesForças concorrentesJ.a. Pindula PindulaNo ratings yet
- Seletividade entre proteções elétricasDocument2 pagesSeletividade entre proteções elétricasJoão Marcelo T HNo ratings yet
- Valvula Rec Vapores 0413Document2 pagesValvula Rec Vapores 0413Juliano André PetryNo ratings yet
- Estudo dos Movimentos: Ponto Material, Corpo Extenso e ReferencialDocument26 pagesEstudo dos Movimentos: Ponto Material, Corpo Extenso e ReferencialLukas100% (1)
- EVDocument10 pagesEVWillian100% (1)
- Movimento 1D e 2D: lista de atividades em sala de aula sobre cinemáticaDocument1 pageMovimento 1D e 2D: lista de atividades em sala de aula sobre cinemáticakkodelNo ratings yet
- Engrenagens Sem-Fim UFMGDocument38 pagesEngrenagens Sem-Fim UFMGTúlioBorelNo ratings yet
- GeometriaDocument14 pagesGeometriaJoseMarquesNo ratings yet
- Jogo de Pitoco - Manual Regras e UsoDocument2 pagesJogo de Pitoco - Manual Regras e UsoJogo de Pitoco100% (2)
- Relatório EspelhoDocument7 pagesRelatório EspelhoHigor Araújo Dos AnjosNo ratings yet
- Problemas Praticas ACE 2019Document13 pagesProblemas Praticas ACE 2019Rui DiasNo ratings yet
- Estabilização de solos argilosos com aditivo químicoDocument17 pagesEstabilização de solos argilosos com aditivo químicoMarcelo Hotta100% (1)
- Aula 1 - Reatores Homogêneos e HeterogêneosDocument110 pagesAula 1 - Reatores Homogêneos e HeterogêneosFENFOG100% (1)
- Preparação do acetato de n-butilaDocument7 pagesPreparação do acetato de n-butilaKaká GerminoNo ratings yet
- Para Preparar e Administrar MedicamentosDocument3 pagesPara Preparar e Administrar MedicamentosDenise FernandesNo ratings yet
- Projeto de blocos de transição em concreto armadoDocument13 pagesProjeto de blocos de transição em concreto armadoAdriano RodriguesNo ratings yet
- Usinagem de VirabrequimDocument4 pagesUsinagem de Virabrequimbacalhaucsb0% (1)
- Dimensionamento de Condutores ElétricosDocument58 pagesDimensionamento de Condutores ElétricosCicero MelloNo ratings yet
- Aula DRXDocument43 pagesAula DRXCarolina de OliveiraNo ratings yet
- Guia rápido do manual do proprietárioDocument236 pagesGuia rápido do manual do proprietárioFélix FerreiraNo ratings yet
- 11FQA Ficha Formativa F1.1 MECANICADocument3 pages11FQA Ficha Formativa F1.1 MECANICAFilipa SantosNo ratings yet